Publicado el 1 de enero de 2010 | http://doi.org/10.5867/medwave.2011.01.4839
Microbiología de las heridas y toma de cultivo
Microbiology of wounds and culture
Resumen
Esta exposición se dan en el contexto de la versión 2010, del postítulo de manejo de heridas y úlceras, realizado por el instituto Nacional de Heridas, y que tiene como objetivo realizar una actualización del tratamiento de heridas complejas y crónicas.
Introducción
Existe una flora comensal cutánea residente y otra transitoria, es decir, el cuerpo humano no es estéril, hay bacterias sobre la piel y en las capas más profundas que corresponden, en general, a bacterias aeróbicas y anaeróbicas.
La flora cutánea residente es constante, de baja patogenicidad, no se asocia a infecciones, su composición depende del sitio anatómico correspondiente. En algunos sitios hay Pseudomonas y en otros algún tipo de Staphylococcus epidermidis.
Entre los agentes más comunes se identifican:
Aerobios
- Staphylococcus coagulasa negativa.
- Corynebacterium SP.
- Micrococcus SP.
- Streptococcus viridans.
Anaerobios
- Peptostreptococcus.
- Propionibacterium.
Todos estos microorganismos son de la flora residente, por lo que en general no son patogénicos.
Interpretación del cultivo
En general en Chile, los cultivos que se hacen son “cualitativos”. Los cultivos cuantitativos son de alto costo y deberían estar sólo indicados para las quemaduras infectadas, en donde la única solución para identificar el germen responsable es mediante un cultivo cuantitativo.
Flora cutánea transitoria
Existe una flora cutánea transitoria de la que habitualmente el equipo de salud es responsable (específicamente en el caso del Staphylococcus aureus) la que se transmite a través de las manos del personal. Se ha visto que los pacientes hospitalizados ya presentan colonización a los tres días, por lo que actualmente se da mucha importancia a acortar la duración de las hospitalizaciones.
El Staphylococcus aureus habitualmente se elimina con agua y por eso el lavado de manos tiene importancia para efectos de la prevención de infecciones intrahospitalarias.
Otros colonizadores de la piel son el Streptococcus Grupo A, enterobacterias, el Acinetobacter, y la Pseudomona, residente en la zona genital pero que en cierta ocasiones puede encontrarse transitoriamente en otras zonas, por ejemplo en las ulceras venosas.
Colonización e infección
La colonización es la presencia y/o multiplicación de microorganismos patógenos sin respuesta clínica y/o inmunológica; es transitoria y no invasiva. Sin embargo, en algunas condiciones se puede transformar en patógena.
La infección es la presencia y/o multiplicación de microorganismos con respuesta clínica y/o inmunológica. En el caso del Staphylococcus aureus, el aumento en su número puede asociarse a presencia de sintomatología de infección.
Infección de heridas
Los pacientes portadores de una herida se pueden infectar por vía endógena u exógena. La vía endógena es la flora, la piel, la mucosa, el “foco a distancia”; por eso es importante que, cuando se realiza una cirugía electiva, el paciente no debe tener caries ni estar resfriado entre otras.
Participando de la vía exógena se encuentra el personal de salud, como primera línea. Los antisépticos también son elementos potencialmente altamente contaminados por el mal manejo de ellos, así como el instrumental que se utiliza en los pacientes.
La probabilidad de infección depende de la localización anatómica de la lesión; así, la extremidad inferior es más alta la probabilidad que la extremidad superior.
Los mecanismos de producción de una herida también tienen importancia, por ejemplo un trauma, una mordedura, una quemadura, un corte, una punción, una lesión vascular, una cirugía en general. La evolución de la herida será diferente dependiendo del cómo se produjo la misma.
El tipo morfológico de la lesión y las características del paciente son también elementos importantes a considerar. Mecanismos causales de infección pueden ser el estado inmunológico del paciente (si es inmunodeprimido), tratamientos con corticoides, con radioterapia o con largos períodos con antibióticos.
El estudio microbiólogico permite confirmar la causa de la infección, orientar la terapia antimicrobiana, conocer el reservorio y la vía de infección, y determinar conducta clínica a seguir con el paciente.
Herida crónica o úlcera
La úlcera es una lesión cuya cicatrización es más tórpida. En este caso, la toma de muestra para cultivo es de un trozo de tejido con cureta, pinza o bisturí. Muchos microbiólogos y tecnólogos médicos que trabajan en microbiología no reciben muestras tomadas con tórula cuando deben informar una úlcera venosa, porque lo único que encuentran son gérmenes colonizadores.
En consecuencia, el cultivo de una ulcera en general se realiza con un trozo de tejido que no debe ser esfacelado ni necrótico para evitar la presencia de detritus y gérmenes muertos.
Toma de muestra
La toma de la muestra es el procedimiento mediante el cual se obtiene el tejido o fluido para estudio microbiológico. La calidad de la muestra debe ser confiable, y la interpretación del resultado del estudio microbiológico depende de la calidad de la muestra.
Normas generales. Se debe preparar el sitio de obtención lavando la herida con suero y por arrastre mecánico. Usar material estéril y técnica aséptica. El volumen de la muestra en general es pequeño; un trozo de tejido puede fluctuar entre 1 y 5 gramos (equivalente al tamaño de una lenteja). La muestra óptima consta de fluidos y tejido. La técnica óptima para tomar fluido es la punción y la aspiración. Si se emplean tórulas, se deben colocar en medio de transporte ya que el cuerpo humano tiene un gran porcentaje de agua, medio en el cual viven bacterias y gérmenes en general; si se envía una tórula seca, los microorganismos se mueren rápidamente. Las tórulas se deben colocar de inmediato en medio de transporte; si no es posible, enviar en tubo estéril con suero fisiológico antes de 30 minutos al laboratorio.
El cultivo Stuart es un medio de transporte que se utiliza en muestras que potencialmente contengan gérmenes aerobios. Una vez tomada la muestra, el tiempo de duración es de 24 horas a temperatura ambiente. No es necesario otro tipo de medidas como acercar a calor o frío.
No se deben tomar muestras de pus ya que éste contiene células muertas y el líquido acidifica rápidamente, provocando la muerte de todas las otras bacterias. Por lo tanto, es importante el arrastre antes de tomar el cultivo. Para el lavado se debe usar un suero tibio.
Uso de antibióticos
Antes, a los pacientes en tratamiento con antibióticos se les indicaba suspender el tratamiento por 48 horas, tomar la muestra, y reinstituir el tratamiento. Hoy en día se recomienda que el paciente continúe con el tratamiento antibiótico, pero lo fundamental es que el microbiólogo sepa qué antibiótico está tomando, en qué dosis y cuántos días.
Cultivo aeróbico
Se pueden clasificar los cultivos en aeróbicos y anaeróbicos, para cada uno hay medios de transporte distintos. Para los cultivos aeróbicos el medio es el Stuart.
El medio de cultivo Stuart contiene: agar-agar, un buffer y agua
Procedimiento para la toma de muestra
Si corresponde a una herida, se lava, se desliza la tórula humedecida sobre los bordes de ésta en forma de zig-zag (Figura 1) y se finaliza en la zona central.
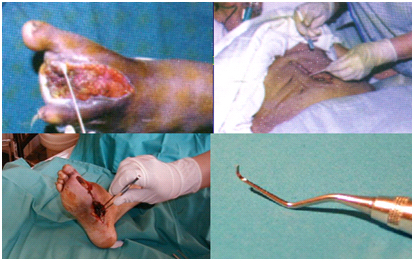 Tamaño completo
Tamaño completo Si la herida es profunda también se debe lavar, se toma la muestra de la parte más profunda.
En el caso de tomar un cultivo de úlcera, se debe lavar y extraer un trozo de tejido viable, es decir que no contenga tejido necrótico o esfacelado.
La toma de un trozo de tejido se puede realizar con curetas (Figura 1) utilizadas por los dentistas, que son bastante buenas para extraer trozos de tejido; también se puede utilizar una tijera de punta curva, un bisturí, o también pinza quirúrgicaque le permitan raspar y sacar un trozo de tejido.
Algunas recomendaciones ya comentadas: arrastre mecánico previo a la toma de muestra; retiro de tejido esfascelado o necrótico; la tórula debe estar húmeda y el medio de transporte en buen estado (cerrado, sellado y estéril) y no debe estar un tiempo mayor de 24 horas, una vez tomada la muestra
Cultivo anaeróbico
El estándar nacional para tomar el cultivo anaeróbico es un “caldo de cultivo”. La diferencia con el medio de transporte es que tiene sustancias y elementos enriquecidos que permiten que el tiempo de duración de las bacterias sea más largo, serán cultivadas, y se seguirán reproduciendo. En cambio en el otro sólo se hace el transporte, sin permitir que las bacterias se reproduzcan.
El caldo de cultivo llamado tioglicolato, es el que seutiliza en los hemocultivos, corresponde a sustancias reductoras.
El cultivo anaeróbico se puede adquirir de varias formas. Una forma es mediante la toma de un trozo de tejido por lavado al igual que el cultivo aerobio. Así, se obtiene un tejido viable y se coloca en tioglicolato. Otra manera es la extracción de líquido con una jeringa. También se puede obtener la muestra con una tórula humedecida en la zona más profunda de la lesión.
Para que sea efectivo, el caldo de cultivo debe estar sellado al vacío ya que los anaerobios viven en un medio sin oxígeno. Al abrir la tapa ingresa el oxígeno, por lo que la toma de muestra se puede hacer en forma conjunta. Por ejemplo, si se tiene un trozo de tejido, éste se frota por las paredes del frasco.
En el caso de un absceso (Figura 2a), idealmente se punciona el absceso con una jeringa y lo extraído se transporta en tioglicolato. Si no hay medio de transporte, la misma jeringa se envía al laboratorio, antes de 30 minutos.
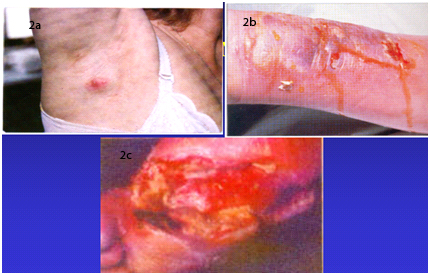 Tamaño completo
Tamaño completo En las celulitis o flegmones (Figura 2b), en que habitualmente no es posible extraer nada por punción, se recomienda que se limpie la zona de igual forma que en los abscesos, y se utiliza una jeringa y una aguja que dependerá de la zona a puncionar y la edad del paciente. Se inyecta solución fisiológica (en niños menores de 2 años se utiliza agua bidestilada y en mayores de 2 años entre 0,5 y 1 cc de solución fisiológica), y sin retirar la aguja se aspira para hacer un barrido. Este procedimiento se debe realizar en cantidades pequeñas ya que de lo contrario se corre el riesgo de expandir las bacterias.
La orden médica debe indicar el nombre del paciente, el número de la ficha clínica, la identificación del establecimiento, el tipo de cultivo (aerobio, anaerobio o combinado), ubicación anatómica del cultivo, la fecha y la hora de la toma de muestra, la identificación del médico solicitante, el diagnostico clínico, y si el paciente está o no en tratamiento con antimicrobianos. El rótulo del tubo debe contener: nombre del paciente, número de ficha clínica, el tipo de muestra, la fecha y hora de su obtención. Estas son las recomendaciones desde el punto de vista microbiológico que solicitan para que la evaluación se realice de manera óptima.

