Congresos
← vista completaPublicado el 1 de octubre de 2005 | http://doi.org/10.5867/medwave.2005.09.1205
Antagonistas TNF alfa en artritis reumatoídea (parte I)
TNF alpha antagonists in rheumatoid arthritis (Part I)
Resumen
Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del XIII Congreso Internacional de Reumatologia, XXV Congreso Chileno, realizado en Las Termas de Chillán entre los días 17 al 20 de noviembre de 2004. El evento fue organizado por la Sociedad Chilena de Reumatología.
Presidente del Congreso: Dr Carlos Fuentealba.
Secretario Ejecutivo: Dr Francisco Radrigán.
Presidente Comité Cientifico: Dr Miguel Gutiérrez.
Edición Científica: Dr. Francisco Radrigán.
Inmunopatología de la artritis reumatoídea
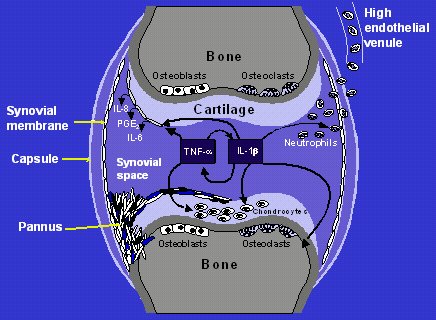
En la fase de inicio de la artritis reumatoídea (AR), la célula presentadora de antígeno activa el macrófago; éste a su vez secreta diferentes citoquinas, entre ellas IL-1 y TNF alfa, las que estimulan los sinoviocitos y condrocitos para ocasionar el daño articular. La fisiopatología de la AR se explica por una desregulación, con exceso de citoquinas proinflamatorias (TNF alfa, IL-1 e IL6) e insuficiencia de citoquinas antiinflamatorias (IL4, IL10, IL13); receptores solubles del TNF alfa, que participan en la regulación de éste; IL1Ra; receptores solubles de IL1; TIMP (Feldmann, Cell 1996; 85:307). La ruptura del equilibrio de las citoquinas lleva al desarrollo de la sinovitis y el pannus, que a su vez provoca las lesiones del hueso y del cartílago (Figura 1).
 Tamaño completo
Tamaño completo Figura 1. Citoquinas proinflamatorias y antiinflamatorias en AR (Dinarello C, Moldawer L. Proinflammatory and Anti-inflammatory Cytokines in Rheumatoid Arthritis: A Primer for Clinicians 3rd ed. Thousand Oaks, Ca, USA: Amgen Inc., 2001).
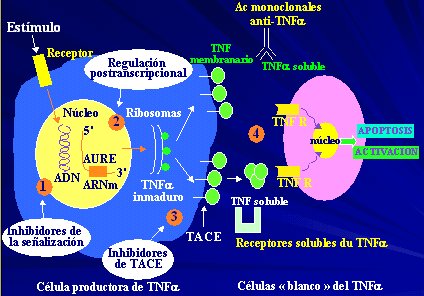
Las diferentes etapas de la síntesis, liberación y acción del TNF alfa dan origen a cinco sitios en que, teóricamente, se podría hacer intervención inmunológica anti-TNFalfa, y que son (Figura 2):
- Regulación transcripcional de la producción de TNF alfa para la fijación sobre el promotor de diferentes factores de transcripción; las dos vías principales son las del NF-kappa beta y la vía de las MAP kinasas (AP-1). Las vías de señalización dependen del tipo de estímulo y del tipo de células productoras de TNF. Inmuno-intervención: inhibidores de la señalización.
- Regulación postranscripcional de la producción de TNF alfa que se puede hacer sobre la regulación de la poliadenilación del ARN mensajero, o sobre la regulación del transporte y degradación de éste, que depende de las secuencias AURE y de las proteínas ligadoras de AURE (TTP, TIA-1, TIAR, etc.). Inmuno-intervención: inhibición de las proteínas reguladoras de las secuencias AURE.
- Regulación de la liberación proteolítica del TNF por la metaloproteinasa TACE (TNF alfa convertase enzyme). Inmuno-intervención: inhibidores de la TACE.
- Regulación de la acción celular de los TNF alfa de membrana y solubles.
- Inmuno-intervención: anticuerpos monoclonales anti-TNF alfa y receptores solubles de TNF.
- Regulación de la señalización inducida por el TNF alfa vía sus receptores TNF-R.
- Inmuno-intervención: inhibidores de la señalización.
 Tamaño completo
Tamaño completo Figura 2. Etapas de la síntesis, liberación y acción del TNF alfa.
Sin embargo, en este momento sólo se puede actuar con dos tipos de fármacos, que son los inhibidores de TNF alfa que están actualmente en uso: los receptores solubles y los anticuerpos anti TNF. Hay dos tipos de receptores: p55 y p75, y el fármaco disponible hoy es un receptor soluble de p75 (etanercept). En un individuo normal, el TNF es muy importante en la lucha contra las infecciones y la regulación se efectúa por los receptores solubles que caen a la sangre y se unen al TNF circulante, de manera que cuando se utiliza receptores solubles para tratar a los enfermos, se está utilizando un mecanismo prácticamente fisiológico.
En conclusión, existen dos alternativas posibles para inhibir la acción del TNF alfa: el receptor soluble que bloquea el TNF circulante e impide su llegada a los receptores, y los anticuerpos monoclonales que actúan sobre el TNF circulante y sobre las células. Actualmente se dispone de varias bioterapias anti TNF; hay fármacos comerciales y otros en curso de desarrollo. Entre los comerciales están el anticuerpo monoclonal quimérico Infliximab (Remicade, de Schering Plough); el anticuerpo monoclonal humano Adalimumab (Humira, de Laboratorio Abott); y el receptor soluble p75 TNF Etanercept (Enbrel, Laboratorio Wyeth).
En cuanto a las moléculas en desarrollo, están el anti-TNF fragmento Fab humanizado PEGylé (CDP 870), que ha tenido muchas dificultades y está muy atrasado, por lo que va a salir en algunos años más, si es que sale algún día, y el receptor soluble p55 PEG: PEGs TNF R1, que probablemente no va a salir todavía, porque hay muy pocos estudios con este fármaco.
Anticuerpos monoclonales
Hay dos tipos de anticuerpos monoclonales anti TNF. El primero es Infliximab, que es un anticuerpo quimérico IgG1 kappa, lo que significa que el enfermo va a reaccionar con anticuerpos, por lo que es obligatorio usarlo con otro medicamento, generalmente metotrexato. Su vida media es de diez días y se administra en perfusión lenta; se encuentra disponible en Francia desde el 1 de agosto de 2000 y es muy bien conocido. El segundo es Adalimumab D2E7, anticuerpo IgG1 totalmente humano cuya vida media es de doce días. Esta característica es importante, porque si se tiene un problema infeccioso, con una vida media de doce días la situación podría ser grave. Es muy fácil administrarlo por vía subcutánea; en Francia se encuentra disponible en los hospitales, pero no en forma comercial.
Todos los fármacos no dan el mismo resultado, hay algunas diferencias, pues algunos son más potentes que otros, pero en general se obtiene eficacia clínica y biológica en 70% de los casos. Hay que tener en cuenta que los enfermos que reciben estos medicamentos son, en su mayoría, portadores de AR grave y han recibido tres o cuatro tratamientos previos, incluso con metotrexato.
En algunos pacientes (alrededor de 15%), especialmente en niños, el resultado se ve en algunas horas o pocos días, y es realmente extraordinario. Lo primero que cambia es el estado anímico del paciente, que antes se sentía muy cansado y ahora se levanta normalmente, sin dolor; luego, en segundo lugar, mejoran las articulaciones. En algunos casos pasan varios meses antes de observar el resultado, pero en la mayoría de ellos esto ocurre en el plazo de un mes.
Lo más importante es que en ciertos enfermos, además de mejorar la calidad de vida, se observa efectos en la evolución radiográfica, algo totalmente nuevo en reumatología. Estos fármacos tienen buena tolerancia, pero hay que vigilar al enfermo, porque hay un riesgo importante de infección; además, deben ir asociados con metotrexato, lo que no es obligatorio con Etanercept (Enbrel).
Receptores Solubles
Etanercept
Entre los receptores solubles está Etanercept (Enbrel, de Wyeth-Immunex), receptor soluble de p75 acoplado a una IgG1 humana mediante ingeniería genética, por lo que también se cataloga como proteína de fusión. Su vida media es corta, de tres a cuatro días; se administra en forma subcutánea dos veces a la semana y en Europa está disponible en el comercio.
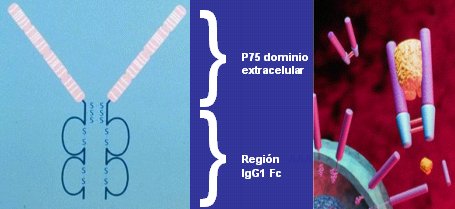
En un esquema de la estructura y del mecanismo de acción de Enbrel (Figura 3) se observa que consiste en una parte de receptor soluble y otra que es la porción Fc de la inmunoglobulina. Los receptores solubles atrapan el TNF circulante y así se inhibe la unión del TNF a la célula y la consiguiente activación celular, lo que es un efecto totalmente fisiológico.
 Tamaño completo
Tamaño completo Figura 3. Estructura y mecanismo de acción de Enbrel (etanercept).
Las indicaciones oficiales de etanercept son:
- artritis reumatoídea que no responde a metotrexato,
- AR grave, activa y evolutiva en primera intención,
- artritis idiopática juvenil,
- artritis psoriática grave, y
- espondiloartritis anquilosante.
El metotrexato es prácticamente obligatorio. Es posible utilizar de vez en cuando este tipo de fármacos en AR, como primera opción, pero se hace muy poco, debido a su alto costo. Se podría utilizar si la enfermedad parece muy activa, pero, en general, los enfermos de este tipo necesitan la asociación de Enbrel con metotrexato. En el caso de la artritis idiopática juvenil, Enbrel es el único fármaco que se puede dar a un enfermo joven, con excelentes resultados. En la artritis psoriática y la espondiloartritis anquilosante grave los resultados también son impresionantes.
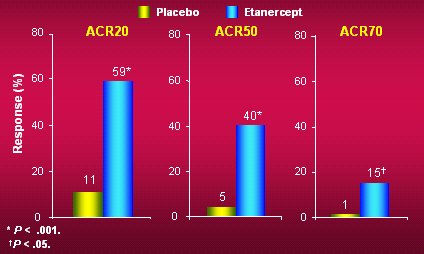
En la práctica, Enbrel es de prescripción inicial hospitalaria, al menos en Francia, por seis meses y está reservada a los especialistas de medicina interna, pediatría y reumatología. La posología es muy simple y se mantiene fija durante todo el tratamiento: en adultos, 25 mg dos veces a la semana y en el niño, 0,4 mg/kg dos veces a la semana (máximo 25 mg por inyección), con un intervalo de 3 a 4 días entre inyecciones. Como monoterapia, a los seis meses Enbrel proporciona una importante respuesta ACR 20, 50 y 70 (Moreland LW et al. Ann Intern Med 1999;130:478-486) (Figura 4). Disminuye el HAQ de 1,8 a 1, lo que realmente constituye una gran mejoría, y el efecto se mantiene durante muchos meses. La CRP baja muy rápidamente, en 8 días o menos; después se normaliza y se mantiene normal durante dos a cuatro años si no se interrumpe el tratamiento.
 Tamaño completo
Tamaño completo Figura 4. Etanercept como monoterapia: Respuesta ACR a los seis meses.
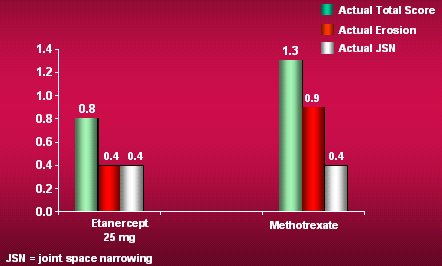
En un estudio se comparó el efecto de Enbrel con metotrexato en AR precoz, sobre la respuesta ACR a las 52 semanas y no se observó diferencias significativas. Sin embargo, en el grupo con etanercept hubo menos evolución radiográfica que con metotrexato (Figura 5). Por eso, en los casos con erosiones al inicio sería ideal administrar rápidamente un fármaco anti TNF alfa, entre los cuales etanercept es el más potente y de menos costo (EIRA-Trial with 632 patients with early RA12 months. Bathon JM et al. N Engl J Med 2000; 343:1586-1593).
 Tamaño completo
Tamaño completo Figura 5. Etanercept como monoterapia en AR precoz: Respuesta radiológica.
En el Etanercept/MTX Combination Trial se observó que la asociación aumenta el resultado de etanercept, en cuanto a respuesta ACR 20, 50 y 70 (Weinblatt ME et al. N Engl J Med 1999;340:253-259) y un dato interesante es que, en los enfermos con quienes se empezó con etanercept y después hubo abandono del tratamiento, el problema se resolvió, en 80% de los casos al añadir metotrexato. A los tres años, la respuesta ACR 20, 50 y 70 con Enbrel es de 77%, 59% y 37%, respectivamente, lo que explica el interés por este tipo de medicamento.
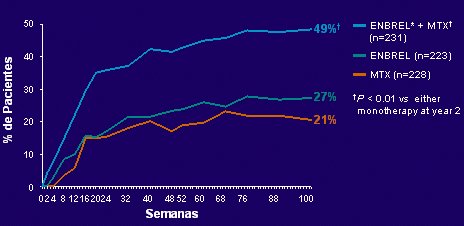
En el estudio TEMPO, estudio doble ciego realizado en 682 pacientes en Europa, Australia e Israel, cuyos resultados fueron publicados en Lancet hace algunos años, se comparó tres tratamientos: Enbrel, metotrexato (MTX) y Enbrel más metotrexato, y se comprobó que con la combinación la tasa de abandono a los dos años fue significativamente menor (MTX 48%; Enbrel 39%; Enbrel + MTX 29% (Klareskog L et al, Lancet 363:675-681, 2004).
La respuesta ACR 70 a los dos años (Figura 6) fue significativamente mayor con la combinación de Enbrel y metotrexato. Por lo tanto, debe utilizarse en pacientes con enfermedad grave. De la misma manera, al año de tratamiento con metotrexato el enfermo mejora, pero la evolución radiográfica, las erosiones y el daño articular continúan, y con Enbrel solo casi no hay evolución. En cambio, si se combinan ambos fármacos se logra una mejoría significativa de las erosiones, las que pueden, incluso, desaparecer.
 Tamaño completo
Tamaño completo Figura 6. Respuesta ACR 70 a los dos años de tratamiento con Enbrel, metotrexato o la combinación (estudio TEMPO).
En niños, el Enbrel tiene resultados muy interesantes. En un estudio abierto, más de 90% de los niños evolucionaron favorablemente; luego se hizo una fase doble ciego y cruzada con Enbrel y placebo, y los resultados fueron extraordinarios. En nuestro departamento tenemos algo de experiencia en niños y es una maravilla, ya que los pacientes tratados con medicamentos de este tipo de drogas vuelven a trabajar, a hacer deportes y a vivir normalmente.
Anticuerpos monoclonales anti TNF alfa
Infliximab (Remicade)
Las indicaciones y características de infliximab son:
- Reducción de los signos y síntomas en pacientes con AR activa, cuando la respuesta a los tratamientos de fondo, incluso a metotrexato, ha sido inadecuada (Estados Unidos agosto 1999, Francia agosto 2000).
- Enfermedad de Crohn grave. El etanercept no tiene utilidad en esta enfermedad.
- Asociado con el metotrexato, eventualmente con Arava o Imurel, pero sin autorización de comercialización.
- La posología es 3 mg/kg, pero en muchos casos hay que subir la dosis hasta 5 mg/kg.
- Se administra en perfusión intravenosa lenta (2 horas), con vigilancia 2 horas después del término.
- Las perfusiones se hacen en las semanas 0, 2 y 6, luego cada dos meses. A veces se debe modificar, porque hay escape y se debe disminuir el tiempo entre dos perfusiones.
En el estudio ATTRACT, realizado en 428 pacientes con AR activa, a pesar del uso de MTX, que fueron tratados durante 24 meses con MTX asociado a placebo o infliximab en distintas dosis, se demostró que la combinación mejoraba significativamente la respuesta ACR a las 30, 54 y 102 semanas (Lipsky PE et al. Arthritis Rheum 2000;43 (suppl):S269).
De la misma manera, en pacientes con enfermedad estable, infliximab detuvo significativamente la progresión radiológica de la enfermedad, en forma similar a lo observado con Enbrel (Lipsky PE et al. N Engl J Med 2000;343:1594). En general, los estudios se hicieron con enfermos con artritis reumatoídea grave y de larga evolución (alrededor de ocho años).
El ASPIRE es un estudio realizado en 1049 pacientes con artritis reumatoídea reciente, de tres meses a tres años, que nunca habían recibido MTX y que fueron asignados al azar a tres grupos de tratamiento, durante 54 semanas: Infliximab 3 mg/kg + MTX ; Infliximab 6 mg/kg + MTX ; o placebo + MTX. La dosis de MTX fue de 7,5 a 20 mg/semana, en 8 semanas. Se evaluó el porcentaje de mejoría ACR-N, HAQ, score de Sharp total modificado y la modificación del score radiológico en función de CRP inicial y área bajo la curva.
Las respuestas ACR 20, 50 y 70 fueron superiores en los grupos infliximab/MTX (40%) que en el grupo placebo/MTX (25%), lo mismo que la mejoría HAQ ; pero lo más interesante fue que la asociación detuvo la evolución radiográfica, lo que es muy importante para bloquear la actividad de la AR. Los pacientes cuyos daños radiológicos eran más marcados al inicio del estudio mostraron mayor progresión radiológica con MTX solo y consiguieron el máximo beneficio con la adición de Infliximab (ACR 2003 - D’après Smolen (LB 4), Saint-Clair (LB 21).
Adalimumab (Humira)
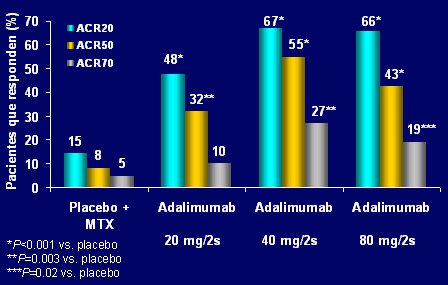
Weinblatt demostró que la actividad del fármaco es de 46% ACR 20, lo que no es tan extraordinario; en cambio, la asociación con MTX obtiene 67% de respuesta (Figura 7) (Weinblatt ME, et al. Arthritis Rheum 2003; 48:35-45). La asociación modificaría el clearance de Adalimumab. El fármaco se utiliza en dosis de 40 mg cada dos semanas, pero se puede subir a una inyección semanal si es necesario y si es posible, ya que el costo subirá al doble.
 Tamaño completo
Tamaño completo Figura 7. Respuestas ACR significativas a las 24 semanas de administración de Adalimumab más MTX.
La evolución radiográfica con Adalimumab es idéntica a la que está descrita con las otras drogas, es decir, se detiene (Keystone et al. ACR 2003. Orlando Presentation Number 741, Poster Board Number 136).

