Cursos
← vista completaPublicado el 1 de abril de 2004 | http://doi.org/10.5867/medwave.2004.03.3286
Tratamiento del sarcoma de partes blandas
Treatment of soft tissue sarcoma
Resumen
Este texto completo es la transcripción editada y revisada de una conferencia dictada en el curso Lesiones Tumorales y Pseudotumorales del Sistema Musculoesquelético, organizado en Santiago por el Departamento de Ortopedia y Traumatología de la Universidad de Chile del 12 al 16 de mayo de 2003.
Director: Dr. Miguel Sepulveda H.
Protocolo I (evaluación 1988-1998)
Este protocolo, que consiste en un tratamiento combinado de quimioterapia, radioterapia y cirugía conservadora, aplicado dentro de un estudio prospectivo y cooperativo con el Instituto Nacional del Cáncer (INC), se aplicó hasta 1998; posteriormente se hizo una revisión de casos.
Está demostrado que el tratamiento de elección, en sarcomas de partes blandas, es radioterapia y cirugía, pero hemos incorporado quimioterapia en algunos casos especiales.
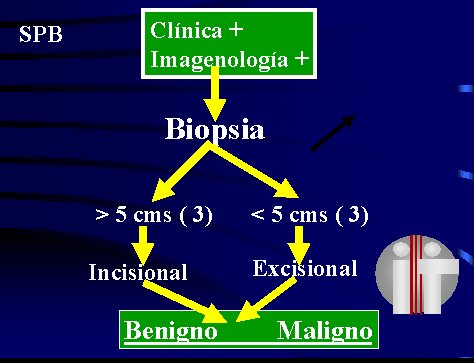
El esquema de manejo se grafica en la figura 1; si un paciente consulta por dolor y aumento de volumen o de consistencia de partes blandas y la imagenología apoya la presencia de un tumor, se efectúa biopsia incisional (si mide más de 5 cm) o excisional (si mide menos), cuyo informe indicará que la lesión es benigna o maligna.
 Tamaño completo
Tamaño completo Figura 1. Esquema de manejo del sarcoma de partes blandas.
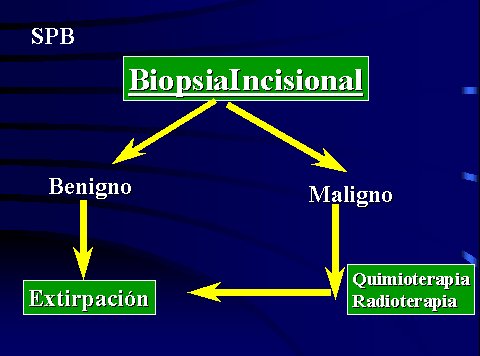
La conducta después de la biopsia se resume en la figura 2. Si la lesión es benigna, se debe extirpar el tumor; si es maligna, pasa al protocolo de quimioterapia y radioterapia preoperatorias, seguidas de cirugía conservadora a las tres semanas. En muy pocos casos, la cirugía puede ser radical.
 Tamaño completo
Tamaño completo Figura 2. Conducta post biopsia.
Estos tumores presentan un falso límite, dado por una pseudocápsula cuya zona externa es la que histológicamente presenta mayor actividad mitótica.
Estudio previo
Los pacientes que participaron en este protocolo pasaron por un estudio completo antes de la biopsia, con anamnesis, examen físico, exámenes de laboratorio, radiografía local y de tórax.
Además se efectúa una TC, en la que se ve con claridad hueso, estructuras musculares y conectivas, y la lesión tumoral de partes blandas. Hoy, la RM es fundamental en las lesiones de partes blandas, con todas las ventajas y limitaciones de este examen.
La biopsia puede ser incisional o excisional, pero siempre se debe hacer en forma longitudinal, con una hemostasia prolija y sin utilizar drenaje en el lecho.
Criterios de inclusión
- Diagnóstico histológico previo.
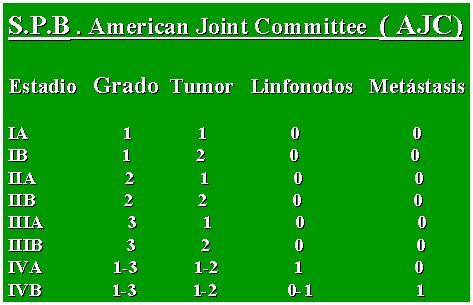
- Etapa IB a IIIB de la clasificación del American Joint Committee (AJC), que se presenta en la tabla I. Esto no significa que los que quedan fuera de estas etapas no se traten, sólo que no se incluyen en el protocolo.
 Tamaño completo
Tamaño completo Tabla I. Clasificación del sarcoma de partes blandas. American Joint Committee (AJC) 1988.
- Si hubo tratamiento previo, se hace biopsia incisional, se revisa la histología y el paciente puede ingresar a protocolo.
- Los pacientes con recurrencia tumoral también entran en el protocolo.
- Edad: mayores de 14 y menores de 70 años.
- Consentimiento informado del paciente, ya que fue un tratamiento experimental.
- Actividad según el Eastern Cooperative Oncology Group (ECOG) 0 - 1 - 2, definida como sigue: 0 = paciente asintomático, capaz de llevar una vida normal; 1 = paciente capaz de vivir en casa, con manifestaciones tolerables del tumor; 2 = pacientes con limitaciones de su vida normal por el tumor, pero menos del 50 %.
Criterios de exclusión
- Etapa IA, que son de bajo grado, menores de 5 cm y sin metástasis. Este grupo queda excluido, porque sólo necesita cirugía.
- Etapa IV, que son de bajo o alto grado, menores o mayores de 5 cm, pero con compromiso de ganglios linfáticos o metástasis pulmonar.
- Pacientes que ya han recibido quimioterapia, radioterapia o cirugía radical.
- Presencia de otra neoplasia.
- Proceso infeccioso importante, cardiopatías graves, con uso de terapia anticoagulante, enfermedad hepática o metástasis a distancia.
Para la quimioterapia se usa epirrubicina, 70 mg/m2 en monodosis por vía endovenosa, en forma ambulatoria.
La radioterapia se efectúa por 2 campos AP, con 3000 rads (30 Gray), en 10 fracciones de 300 rads diarios, de lunes a viernes, por dos semanas.
La cirugía conservadora se realiza tres semanas después de la radioterapia. Consiste en resección en bloque, incluyendo la cicatriz, con margen de tejido sano y biopsia intraoperatoria. La sutura debe ser firme, por lo que además de la sutura convencional se coloca una doble sutura encima para evitar la dehiscencia, complicación que se ve después de la radioterapia.
Resultados
Se evaluó a 65 pacientes. De las biopsias realizadas, 90% fueron incisionales, ya que en su mayoría, los pacientes consultaron con tumores mayores de 5 cm.
La distribución fue similar en todas las edades, con predominio en el sexo masculino. En cuanto a la localización, 73% de los pacientes tenían el tumor en la extremidad inferior y 27%, en la superior. Con respecto al tamaño, 70% de los tumores eran mayores de 5 cm.
Histología
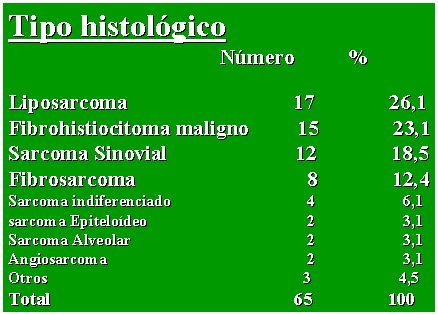
En la tabla II se detallan los tipos histológicos que se encontraron. Los cuatro más frecuentes fueron: el liposarcoma, el fibrohistiocitoma maligno, el sarcoma sinovial y el fibrosarcoma, lo que coincide con lo que se describe en la literatura.
 Tamaño completo
Tamaño completo Tabla II. Sarcoma de partes blandas.Tipos histológicos encontrados.
En cuanto a la etapa clínica, no hay diferencia muy significativa. Lo más importante es que las etapas IIB, IIIA y IIIB agrupan la mayor incidencia, es decir, son lesiones grandes.
Complicaciones
Las complicaciones de la cirugía ocurrieron en 20% de los casos (12 pacientes). La cirugía y radioterapia se complicaron de dehiscencias de sutura e infecciones superficiales, todas manejables.
La radioterapia tuvo 15,4 % de complicaciones y la quimioterapia, 13,8 %. Esta baja incidencia de complicaciones se explica por el uso de monodosis, pero en el protocolo II ellas aumentan.
En 8,1 % de los casos hubo recidiva local, lo que es muy satisfactorio y, en 22,5%, hubo metástasis a distancia. Hubo que amputar a cuatro pacientes después de la cirugía conservadora, debido a recidiva local u otros problemas.
A pesar de que los protocolos han ido mejorando y se han desarrollado técnicas que permiten decir que el problema local está totalmente controlado, no existe actualmente un protocolo que evite el problema a distancia, de modo que finalmente todos los pacientes fallecerán por metástasis.
Sobrevida
- La sobrevida global es de 74%.
- En el grupo IB, es decir, con tumores menores de 5 cm, de bajo grado, la sobrevida es de 100% a los cinco años.
- En el grupo II, de mediano grado, ya sea menor o mayor de 5 cm, la sobrevida es 78%.
- En los tumores de alto grado, es de 47%. Por lo tanto, este protocolo no sirve para tratar a los pacientes con alto grado histológico.
El período más importante, en los protocolos de tumores de partes blandas y óseos, es el de los 24 primeros meses; si un paciente sobrevive al cabo de este lapso y no hace recidiva local, se puede concluir que el tratamiento tuvo éxito, aunque no se sabe por cuánto tiempo más.
En suma, todos los pacientes sufren recidivas, metástasis y muerte dentro de los 24 primeros meses. En la mayoría de los casos, los pacientes cuyo tratamiento fracasa, en los protocolos de osteosarcoma, sarcoma de Ewing o sarcoma de partes blandas, fallecen a los 24 meses; en los pacientes que logran pasar esa barrera, la mortalidad se mantiene casi inalterada en el tiempo.
Ventajas de la radioterapia preoperatoria
- Separa el tumor del tejido indemne.
- Disminuye el tamaño del tumor en alrededor de 50%.
- Como consecuencia de lo anterior, la cirugía es de menor tamaño.
- Disminuye la morbilidad operatoria.
- Disminuye el número de células viables. Por eso, históricamente, a estos pacientes se les trataba sólo con radioterapia.
La quimioterapia en monodosis y radioterapia posterior potencian su efecto; es decir, con dosis bajas de quimioterapia se logra un efecto mayor y esto permite usar dosis bajas de radioterapia, y disminuir así los efectos colaterales, costos y complicaciones.
La cirugía conservadora no empeora el pronóstico en ningún tipo de sarcoma, tampoco aumenta las complicaciones; en cambio, mejora la calidad de la sobrevida, por lo que no se debe realizar cirugía ablativa, salvo contadas indicaciones.
En resumen, este tratamiento es adecuado en las etapas iniciales y hoy se aplica en la mayor parte del país. En las etapas III tiene mal resultado, de modo que da lo mismo tratar o no; el pronóstico se mantiene ominoso, a pesar de los avances logrados en el control local, pues no se ha podido lograr el control a distancia.
Es un mal tratamiento, si el tumor mide más de 5 cm, es profundo y tiene grado histológico alto. El grado histológico marca el pronóstico y permite etapificar, dentro de la clasificación de la AJC, para determinar el tratamiento.
Por esto, se formuló un nuevo protocolo que se aplica en las etapas III y IV, es decir, de alto grado, con metástasis o sin ellas. El protocolo que se acaba de exponer se continúa aplicando en los pacientes en etapa I o II, sin variación; los pacientes que responden mal en la primera etapa y que además tienen metástasis a distancia ingresan al nuevo protocolo.
En la actualidad, toda la patología oncológica maligna, cualquiera sea la localización, se trata con protocolos, los que en Chile son todos prospectivos. Aquí no se puede realizar estudios aleatorios ni doble ciego, porque el número de pacientes por tratar es muy bajo.
Perspectivas
Se ha demostrado que la presencia de marcadores tumorales en las biopsias, o de alteraciones tales como translocaciones o eliminaciones en los estudios citogenéticos, se observan en los pacientes que no responden a quimioterapia, de manera que dicha presencia se podría utilizar para seleccionar a los candidatos para este tratamiento.
En los Estados Unidos hay estudios en curso que evalúan ambos factores en conjunto, para determinar cuándo se debe utilizar un protocolo u otro, y cuándo se debe tratar.
Protocolo II (evaluación 1999-2002)
Este nuevo protocolo para el tratamiento del sarcoma de partes blandas se realizó con base en la experiencia de un equipo multidisciplinario, la que se usó para confeccionar una proyección nacional.
En 1998, con la asesoría del equipo italiano, se hizo una evaluación de los resultados de todo el país y se publicó un metaanálisis de los pacientes tratados con diferentes esquemas de quimioterapia.
Este protocolo se basó en un estudio cooperativo italiano dirigido a administrar poliquimioterapia. En él se mantuvieron los estándares de cirugía y radioterapia, y se plantearon las mismas bases que para el protocolo I, es decir, que el tratamiento de elección, en sarcoma de partes blandas, es radioterapia y cirugía, y que se obtiene un control local satisfactorio, pero no así a distancia.
Esquema de tratamiento
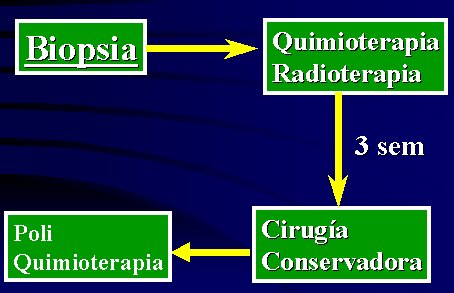
En la fase inicial se utiliza el mismo esquema, que está representado en la figura 3: biopsia, monodosis de quimioterapia, radioterapia preoperatoria y cirugía conservadora a las tres semanas. Además se administra poliquimioterapia postoperatoria durante seis ciclos.
 Tamaño completo
Tamaño completo Figura 3. Esquema de tratamiento.
El estudio previo a la biopsia es idéntico al del protocolo I. La biopsia es incisional, se realiza en el eje longitudinal de la extremidad y en la resección nunca se debe visualizar el tumor. En la poliquimioterapia se administra ifosfamida y doxirrubicina; después del estudio cooperativo, se determinó que eran los fármacos de mejor aceptación.
Los criterios de inclusión son idénticos a los del protocolo I, pero además se agrega a los pacientes mayores de 12 años y las etapas III a IV de la AJC. Los criterios de exclusión también son los mismos.
Resultados
Participaron 16 pacientes, en quienes sigue predominando la biopsia incisional (91% de los casos). No se debe extraer el tumor en la primera etapa.
En los mayores de 50 años, hay predominio en el sexo masculino; la distribución etaria prácticamente no varía. En los pacientes de más edad, predomina el fibrohistiocitoma maligno; en la edad intermedia, el liposarcoma; y en los más jóvenes, es más frecuente el rabdomiosarcoma.
En cuanto a localización, predomina en extremidades inferiores (73, 4% versus 26,6% en las superiores) y la mayoría de los pacientes consulta cuando el tumor es mayor de 5 cm (69%).
Con respecto a la etapa clínica, se incluyeron los tumores grupo III y IV; la mayoría de los pacientes eran grupo III (68,8 % versus 31,2% del grupo IV); es decir, son los pacientes que respondieron mal al protocolo I y los que presentan metástasis a distancia.
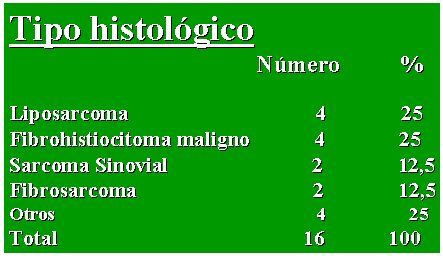
En cuanto al tipo histológico observado, hubo la misma proporción de liposarcoma y fibrohistiocitoma maligno, y los mismos tumores se mantuvieron en los cuatro primeros lugares, que corresponden a más de 80% de los casos (Tabla III).
 Tamaño completo
Tamaño completo Tabla III. Sarcoma de partes blandas, protocolo II. Tipos histológicos encontrados.
Las complicaciones se mantienen básicamente iguales, pero con un gran aumento de las que se asocian con quimioterapia. En la cirugía persisten bajo 20% y con radioterapia hay 15 %; en cambio, las asociadas a la quimioterapia aumentan a 56,2 %, debido a que los fármacos se utilizaron en dosis máximas, lo que produjo una mayor incidencia de dehiscencia de suturas, infecciones, etc.
En cuanto a las complicaciones, hubo recidiva local en 18,8 % de los casos, con un paciente que no consultó, y hubo metástasis en 31,2 %.
Lo más importante es que los pacientes que necesitaron amputación o desarticulación, que fueron 12,5% de los casos, se recuperaron en menos de 24 horas.
Los pacientes que se complican presentan mayor número de metástasis, son pacientes con sarcoma de alto grado, que ya presentan metástasis o que se manifiestan posteriormente.
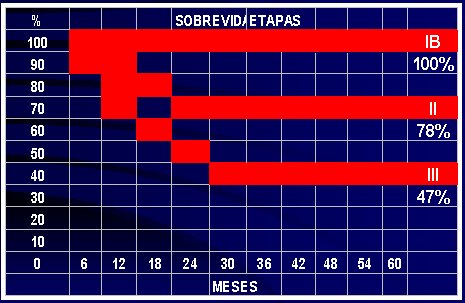
En la actualidad, con alrededor de 100 pacientes en el protocolo, se ha visto que la sobrevida aumenta, de 47%, que se observó en el protocolo I, a 50%, en el protocolo II; que en la etapa III se mantiene igual; que no hay variaciones en la etapa IB; y que en la etapa II mejora de 75% a 78% (Figura 4).
El análisis de X2 (ji cuadrado) indica que la diferencia no es significativa, lo que significa que la quimioterapia no ha demostrado utilidad en el control de la enfermedad a distancia.
 Tamaño completo
Tamaño completo Figura 4. Sobrevida según etapa clínica. (Protocolo II).
Conclusiones
No se observa mejoría del pronóstico con el protocolo II, lo que coincide con lo que se describe en la literatura; además, aumentan las complicaciones debidas a la quimioterapia, de modo que el futuro es incierto.
Lo concreto es que los protocolos I y II son satisfactorios en cuanto al control local, con resultados comparables a lo que describen otros grupos de trabajo a nivel mundial, y con iguales resultados en el tipo III. La única diferencia es que en los Estados Unidos el número de amputaciones se eleva al doble, debido al elevado riesgo de demandas médicas.

