Publicado el 1 de enero de 2004 | http://doi.org/10.5867/medwave.2005.01.2472
Manejo anestésico del bloqueo AV
Anesthetic management of AV block
Resumen
La publicación de las Actas de las Reuniones Científicas de la Sociedad de Anestesiología de Chile ha sido posible gracias a una colaboración editorial entre Medwave y la Sociedad.
El anestesista debe diferenciar si el bloqueo AV completo es conocido o desconocido, y en ambos casos, si tiene o no compromiso hemodinámico.
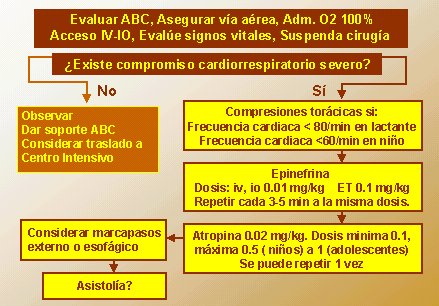
En caso de bloqueo AV desconocido, como el caso que se ha presentado, la American Cardiology Association diseñó un algoritmo de la bradicardia, según el cual lo primero es asegurar la vía aérea, buscar una vía venosa y ver si el paciente tiene un compromiso cardiorrespiratorio grave; si no lo tiene se debe dar soporte de la vía aérea, oxígeno y trasladarlo a un centro intensivo para continuar su estudio.
Si la frecuencia cardíaca es menor de 80 por minuto en el lactante o 60 por minuto en el niño mayor, debiera ser sometido a compresiones torácicas mientras se prepara la epinefrina, administrando cada tres a cinco minutos. El orden es epinefrina y después atropina. Si no responde a estos fármacos, y existe la disponibilidad, debe considerarse un marcapaso externo o esofágico. Si el paciente cae en asistolía, debe utilizarse el algoritmo indicado para esos casos. Esto está resumido en la figura 1.
 Tamaño completo
Tamaño completo Figura 1. Algoritmo de bradicardia (PALS).
En caso de bloqueo AV conocido, es decir, que el paciente se presenta a la anestesia ya diagnosticado, debe revisarse su historia, los antecedentes obstétricos y preguntar si ha presentado una insuficiencia cardíaca intra utero, caso en el cual hay hidrops fetal. En un paciente mayor, se debe preguntar si ha tenido síncopes, hipotensión, arritmias o paro cardiorrespiratorio previo, antecedentes útiles para anticipar problemas. En el examen físico se deben buscar signos de insuficiencia cardíaca congestiva.
En el electrocardiograma es importante buscar actividad ectópica, que puede estar avisando que podrían existir problemas de arritmias ventriculares durante el procedimiento anestésico. La radiografía de tórax permite descartar alteraciones de la silueta cardíaca, derrames pleurales, etc. El ecocardiograma es importante, porque permite detectar si el paciente tiene una cardiopatía congénita. Algunos especialistas proponen realizar test de tolerancia al ejercicio o con atropina para evaluar cómo responde el sistema excitoconductor a estos estímulos.
Durante la inducción anestésica, dos o tres estudios sugieren que el sevofluorano es una buena alternativa, porque produce una profundidad anestésica adecuada, con bajo riesgo de apnea postoperatoria. Es importante recordar que en muchas ocasiones es necesario resolver en el postparto inmediato los problemas de los neonatos, que tienen el sistema respiratorio inmaduro. El sevofluorano puede producir incluso, a través de un estímulo simpático, un aumento de la frecuencia cardíaca, lo que protegería en parte de la bradicardia. Además existe una recuperación rápida, con buena estabilidad hemodinámica.
Otra alternativa mencionada es la ketamina, que podría permitir, mediante la disminución de la inhibición de la recaptación de catecolaminas, una frecuencia cardíaca basal un poco más rápida. También aumenta la resistencia vascular sistémica y pulmonar, por el mismo mecanismo, lo que disminuye el riesgo de hipotensión secundaria a los halogenados utilizados para la mantención anestésica. Evitaría la necesidad de administrar dosis altas de opiáceos, porque tiene una acción antagonista anti NMDA, que produce analgesia en el niño.
En cuanto a la mantención anestésica, el sevofluorano y el isofluorano son agentes que producen menos depresión de los barorreceptores que otros agentes halogenados, además de una menor depresión de la contractilidad, pero producen una disminución importante de la resistencia vascular, y si el niño tiene un compromiso hemodinámico, puede hipotensarse aún más.
Con respecto al isoprotenerol, que se utilizó durante el tercer procedimiento anestésico, es un agonista potente de los receptores beta 1 y 2, sin mucho efecto alfa, por lo tanto es un buen agente cronotrópico e inotrópico, pero se debe tener cuidado con las taquicardias y arritmias ventriculares que pueden producirse; de hecho, la American Heart Association no lo incluye dentro del algoritmo de la bradicardia. Se administra en infusión de 0,05 a 10 microgramos/min en adultos; no encontré la dosis en niños. Se considera categoría IIb (posiblemente útil).
En cuanto al uso de relajantes musculares, se debe ser cuidadoso, sobre todo los de larga duración, porque en esos casos es necesario antagonizar su efecto con neostigmina, la que disminuye la frecuencia cardíaca. No es recomendable utilizar succinilcolina, por lo mismo, ya que es un agente anticolinérgico. Los opiáceos también producen bradicardia. El halotano no sería recomendable, de hecho existe un case report sobre un paciente que casi hizo un paro cardíaco secundario a la administración de este agente. En general, se debe tener precaución con el uso de los agentes crono e inótropos negativos.
El uso de marcapasos profiláctico es muy controvertido, ya que se debería evaluar si la anestesia requiere la implantación de un marcapasos definitivo u otro tipo de cirugía. En la mayoría de los casos no sería necesario implantar un marcapasos profiláctico transvenoso; no se dudaría en realizarlo si el paciente ha tenido un síncope previo, tiene un QRS ancho o signos de insuficiencia cardíaca congestiva, pero no en otros casos.
Existe un autor que opina que el riesgo del marcapasos transvenoso sería menor que el de una cirugía sin él, pero aún no está resuelta esta disyuntiva (Anesth Analg 1980; 59-81).

