Publicado el 1 de junio de 2002 | http://doi.org/10.5867/medwave.2002.05.2323
Manejo anestésico del paciente con traumatismo encéfalo craneano
The anesthetic management of patients with traumatic brain injury
Siglas y abreviaturas:
TRM: Trauma Raquimedular
SDRA: Síndrome de estrés respiratorio del adulto
PIC: presión intracraneana
SIADH: síndrome de secreción inapropiada de ADH
TEP: Tromboembolismo pulmonar
PAM: Presión arterial media
Introducción
Definición de traumatismo encéfalo craneano (TEC)
Lesión física o deterioro funcional del contenido craneal debido a un intercambio brusco de energía mecánica (1).
El TEC es el principal problema de salud pública en los Estados Unidos, dando cuenta del 44% de todas las muertes por trauma.
Sólo un pequeño porcentaje de los pacientes con TEC tienen lesiones intracraneanas tratables quirúrgicamente, y por lo tanto la gran mayoría tiene tratamiento médico, frecuentemente en una UTI.
El objetivo del tratamiento es mantener al paciente de modo tal de permitir la máxima recuperación de la Lesión Primaria y revertir o prevenir la lesión secundaria.
Producida la lesión primaria comienza el periodo de la lesión secundaria que puede presentarse minutos, horas, e incluso, en los días posteriores al traumatismo consistiendo en una serie de agresiones sistémicas o intracraneanas, las cuales magnifican y/o producen nuevas lesiones cerebrales.
Por lo tanto el perioperatorio se caracteriza por ser un periodo de reanimación y vigilancia proactiva y orientada, al lado del paciente tanto como así lo requiera, tratando de ir un paso adelante de las complicaciones potenciales más frecuentes de acuerdo a cada patología neuroquirúrgica.
Clasificación de la OMS de la gravedad del TEC. (2)
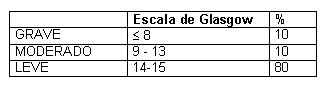 Tamaño completo
Tamaño completo Clasificación de masters de riesgo de los pacientes con TEC.
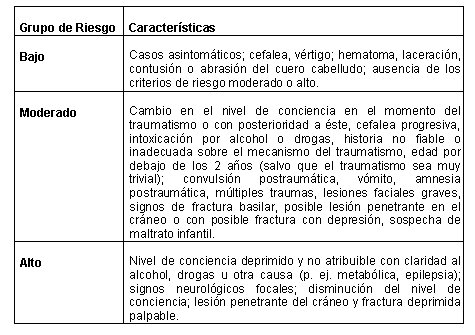 Tamaño completo
Tamaño completo Efectos sistémicos del trauma del sistema nervioso central (SNC).
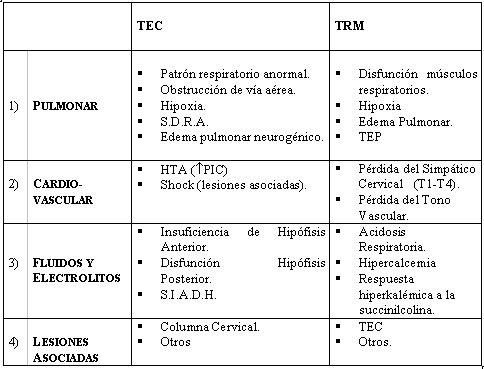 Tamaño completo
Tamaño completo TRM: Trauma Raquimedular; SDRA: Síndrome de estrés respiratorio del adulto; PIC: presión intracraneana; SIADH: síndrome de secreción inapropiada de ADH; TEP: tromboembolismo pulmonar; PAM (presión arterial media).
Flujograma en el manejo del TEC
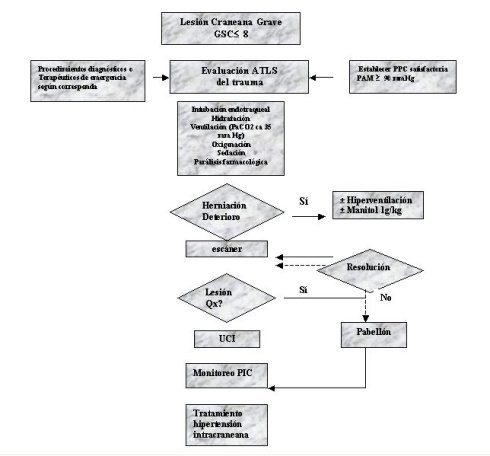 Tamaño completo
Tamaño completo Se debe contar además, al igual que el flujograma anterior, con normas o un protocolo de transporte del paciente dentro del hospital o instituto para garantizar que en estos periodos no se disminuya la vigilancia y menos un tratamiento determinado. Durante estos momentos se pueden producir eventos o situaciones que pudieran determinar el futuro de la evolución del paciente. A continuación un ejemplo de transporte a la sala de tomografía axial computada.
Protocolo para un transporte seguro y eficiente del paciente con TEC para la realización de exámenes neuroradiológicos:
- Asegurar que al paciente se le realizará inmediatamente la Tomografía Axial Computada (TAC) al llegar a radiología. El paciente nunca debe esperar en el servicio de radiología para la realización de un examen.
- Disponer del equipamiento de manejo respiratorio necesario para el transporte. Idealmente utilizar un ventilador de transporte.
- Revisar el equipo de transporte que debe contar con los medicamentos y accesorios necesarios.
- Preparar el equipo de monitoreo para el transporte. Punto cero, calibración y programar las alarmas. El monitoreo mínimo de transporte incluye ECG, presión arterial y saturación periférica de O2.
- Si está indicado, administrar el tratamiento para la hipertensión intracraneana.
- Conectar al paciente al ventilador de transporte. Si tal ventilador no está disponible, ventilar manualmente con ambú y O2 al 100%.
- Transportar al paciente al servicio de radiología y luego directamente a la camilla del tomógrafo.
- Disponer del equipo de monitoreo de modo que pueda ser visualizado desde la sala de control del tomógrafo. Revisar la condición de las alarmas.
- Realizar una rápida evaluación neurológica. Indicar tratamiento médico al paciente según lo requiera.
- Iniciar el examen.
- Continuar la observación del paciente y los parámetros de los monitores durante el examen. En presencia de un hallazgo adverso, detener inmediatamente el examen y corregir la situación.
- Disponer de un informe preliminar de la tomografía por el personal responsable previo a la conclusión del mismo. Antes del término de la tomografía el equipo a cargo debe determinar el lugar adecuado a donde deberá ser trasladado a continuación.
Indicaciones neuroquirúrgicas de urgencia:
- Hematoma intracraneano accesible y responsable de deterioro neurológico y/o de un efecto de masa con una desviación de línea media mayor o igual a 3mm.
- Hidrocefalia aguda.
- Lesión craneo cerebral.
- Hundimiento muy desplazado, nocivo para el parénquima subyacente.
Clasificación de las lesiones traumáticas:
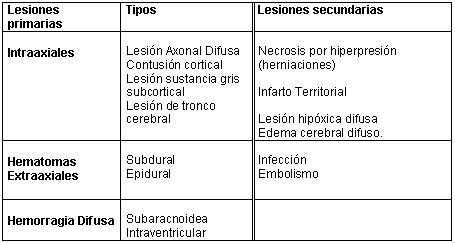 Tamaño completo
Tamaño completo El resultado clínico en bueno o moderado, grave-vegetativo o muerto, dependerá también de la presencia o no al momento del ingreso de agresiones secundarias tales como la hipoxia (11,2%) y/o hipotensión (16,2%) que cuando se presentan ambas (7,4%) da como resultado hasta un 75% de mortalidad según los datos del Traumatic Coma Data Bank (4). Por lo tanto el perioperatorio se caracteriza por ser un periodo de reanimación y de vigilancia proactiva y orientada, al lado del paciente tanto como así lo requiera, tratando de ir un paso adelante de las potenciales complicaciones más frecuentes de acuerdo a cada patología neuroquirúrgica.
La autorregulación cerebral se encuentra abolida o alterada en un 57% de los pacientes con TEC y lesiones difusas (5).
La hipotensión arterial moderada posthemorragia en animales con TEC, reduce el flujo sanguíneo cerebral (FSC), el transporte cerebral de oxígeno y la actividad electroencefalográfica en niveles notablemente mayores que cuando estos animales sufren aisladamente un TEC o hipotensión arterial, confirmando, de este modo, la susceptibilidad del cerebro traumatizado a la hipotensión arterial por disminución de la reserva vasodilatadora (6).
Una PPC menor o igual 60 mmHg se asocia a una mortalidad de aproximadamente 95%.
Mecanismos de lesión secundaria en el TEC
Sistémicos
- Hipotensión arterial
- Hipoxemia
- Hipercapnia/Hipocapnia
- Anemia
- Hipertermia
- Hiponatremia
- Hiper e Hipoglicemia
- Acidosis
- Síndrome de respuesta inflamatoria sistémica
Intracraneales
- Hipertensión intracraneana
- Vasoespasmo
- Convulsiones
- Edema cerebral
- Hiperemia
- Hidrocefalia
- Trastornos metabólicos y fisiológicos a nivel celular y subcelular
- Hematoma cerebral tardío
- Infecciones
- Disección carotidea
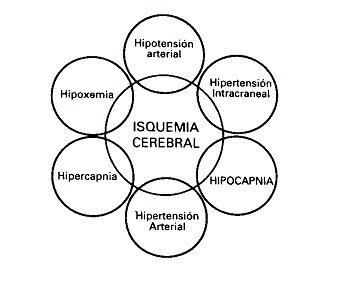 Tamaño completo
Tamaño completo Figura 1: Mecanismos fisiopatológicos capaces de provocar isquemia cerebral secundaria.
Mecanismos involucrados en la lesión postraumática.
- Lesión de las células endoteliales y la disrupción de la barrera hematoencefálica con la consiguiente formación de edema vasogénico.
- Disfunción de la maquinaria proteica celular que da lugar a cambios estructurales en neuronas y glia.
- Degeneración mielínica y falla de la conducción axónica; aunque este mecanismo de lesión secundaria en el TEC ha sido recientemente probado, son numerosas las evidencias que demuestran en experimentación animal que la interrupción farmacológica de este proceso revierte la hipoperfusión postraumática y algunas de las alteraciones de la microcirculación cerebral.
Monitorización neurológica clínica
El examen de pacientes con alteración de conciencia es una destreza eminentemente clínica. Brevemente se debe determinar el nivel de conciencia y establecer la integridad de los pares craneanos y de la función sensitivo motora. Las alteraciones sutiles pueden pasar desapercibidas, especialmente si el paciente está intubado o afásico.
Evaluación neurológica por lo menos horaria, pesquisando deterioro neurológico, en base a:
- las características de las pupilas (tamaño y reflejos)
- Evolución de la escala de Glasgow
- Movilidad de las extremidades
- PAM
- PIC
PAM (presión arterial media)
PIC (presión intracraneana)
La hipertensión arterial sistémica postoperatoria (dolor, hipertensión intracraneana) puede precipitar una hemorragia, especialmente después de la evacuación de un hematoma intraparenquimatoso o de la extirpación de una malformación arteriovenosa (MAV).
La disminución en 2 o más puntos del Glasgow y la aparición de un nuevo déficit se considera significativo y se debe realizar rápidamente una determinación de las posibles causas de tal deterioro tales como:
- hipoxia
- hipotensión
- alteraciones hidrosalinas
- Síndrome de hipertensión endocraneana (hematoma, edema, etc.).
Se debe minimizar la sedación:
 Tamaño completo
Tamaño completo En el caso del paciente con TEC grave (Glasgow menor o igual a 8), agitado e intubado en quién se trata de controlar la ventilación y está con monitoreo de la PIC se utiliza relajantes musculares de corta acción en infusión continua (por ej.: vecuronio, tracrium, etc.).
Nivel de conciencia
- Lúcido: la persona es capaz de reconocerse, conectarse y responder adecuadamente al medio externo. Está orientado en tiempo y espacio
- Obnubilado: la persona tiene un grado de rebajamiento de conciencia, en el cual está disminuida la capacidad del sujeto de reconocerse y relacionarse con el medio externo. No tiene claridad en el razonamiento, está bradipsíquico, confuso y desorientado en tiempo y espacio (total o parcialmente).
- Somnolencia: el sujeto para responder adecuadamente necesita ser despertado mediante estímulos auditivos o táctiles. Luego de responder se volverá a dormir.
- Sopor: el sujeto necesita de estímulos enérgicos para responder, tiene pérdida de las funciones vitales (pérdida de control de esfínteres) pero aún es capaz de responder frente a estímulos con estructuración o no (apertura de ojos, movilidad momentánea). Al cesar los estímulos el sujeto entra nuevamente en inconsciencia.
- Coma: el sujeto ha perdido la capacidad de respuesta correcta, mantiene los ojos cerrados, con músculos flácidos y se acompaña de función vegetativa (sudación y movilidad alterada).
Monitorización y manejo de la presión intracraneana (PIC).
Edema cerebral post TEC.
1. Focal
- Asociado a contusiones o laceraciones cerebrales.
- Asociado a "estallido" de lóbulo.
- Infartos cerebrales.
2. Difuso
- Hemisférico Unilateral
i) Aislado
ii) Asociado a hematomas extra-axiales
iii) Post-evacuación de hematomas
- Hemisférico Bilateral
I.- Monitorización
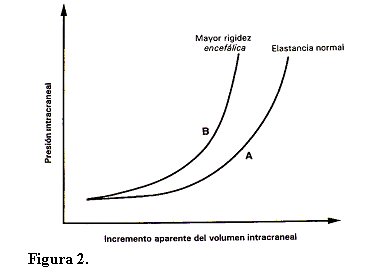 Tamaño completo
Tamaño completo Ventajas de la monitorización continua
- Identificación de la hipertensión intracraneana.
- Alarma precoz de la aparición de complicaciones (especialmente en pacientes comatosos o con parálisis muscular farmacológica).Entre los pacientes con daño grave, con puntaje de Glasgow inicial de 3-5, la tasa de mortalidad podría disminuir significativamente según evidencian algunos trabajos publicados cuando se utiliza monitorización de PIC.
- También tiene valor pronóstico en la recuperación después del TEC. Los pacientes con elevación intratable de PIC mueren o tienen un muy mal ronóstico.
Técnicas de monitorización:
- Catéteres intraventriculares
- Fibra Óptica (Camino): que es de fácil y rápida instalación (espacio subaracnoideo, parénquima cerebral o ventrículo).
- Microchip de Codman. Tiene todas las ventajas del monitor de fibra óptica pero sin los riesgos de fractura ni dificultades de instalación ni mantención.
- Catéteres Subdurales (monitorización postoperatoria).
La monitorización se mantiene por lo menos hasta 24 horas después de normalizada la PIC y ya no sean necesarias las medidas tales como la hiperventilación y la administración de manitol.
Mientras se mantenga la monitorización invasiva intracraneana es aconsejable la profilaxis antibiótica con cobertura antiestafilocócica.
II- Manejo de la hipertensión intracraneana
Realizada la reanimación básica, se debe considerar los siguientes aspectos:
- Hiperventilación controlada.
- Manitol (0,25 – 1,0 g/k en bolos IV).
- Furosemida.
- Elevación de la presión de perfusión cerebral.
- Elevación de la cabecera 10º - 20º - 30º.
- Analgesia y sedación para el reposo.
- Parálisis en la agitación grave.
- Uso de barbitúricos.
La autorregulación cerebral se encuentra abolida o alterada en un 57% de los pacientes con TEC y lesiones difusas (5).
Hiperventilación
La PaCO2 se mantiene entre 30-35 mmHg (en casos excepcionales y en que idealmente se cuente con monitoreo metabólico o exista riesgo vital, se lleva a rangos entre 20-30 mmHg) para producir vasoconstricción cerebral, pero al grado que no reduzca el flujo sanguíneo cerebral bajo los niveles necesarios para la mantención de un metabolismo normal (evidenciado parcialmente por la diferencia arteriovenosa (AVDO2).
Se evita utilizar una hiperventilación más allá de la señalada, ya que no se traduciría en una vasoconstricción mayor y además para evitar causar complicaciones metabólicas derivadas de la alcalosis grave. Sin embargo en niños existe evidencia de que sí produciría mayor disminución de la PIC (con PaCO2 de 10-15 mmHg). Evitando la complicación isquémica mediante la monitorización de la Saturación Yugular de O2 (SJO2) y calculando la AVDO2.
Un aumento de la AVDO2 sugiere un aumento de la extracción de O2 y la aparición potencial de isquemia cerebral.
Causas de disminución de la SJO2:
- Hipertensión intracraneana.
- Hipocapnia grave.
- Hipoxemia.
- Hipotensión arterial.
Por lo tanto la monitorización continua de estos parámetros SJO2 y AVDO2, pueden ser de mucho valor clínico en el paciente con TEC.
La hiperventilación puede ser ineficaz después de 20-24 horas de iniciada en producir vasoconstricción. Por lo tanto sólo se intenta usar inicialmente hasta tener una monitorización de la PIC y luego se usa en forma intermitente de acuerdo a los requerimientos.
La hiperventilación NO debe utilizarse en:
- prevención del aumento de la PIC,
- en forma aislada para el manejo de la PIC.
Una excepción a estas recomendaciones puede ser el caso de los niños pequeños, quienes después de un TEC grave pueden presentar una hiperemia difusa y un aumento del flujo y volumen sanguíneo cerebral.
Terapia hiperosmolar
Junto a la hiperventilación se utiliza manitol y simultáneamente otros diuréticos para disminuir el volumen extracelular en el cerebro.
Manteniendo un paciente normovolémico con aumento de:
- Natremia (145-155 mEq/l),
- Osmolalidad (300-330 mOsm/l),
- Tonicidad.
Para lograr estos objetivos es necesario:
- monitorizar la PVC,
- administrar soluciones cristaloides isotónicas o coloides para mantener una PVC de 2-5 mmHg,
- si se usa Swan-Ganz se recomienda mantener una presión de enclavamiento > 5mmHg.
Dosis Mannitol: 0,25-0,5 gr/k, hasta cada 4 horas.
Efectos de la administración de manitol en bolo:
- Inmediato aumento del volumen circulante (que puede producir un aumento significativo de la PIC).
- Aumento de la presión arterial
- Disminución de la viscosidad sanguínea.
- Aumento de la deformabilidad del glóbulo rojo.
Complicaciones del uso de manitol:
- Hiperosmolalidad,
- Deshidratación,
- Aumento del edema cerebral (dosis repetidas).
Por lo tanto su uso se debe limitar al mínimo necesario para controlar la PIC y la PPC y no debe darse junto con la furosemida a menos que el control de la PIC sea pobre.
Furosemida
Mecanismo de acción de la furosemida
Aumenta la natremia, aumentando la presión oncótica intravascular extrayendo agua libre del cerebro. Además disminuye la producción de LCR. Su administración junto con el manitol potencian sus efectos (primero el manitol seguido en quince minutos después de furosemida).
- Disminuye el agua libre cerebral,
- Disminuye el edema cerebral.

