Publicado el 1 de mayo de 2003 | http://doi.org/10.5867/medwave.2003.04.2364
Defectos de cierre del tubo neural
Neural tube closure defects
Introducción
Los Defectos de Cierre de Tubo Neural (DTN) corresponden a defectos estructurales del sistema nervioso, de origen multifactorial, lo que implica la acción de numerosos genes y la influencia de factores ambientales. La incidencia es variable, según zona geográfica, así en el Reino Unido, particularmente en Irlanda se dan cifras de hasta 8 por 1000 nacidos vivos (NV). Las cifras de ECLAM ( Estudio Colaborativo LAtinoamericano de Malformaciones congénitas), en que se incluyen cifras de hospitales chilenos, bordea 0,8 por 1000 NV.
Estos trastornos involucran un alto costo social y psicológico para el sujeto afectado, la familia y la sociedad, ya que se asocian a muerte inevitable, a una discapacidad grave y permanente y en algunos casos a retraso mental.
El tubo neural deriva del ectodermo primitivo y se desarrolla hasta formar el encéfalo y la médula espinal. Normalmente, al final de la 3° semana de desarrollo embrionario, se encuentra completamente cerrado. Algunas mujeres en esta etapa, que sería aproximadamente 28 días, aún no han percibido su embarazo y han estado expuestas a diferentes teratógenos ambientales como tabaco y alcohol.
El cierre defectuoso va a causar distintas manifestaciones de acuerdo al sitio de cierre afectado; así un defecto de cierre superior causa anencefalia incompatible con la vida; y un cierre defectuoso en el extremo inferior del tubo neural ocasiona mielomeningocele lumbosacro, generalmente asociado a parálisis parcial o completa de extremidades inferiores.
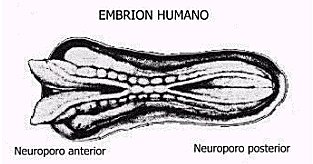
Con respecto a los puntos de cierre, en forma tradicional se considera que el cierre del tubo neural es un proceso continuo que se inicia en la region cervical del embrión y continúa en forma bidireccional hacia la parte rostral y caudal; sin embargo, actualmente se plantea que el cierre del tubo neural sigue un modelo intermitente. En 1993, Van Allen y cols, sugieren que en el hombre se produce un patrón intermitente, similar al observado en animales de experimentación. Los puntos de cierre serían 5 :
Punto 1: ocurre en región cervical del embrión y progresa bidireccional hacia cefálico y caudal.
Punto 2: se inicia en la cabeza, en la unión del prosencéfalo y mesencéfalo, progresa bidireccional formando dos neuroporos, en la dirección cefálica progresa sobre prosencéfalo hasta encontrarse con punto de cierre 3, en la dirección caudal progresa sobre mesencéfalo para terminar en la parte superior del romboencéfalo.
Punto 3: se inicia en el ectodermo, es unidireccional progresando sobre el mesencéfalo hasta encontrarse con el punto de cierre 2 en su porción descendente.
Punto 4: se inicia en la parte caudal del romboencéfalo, es unidireccional hacia la parte cefálica, progresa hasta encontrar la parte caudal del punto de cierre 2.
Punto 5: es unidireccional, se inicia en la parte más caudal del tubo neural, progresando hacia la parte cefálica hasta encontrarse con la parte caudal del punto de cierre 1.
 Tamaño completo
Tamaño completo Figura 1. Puntos de cierre del tubo neural.
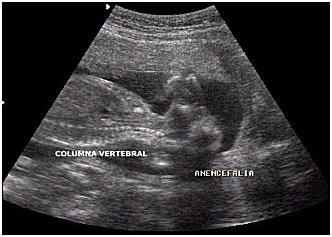
Anencefalia es una condición en que hay ausencia total o parcial de bóveda craneana con escaso remanente de tejido cerebral (Figura 2). Falta por completo cuero cabelludo, huesos craneales y encéfalo, tanto la corteza como sustancia blanca, solo se observa tallo cerebral, cerebelo y medula espinal pero con frecuencia también están malformados. Es más frecuente en las mujeres, es una condición letal, se presentan como mortinatos o mortineonatos, el 65% muere intrauterino o hacia el término del embarazo; en caso de sobrevida no sobrepasa la primera semana.
 Tamaño completo
Tamaño completo Figura 2. Anencefalia
Encefalocele existe protrusión del cerebro o de las membranas que lo recubren a través de la calota, el más frecuente es el occipital.
Los encefaloceles frontales pueden deformar la frente o mantenerse ocultos, plantean riesgo de meningitis. Los encefaloceles nasales pequeños pueden no dar signologia neurológica, pero si son resecados puede existir peligro de fístulas de líquido cefalorraquídeo (LCR). Los occipitales son los más frecuentes y de mayor tamaño se acompañan de ceguera, ataxia y retraso mental.
Mielomeningocele o Espina Bífida defecto de cierre de los arcos neurales, se exponen la medula espinal y los nervios, se puede presentar como espina bífida oculta, meningocele o mielomeningocele propiamente.
Espina bífida oculta, la médula se conserva dentro del conducto y no hay saco externo, aunque el sitio de la lesión puede estar marcado por un lipoma subcutáneo o un mechón de pelo en la piel suprayacente.
Meningocele: hay protrusión de la duramadre y la aracnoides a través del defecto en las láminas vertebrales, que forma una tumefacción quística por lo general a nivel lumbosacro. La médula, sin embargo, se conserva dentro del conducto.
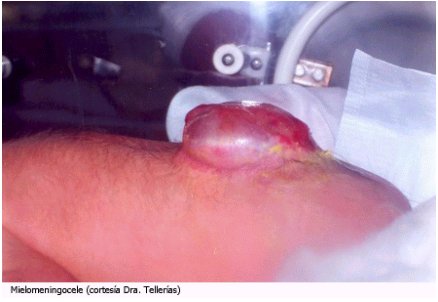
Meningomielocele o mielomeningocele es 10 veces más frecuente que el anterior, hay protrusión de la médula en conjunto con las meninges (Figura 3).
Complicaciones en esta condición son la meningitis y la hidrocefalia progresiva. La anencefalia y la espina bífida son más frecuentes que el encefalocele.
 Tamaño completo
Tamaño completo Figura 3. Mielomeningocele.
Etiología
En el 95% de los casos no hay antecedentes previos familiares de este defecto estructural, se asocian factores genéticos y ambientales, la mayoría multifactorial. Los factores ambientales que se asocian en la etiología de DTN incluyen nivel socioeconómico bajo, multiparidad y embriopatías por teratógenos especialmente ácido valproico. No está demostrado el efecto directo de los plaguicidas en la presentación de esta patología, sin embargo debe considerarse como teratógeno. Otros factores de riesgo a considerar incluyen la etnia ( más frecuente en irlandeses), edad materna y antecedentes hijo previo con DTN.
No se ha identificado ningún gen responsable de producir DTN, aunque existen evidencias que cerca del 10% de los casos pueden atribuirse a mutaciones en el gen que codifica la enzima metilentetrahidrofolato reductasa ( MTHFR).
La disminución de actividad de la MTHFR implica disminución de niveles de folato en el plasma, lo que se asocia directamente con DTN. Los folatos son cofactores de enzimas que sintetizan DNA Y RNA que se requiere para la conversión de homocisteína a metionina; al existir disminución de folatos los ácidos nucleicos son inhibidos y las células no tienen suficiente DNA para realizar la mitosis.
Riesgo de recurrencia
Luego del nacimiento de un niño con esta malformación, el riesgo de recurrencia en el siguiente embarazo es de aproximadamente 5 %; se ha observado que el riesgo depende en alguna medida de la incidencia de DTN en la población circundante, cuanto más elevada la incidencia en la población más alto es el riesgo en el embarazo siguiente. Lo que está ampliamente demostrado en diversos estudios es el efecto de la intervención con uso de ácido fólico preconcepcional en la disminución de la incidencia de los DTN, tanto en la ocurrencia como en recurrencia.
Prevención
Existen firmes evidencias que aportes vitamínicos suplementarios con ácido fólico reduce en un 70 % la presentación de estos defectos. La suplementación con folatos debe iniciarse al menos un mes preconcepción, idealmente 3 meses antes y mantenerse hasta las 12 semanas de gestación.
La recomendación general para mujeres en edad fértil es la ingesta de folatos de 0,4 mg al día, para evitar ocurrencia.
En el caso de que exista historia previa familiar (mujer, pareja o alguna concepción con DTN) se recomienda dosis mayores de 4 mg/día de ácido fólico.
Diferencias entre ácido fólico y folatos
El ácido fólico es una vitamina del complejo B que no se almacena, se requiere su ingesta diaria, cuando se agrega artificialmente se llama ácido fólico.
Si la vitamina B es producto o componente natural de las comidas se llama folato. Es importante señalar que dosis excesivas de ácido fólico pueden encubrir una deficiencia de vitamina B12.
La prevención de ocurrencia de DTN, de origen multifactorial, actualmente se está manejando con el programa de fortificación de las harinas de panificación con ácido fólico, esto sin embargo es insuficiente en el caso de recurrencia, en estas pacientes se aconseja aumentar a dosis de 4 mg al día por al menos 2 meses preconcepcional; de modo que es fundamental el seguimiento de las parejas que han tenido hijos con esta malformación.
Consulta preconcepcional
Consideramos que debe implementarse como un programa, dentro del Programa de la Mujer, no sólo considerando esta patología, en la que se ha demostrado resultados absolutos en prevención.
Diagnóstico prenatal
- La elevación de alfafetoproteínas, tanto séricas como en LCR, es un indicador precoz.
- Ecografía, permite planificar conducta y ofrecer la mejor opción en resguardo de la vida del binomio madre – hijo; en aquellos pacientes que presenten mielomeningocele no sindromático, se contacta con los neurocirujanos previo a interrupción del embarazo que en este caso se planificará por vía alta.
- Estudio citogenético, en algunos pacientes el DTN corresponde a manifestaciones de alteraciones cromosómicas, como trisomía 18, que deben ser evidenciadas en el período prenatal y evitar acciones innecesarias al momento del nacimiento; es fundamental además para las parejas estar informados del pronóstico real.

