Publicado el 1 de junio de 2002 | http://doi.org/10.5867/medwave.2002.05.2550
Embolía de cristales de colesterol (ateroembolía)
Cholesterol crystal emboli (atheroembolism)
Resumen
La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
Introducción
Es un caso muy interesante, porque hemos estado viendo pacientes de estas mismas características desde hace bastantes años e inicialmente pensábamos que eran pacientes con daño crónico, que recibían medios de contraste, y parte de la nefrotoxicidad “irreversible” era mediada por el medio de contraste yodado.
Como fue discutido previamente, en pacientes de alto riesgo para toxicidad para medio de contraste (diabéticos con insuficiencia renal severa), ocasionalmente se produce nefrotoxicidad irreversible por medios de contraste. Sin embargo, esto es poco frecuente, y en la actualidad sabemos que gran parte de estos pacientes presentaron embolía por cristales de colesterol.
Quisiera hacer una revisión de este cuadro clínico, conocido también como ateroembolía o ateroembolismo.
El paciente descrito en el caso clínico cumple varios criterios de ateroembolía, pero sin confirmación de la biopsia. Veremos posteriormente que se puede plantear el diagnóstico en los casos típicos sin necesidad de confirmación biópsica.
La embolía por cristales de colesterol fue descrita por Panum en 1868, quien hizo la primera descripción patológica y se consideró un fenómeno absolutamente raro. Flory, en 1945, en estudios de autopsias, correlacionó la ateroembolía con ateromatosis aórtica grave y se dio cuenta de que, a medida que aumentaba el grado de ateromatosis de la aorta, se encontraban émbolos de cristales de colesterol localizados en el riñón, en los músculos y en otros órganos, y por primera vez logró comprobar que esto no era algo extremadamente raro, y que se relacionaba con el grado de ateromatosis aórtica. Además, construyó un modelo experimental: inyectó placas de ateroma en los conejos por vía i.v. y logró ver cambios histopatológicos a nivel pulmonar; encontró que muchos de estos cambios eran parecidos a los de las enfermedades humanas. De todas maneras, esto quedó como una curiosidad, pero en los veinte últimos años ha evolucionado de una curiosidad patológica a una entidad clínica bien definida.
Patogenia
Los cristales de colesterol se liberan de las placas ateromatosas. En general, se originan de la aorta y ocasionalmente de otros arterias como las carótidas, las arterias renales, las arterias ilíacas, las mesentéricas, etc. Se presentan, la mayoría de las veces, en pacientes que tienen factores de cardiovasculares de riesgo, que son los mismos de la ateromatosis:
- Sexo masculino.
- Edad mayor de 60 años.
- Raza blanca (esto no tiene una explicación muy clara, porque la aterosclerosis es más frecuente en la raza negra, pero la manifestación clínica que muchas veces hace sospechar la enfermedad es la manifestación cutáneas, probablemente en la raza negra es más difícil visualizarla por el color de piel).
- Hipertensión arterial.
- Tabaquismo.
- Diabetes mellitus.
- Morbilidad previa importante, como cardiopatía coronaria, accidentes cerebrovasculares, aneurisma de la aorta abdominal, nefropatía isquémica y enfermedad vascular periférica.
Las primeras comunicaciones de embolía de cristales de colesterol demostraban que la mitad de los pacientes tenían embolías espontáneas, pero en la actualidad esto ha ido disminuyendo y sólo alrededor de10% de los pacientes que tienen embolía documentada no presentan un procedimiento endovascular ni administración de un medicamento de riesgo, y se las ha considerado espontáneas. No solamente es necesario tener placas ateroscleróticas, sino que deben desprenderse por algún motivo, es decir, se necesitan factores precipitantes.
La placa aterosclerótica, está compuesta por una cápsula fibrosa que cubre un núcleo de detritus necróticos, cristales de colesterol extracelulares y macrófagos.
Hay placas ateroscleróticas vulnerables y eso se ha visto a nivel coronario y aórtico. La placa aterosclerótica vulnerable presenta una cápsula fibrosa delgada y un gran núcleo rico en lípidos; el estrés mecánico o hemodinámico lleva a rotura de la cápsula y a la liberación del núcleo, que contiene cristales de colesterol que se van a depositar en pequeñas arterias distales de cualquier órgano, pero como habitualmente esto se origina en la aorta abdominal o torácica, las manifestaciones que predominan pueden ser renales o de las extremidades inferiores.
En estos pacientes hay factores de riesgo y comorbilidad, pero no bastan, en la mayoría de los casos, y deben existir factores precipitantes.
Factores precipitantes
En la actualidad la mayoría de los pacientes tienen uno o múltiples factores precipitantes:
- Cateterización aórtica diagnóstica o terapéutica.
- Cirugías vasculares de aneurismas de la aorta, cirugías coronarias, etc.
- Terapia anticoagulante (alrededor de 30% a 40% de los pacientes están anticoagulados). El paciente del caso clínico estaba anticoagulado.
- Trombolisis: se ha descrito sólo en forma anecdótica, los grandes ensayos de trombolisis no encontraron esta complicación, probablemente por seguimientos cortos y la ausencia de una búsqueda activa de esta patología.
- Disección aórtica: Hubo un paciente en la unidad coronaria, con accidente vascular y embolía de colesterol en el fondo de ojo, secundario a una disección aórtica que se operó. Esto es excepcional.
- Trauma abdominal cerrado en que probablemente puede haber lesión y contusión de la aorta.
Anatomía patológica
Los cristales de colesterol se depositan en arteriolas de 150 a 200 micrones de diámetro. Esto lleva a una reacción de cuerpo extraño, con macrófagos y células gigantes que se empiezan a producir precozmente en animales; a la semana ya existen células gigantes, aparición de eosinófilos al lado de estas lesiones, lo que probablemente explica la eosinofilia periférica, sumada a una reacción endotelial, con proliferación de la íntima, fibrosis y estrechamiento del lumen, que produce isquemia distal.
Las biopsias se fijan con formalina; los cristales de colesterol desaparecen y lo que queda es la marca de los cristales que son unas hendiduras (clefts), en forma de agujas biconvexas, en el lumen vascular y tienen una reacción inflamatoria, a veces producida por polimorfonucleares con fibrosis y alteraciones de la íntima. Los cristales de colesterol no se retiran por fagocitosis y pueden persistir durante meses. En animales de experimentación, a los seis meses aún pueden persistir cristales que producen daño.
En el riñón generalmente se localiza en arteriolas arcuatas e interlobulares, pero se pueden encontrar en vasos distales como la arteriola aferente o el glomérulo.
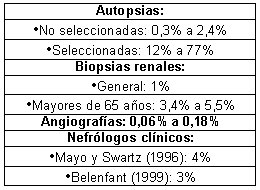
En autopsias no seleccionadas, alrededor de 1% de los pacientes tienen embolías de colesterol documentadas por biopsias, pero si se seleccionan pacientes sobre una cierta edad o con ateromatosis grave, en más de 50% se encuentran estas lesiones. Por tanto, está claramente disociada la clínica de la anatomía patológica; esto llevó a que se la considerara una enfermedad anatomopatológica más que una enfermedad clínica.
Uno por ciento de las biopsias renales tienen ateroembolía, pero cuando se hace en pacientes sobre 75 años alrededor de 4% de las biopsias pueden tener cristales de colesterol.
Cabe destacar que como complicación de estudios angiográficos (el factor precipitante de mayor importancia) se decribe embolía de colesterol hasta el 0,18%, lo cual traduce una disociación entre el diagnóstico clínico y las series de autopsia o biopsia.
Los nefrólogos clínicos de hospitales terciarios han observado que hasta en el 4% de sus interconsultas se plantea la embolía de cristales de colesterol como la enfermedad que probablemente explica las manifestaciones clínicas de sus pacientes, impresión que nosotros compartimos, ya que en la actualidad planteamos este diagnóstico cada 2 a 3 meses en nuestro hospital. Esto mismo se vio en un estudio francés, en el que 3% de los pacientes que ingresaba a la unidad de nefrología intensiva tenían embolía de colesterol documentada.
Epidemiología
 Tamaño completo
Tamaño completo Clínica
Los síntomas dependen de la cuantía y origen de los cristales de colesterol. Con respecto al origen, si está bajo la bifurcación de las carótidas no hay manifestaciones neurológicas, si está bajo las arterias renales no hay manifestaciones renales. Depende también de la cuantía y esto tiene importancia, ya que diferencia tres tipos de presentaciones clínicas frecuentes:
- El que se diagnostica en forma inmediata, el paciente es sometido a un procedimiento angiográfico y en el día, o al día siguiente, aparecen lesiones cutáneas de ateroembolía; traduce una liberación masiva de cristales de colesterol.
- La segunda forma, que es la más frecuente, se caracteriza porque las manifestaciones clínicas aparecen después de una semana del factor precipitante; en promedio el diagnóstico se establece en 4 a 8 semanas, por lo cual se pesquisa generalmente en forma ambulatoria.
- Otra forma es la de los pacientes con función renal deteriorada, pero estable, que se consideran casos de nefroesclerosis, enfermedades renovasculares bilaterales, etc. A veces a estos enfermos se les ha sometido a biopsia y se han documentado cristales de colesterol.
Una forma rara es aquella que se parece a una vasculitis sistémica con compromiso del estado general, fiebre, deterioro de la función renal, baja del complemento, etc.
Los síntomas, cuando se presentan, pueden estar documentados a nivel:
- renal
- cutáneo
- gastrointestinal
- sistema nervioso central
Rara vez se ha descrito compromiso pulmonar (síndrome riñon-pulmón).
Manifestaciones renales
El compromiso renal se presenta en más de 50% de los casos. Puede pasar inicialmente inadvertido. El diagnóstico se realiza, en promedio, a las 6 a 8 semanas. Se presenta como deterioro de la función renal: agudo cuando existe una embolía importante (35%), subagudo cuando existen placas que embolizan en forma recurrente (55%), o crónico, en que aparecen cristales de colesterol en pacientes que tienen un deterioro estable de la función renal (10%). Entre 30% y 60% necesitan diálisis y sólo un tercio de ellos se recuperarán parcialmente.
Es frecuente la aparición de hipertensión arterial acelerada o de novo. Es raro el dolor lumbar y hematuria macroscópica (que hace sospechar embolía de mayor tamaño).
Manifestaciones cutáneas
Es variable, entre 35% y 90% presenta manifestaciones cutáneas, y es más frecuente en las series recientes, en las cuales estas manifestaciones se buscan intencionadamente. Pueden ser:
-Clásicas
- Síndrome ortejo azul/púrpura, que se observan como lesiones pequeñas, violáceas, dolorosas, localizadas distalmente en las extremidades inferiores. Muchas veces los pulsos distales están conservados.
- Livedo reticularis, frecuente en extremidades inferiores y en los glúteos, que se visualizan como cianosis en forma de malla.
-Otras manifestaciones
- gangrena
- cianosis
- ulceración
- nódulos
- púrpura
A veces los pacientes aportan el antecedentes de las lesiones cutáneas, pero no fueron presenciadas por algún médico.
Compromiso digestivo
El compromiso clínico digestivo es bastante frecuente, entre 18% y 48%. Los síntomas y signos más frecuentes son el dolor abdominal y la hemorragia digestiva. Otras manifestaciones incluyen el infarto y la perforación intestinal, los pseudopólipos colónicos, la pancreatitis aguda, la colecistitis necrotizante alitiásica y la hepatitis.
Manifestaciones neurológicas
Son menos frecuentes (4% a 23%) y pueden incluir las siguientes:
- infartos cerebrales,
- accidentes isquémicos transitorios,
- estados de confusión inexplicados,
- deterioro orgánico cerebral inexplicado,
- compromiso medular, y
- embolías retinales (Cuerpos de Hollenhorst): Se observan en 10% a 20% de los pacientes, pero son diagnósticas, y deben buscarse de rutina y en forma seriada.
Laboratorio
Las alteraciones son inespecíficas pero orientadoras. Entre ellas están las siguientes:
- aumento de nitrógeno ureico y creatinina;
- hematuria microscópica en 40%, aproximadamente;
- proteinuria no nefrótica, entre 50 y 60%;
- eosinofilia, que suele presentarse entre los 10 y 21 días, y ocurre en formas variables, entre 20% y 70% de los enfermos;
- hipocomplementemia, clásico, pero raro en la actualidad;
- marcadores de inflamación: aumento de VHS, proteina C reactiva, fibrinógeno;
- Compromiso de órganos específicos, manifestado por aumento de amilasa, de CK, de LDH, de transaminasas, de fosfatasas alcalinas, etc.
Para diagnosticar esta enfermedad se debe tener un alto índice de sospecha, sobre todo en pacientes añosos, ateromatosos, que presentan falla renal aguda o subaguda, y tienen factores precipitantes de ateroembolía.
Lo idealmente es hacer una confirmación biópsica, que puede ser renal, cutánea, muscular o gastrointestinal. El problema está en que una biopsia negativa no descarta el diagnóstico. Se debe realizar fondo de ojo, en busca de cuerpos de Hollenhorst. No es necesaria la biopsia renal de rutina, para hacer el diagnóstico, y se puede hacer sólo con bases clínicas.
Belenfant, en 1999, publicó su serie de 67 pacientes, que recolectó durante años en una unidad intensiva nefrológica, y encontró que todos ellos tenían ateroesclerosis difusa, 64 pacientes habían tenido exposición a un factor precipitante conocido, como cateterización aórtica retrógrada, cirugía cardíaca o vascular, y terapia anticoagulante de 24 horas, a lo menos; 63 de los 67 pacientes tenían insuficiencia renal aguda o subaguda, con aumento de creatinina en más de 50% del valor basal, luego de exposición a un factor precipitante, y la mayoría de estos pacientes presentaban livedo reticularis, necrosis cutánea, ortejos azules o evidencia fundoscópica de embolía de cristales de colesterol. Ellos buscaban las lesiones en forma dirigida. Si uno se da cuenta de que los pacientes cumplen estos tres requisitos, el diagnóstico es virtualmente de certeza. Cuando se produce un factor precipitante, en un paciente predispuesto, y cumple los tiempos, si el laboratorio apoya y hay lesiones cutáneas, la enfermedad se puede diagnosticar con alta probabilidad sin necesidad de tener confirmación biópsica (la cual debe realizarse sobre todo en las lesiones cutáneas, ya que por la gravedad de estos pacientes, es difícil realizar, de rutina, una biopsia renal).
Diagnóstico diferencial
- Nefropatía por medio de contraste: lo más importante es que la nefropatía por contraste es precoz, dentro de unos pocos días, en cambio, la ateroembolía se presenta frecuentemente semanas después de un factor precipitante conocido.
- Vasculitis sistémica.
- Nefritis intersticial aguda: en esta enfermedad existe deterioro de la función renal, muchas veces asociado a eosinofilia y rash cutaneo, por lo cual se puede confundir.
- Endocarditis infecciosa.
Tratamiento
No existe tratamiento especifico de utilidad documentada, sólo hay informes anecdóticos de beneficios:
- Corticoides: se han utilizado frente a hemorragias pulmonares, o en pacientes con manifestaciones generales marcadas, pero sólo en casos aislados.
- Estatinas: tienen el potencial de estabilizar las placas de ateroma, pero no existe evidencia sólida para recomendar su uso.
- Pentoxifilina: También hay sólo informes anecdóticos.
Los mejores resultados se han conseguido con tratamiento conservador.
Tratamiento conservador
Evitar recurrencia de ateroembolía: evitar todos los factores precipitantes y no someter al paciente a nuevos procedimientos que puedan llevar a episodios recurrentes de ateroembolía:
- Suspender tratamiento anticoagulante.
- Proscribir cateterización aórtica o cirugía vascular, salvo situaciones de emergencia vital.
- Tratar o prevenir la insuficiencia cardíaca: control de presión arterial, la ideal es 140/80 mm Hg o menos, con vasodilatadores, incluyendo los inhibidores ECA, que tienen un efecto beneficioso en insuficiencia cardíaca.
- Evitar y tratar la desnutrición: nutrirlos adecuadamente y, si es necesario, apoyarlos con nutrición enteral o parenteral.
- Diálisis cuando exista insuficiencia renal severa o sobrecarga de volumen no manejable por otros métodos. No está definido si la hemodiálisis o la peritoneodiálisis es superior. La peritoneodiálisis no necesita anticoagulación pero muchos de estos pacientes tienen compromiso digestivo que dificulta su uso; se puede usar cualquiera de las dos técnicas, pero, si es hemodiálisis, debe evitarse la anticoagulación.
- Permitir procedimientos invasivos (cateterismo o cirugía vascular) sólo frente a situaciones de riesgo vital. Tratar de manejar al paciente con tratamiento médico, sin someterlo a un nuevo procedimiento de alto riesgo.
Pronóstico
Clásicamente el pronóstico vital es malo, con mortalidad, al año, de 64% a 87%. Las causas principales de muerte son las siguientes:
- cardíacas,
- gastrointestinales,
- accidentes cerebrovasculares,
- aneurismas aórticos rotos.
Con el tratamiento conservador “agresivo”, que vimos recién, la sobrevida al año es de 69% a 79%, y, a los dos años, sobre el 50%, lo cual es esperanzador, ya que se está produciendo un cambio en la evolución natural de esta enfermedad, de muy mal pronóstico hasta hace pocos años.
Conclusión
Si nosotros vemos este caso, a pesar de que no hay biopsia, es bastante compatible con una embolía por cristales de colesterol, ya que tuvo un procedimiento vascular precipitante, múltiples factores de riesgo cardiovascular, no tiene la evolución temporal de la nefropatía por medio de contraste, su insuficiencia renal se produce desde la semana hacia delante, es progresiva, no mejora tanto y se acompaña de lesiones cutáneas que fueron documentadas por los médicos, es decir, tiene criterios clínicos para pensar que este cuadro corresponde a una embolía de cristales de colesterol.

