Publicado el 1 de julio de 2006 | http://doi.org/10.5867/medwave.2006.06.2305
Resistencia insulínica e hipertensión arterial I: mecanismos
Insulin resistance and hypertension I: mechanisms
Resumen
La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y la Sociedad Chilena de Nefrología.
Introducción
“De los pacientes que han tenido infarto agudo del miocardio, el 60% tienen resistencia a la insulina, es decir, presentan una glicemia de ayuno elevada, intolerancia a la glucosa o diabetes.”
El concepto de resistencia a la insulina nació en 1920, cuando Kylin designó el síndrome metabólico como la agrupación de hipertensión, hiperglicemia y gota (Kylin E. Zentralblatt fuer Innere Medizin 1923; 44: 105-27). En 1947, Vague agregó a esta definición, la distribución centrípeta de la grasa, como una característica muy importante del síndrome de resistencia a la insulina y su relación con la enfermedad cardiovascular. Es la resistencia a la insulina la que hoy le da la mayor importancia a este síndrome. En 1988, Reaven definió, a nivel internacional, lo que se conoce hoy por varios nombres, como “Síndrome de resistencia a la insulina”, “El Cuarteto de la muerte”, “Síndrome Metabólico o “Síndrome X” (Reaven GM. Diabetes 1988 37: 1595-1607).
La resistencia a la insulina se define, desde el punto de vista biológico, como la disminución de la capacidad de la insulina para ejercer sus acciones en los órganos diana, en especial el hígado, el músculo esquelético y el tejido adiposo. Esta alteración causa una hiperinsulinemia de ayuno para mantener la euglicemia. Antes sin embargo, se produce una hiperinsulinemia postprandial, muy frecuente en los insulinorresistentes obesos. La causa de que los tejidos se “resistan” a la acción de la insulina no está clara, pero hoy se sabe que la obesidad intraabdominal, también conocida como obesidad visceral, se asocia estrechamente con la insulino-resistencia.
Resistencia insulínica e hipertensión arterial
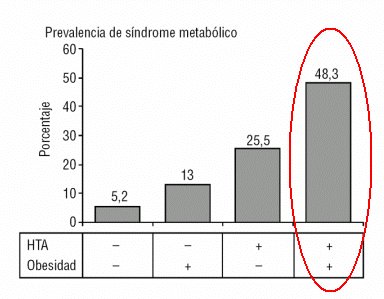
Los dos factores que hoy se consideran como los más importantes en el desarrollo del síndrome metabólico son la hipertensión y la obesidad, y se puede ver que cuando ambos están presentes la prevalencia de este síndrome es casi de 50% (Fig.1). Por otro lado 25% a 40% de los hipertensos no obesos y no diabéticos tienen resistencia a la insulina y más de 50% de los obesos son hipertensos.
 Tamaño completo
Tamaño completo Figura 1. Influencia de la HTA y la obesidad en la prevalencia del síndrome metabólico
En cuanto a los aspectos fisiopatológicos de la relación entre resistencia insulínica, hiperinsulinemia e hipertensión arterial, el mayor contribuyente molecular al desarrollo de la resistencia insulínica es el exceso de ácidos grasos libres. Estos son los principales responsables de toda la cascada de episodios que van a causar el síndrome metabólico. Estos ácidos grasos provienen de la lipólisis de las grasas y son liberados por la lipasa lipoproteica. Una de las principales acciones de la insulina, normalmente, es ejercer un efecto antilipólisis.
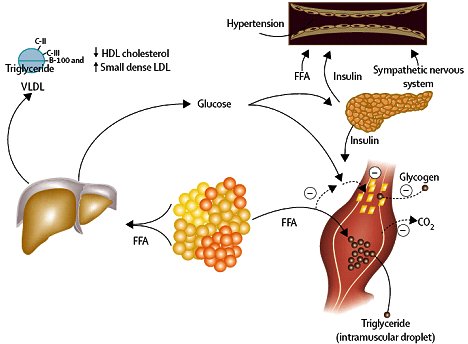
Los ácidos grasos libres aumentan la producción hepática de glucosa y triglicéridos, y la producción de lipoproteínas de muy baja densidad (VLDL), lo que explica la dislipidemia aterogénica que caracteriza a este síndrome. Se produce así mismo, una disminución del colesterol HDL, que es la molécula que devuelve el colesterol al hígado (transporte reverso), y aumentan, por otro lado, las partículas de LDL densas, que son muy aterogénicas, ya que son las que más se oxidan, formando la placas ateroescleróticas. Por otro lado, estos ácidos grasos libres originan resistencia a la acción periférica de la insulina y aumentan la insulina plasmática, y ésta a su vez, actúa en el músculo esquelético disminuyendo la formación de glicógeno y aumentando el depósito intramuscular de triglicéridos. Además, la hiperinsulinemia produce retención de sodio y agua y activación del sistema nervioso simpático, favoreciendo al desarrollo de hipertensión arterial (Fig. 2).
 Tamaño completo
Tamaño completo Figura 2. Fisiopatología del síndrome metabólico y de la resistencia a insulina (Eckel R. The Lancet, 2005;365:1415)
En forma concomitante y contribuyendo con el síndrome de resistencia insulínica producido por el exceso de ácidos grasos libres, están los efectos paracrinos y endocrinos del estado proinflamatorio. Este estado es producido por una variedad de células en el tejido adiposo que incluye monocitos y adipocitos. En las personas insulinorresistentes, estas células producen IL-6 y factor de necrosis tumoral. La inflamación que se produce es un fenómeno importante dentro de la fisiopatología del síndrome metabólico: la producción elevada de IL-6 eleva la producción de proteína C reactiva a nivel hepático; la IL-6 y otras citoquinas pueden elevar más la producción de glucosa en el hígado y estimulan la lipólisis en el tejido adiposo, con generación de más ácidos grasos, produciéndose más insulinorresistencia. Por otra parte, las mismas citoquinas aumentan la producción de agentes protrombóticos. Lo anterior, sumado a la cascada metabólica que se está produciendo por la resistencia a la insulina, determina un estado proinflamatorio y protrombótico que aumenta el riesgo de episodios cardiovasculares.
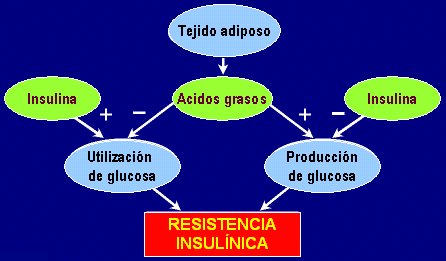
Se puede decir entonces, que los ácidos grasos libres que resultan del aumento de la lipólisis son un factor importante en la relación entre obesidad e insulinorresistencia, ya que disminuyen la utilización de glucosa a nivel del músculo, afectan la función de éste y aumentan la producción de insulina a nivel plasmático. Ambos hechos conducen a un estado de resistencia insulínica importante (Fig. 3).
 Tamaño completo
Tamaño completo Figura 3. Papel de los ácidos grasos libres en la relación entre obesidad e insulinorresistencia
Cuando se habla de relación o asociación entre dos hechos, no significa que uno sea la causa del otro. Para que un factor sea “causal” debe cumplir una serie de requisitos, que son los llamados criterios epidemiológicos de causalidad. La resistencia a la insulina no cumple todos los criterios de causalidad epidemiológica para considerarla “causa” de hipertensión arterial. No obstante, sí existe una relación muy estrecha entre ambos factores, como lo ha demostrado Ferranini et al (N Engl J Med 1987; 317:350). Hoy lo que se acepta, es que la hipertensión es un componente más del síndrome metabólico, lo que no significa que haya una relación de causa-efecto. La relación entre hipertensión e insulinorresistencia se ha confirmado en varios estudios longitudinales, sin embargo, no todos los resultados han sido concordantes. Esto es importante, ya que cuando hablamos de factores causales debe haber “concordancia epidemiológica” en todos los estudios publicados. Como ejemplo, hace poco se publicó el estudio ARIC (Atherosclerosis Risk In Communities), en el que no se demostró causalidad entre resistencia insulínica e hipertensión: al ajustar los resultados por obesidad, que es un factor importante en el síndrome metabólico, se perdía la relación existente entre ambas. Por lo tanto, el papel causal de la resistencia a la insulina en el desarrollo de la hipertensión sigue siendo controvertido, lo que no quiere decir que no exista una profunda relación fisiopatológica entre la hipertensión y la resistencia a la insulina, como lo ha demostrado el Dr Haffner en un estudio con un “n” grande, longitudinal, realizado al respecto (Haffner, Arch Int Med, 1996).
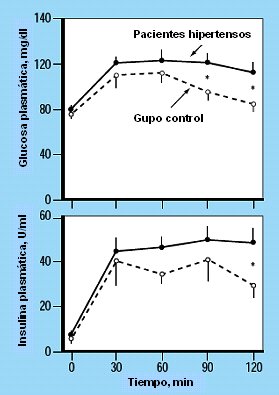
Algunas evidencias apoyan la teoría de que la resistencia a la insulina puede anteceder al desarrollo de la hipertensión. Existe, por ejemplo evidencia que la insulinemia de ayuno se asocia con la presión arterial sistólica, evidencia concreta, válida y establecida por muchos estudios. Otro ejemplo es que en los parientes normotensos de primer grado de hipertensos esenciales, se detecta insulinorresistencia si se les realiza una prueba de resistencia insulínica, como el HOMA (Homeostatic Model Assessment). Otra evidencia que apoya esta teoría es que la caída de la presión arterial cuando un obeso baja de peso, se relaciona con una mejoría de la sensibilidad a la insulina. Existen también estudios que muestran que los pacientes que son tratados con insulina no presentan aumento de la presión arterial, lo que también habla en favor de la relación. Por último, está el hecho de que los fármacos que aumentan la sensibilidad a la insulina, como las glitazonas, atenúan el desarrollo de la hipertensión y bajan la presión arterial. Como ejemplo, en un estudio de Ferranini et al (Fig. 4) se demuestra que en un test de tolerancia a la glucosa en los sujetos con HTA, los niveles de glucosa e insulina tienden a ser más elevados. Esto sugiere que los pacientes hipertensos son, efectivamente, insulinorresistentes. En otro estudio, el Dr Julius demostró que el nivel de insulina es mucho menor en los sujetos normales, es decir, no hipertensos, que en los portadores de hipertensión crónica. El estudio se publicó en la década de 1990 y su interés radica en que el autor estudió el curso natural del síndrome metabólico y su relación con la hipertensión (Julius et al., Hypertension 16, 1990).
 Tamaño completo
Tamaño completo Figura 4. Respuesta a sobrecarga de glucosa en hipertensos y normotensos
Otros estudios que apoyan la relación resistencia insulínica-HTA se evidencian en un estudio publicado por Raji et al, quién describió que la mejoría de la resistencia insulínica se asocia con reducción de la presión arterial en sujetos tratados con una glitazona, es decir, con un sensibilizador insulínico. En su estudio, el delta en la presión sistólica fue cayendo en la medida que aparecían cambios en la sensibilidad a la glucosa mediada por la glitazona (Raji A et al. Diabetes Care. 2003;26:172-8).
En resumen, la hipertensión y la resistencia a la insulina guardan una “relación epidemiológica” estrecha, pero esta relación no es uno a uno, como se pide a los factores causales (por ejemplo: colesterol y enfermedad ateroesclerótica), sino que más bien corresponde a fenotipos que se están mezclando.
Con respecto a la posibilidad de que exista una relación inversa, es decir, que la hipertensión lleve a resistencia insulínica, se puede decir que esta hipótesis ha ido cayendo en descrédito, ya que la insulinorresistencia no se presenta en los pacientes con hipertensión arterial secundaria (por ejemplo, hipertensos renovasculares que no son insulinorresistentes). Además, al bajar la presión arterial en hipertensos que tienen resistencia insulínica no necesariamente éstos mejoran la sensibilidad del músculo a la insulina, y por el contrario, en algunos pacientes, el tratamiento antihipertensivo empeora la insulinorresistencia.
Mecanismos de hipertensión en la insulinorresistencia
Los mecanismos que generan hipertensión en los pacientes con síndrome de resistencia a la insulina son: a) la hiperactividad del sistema nervioso simpático; b) la alteración del sistema renina-angiotensina; c) el desequilibrio entre los efectos vasodilatadores y el efecto retenedor de sal de la insulina y d) la obesidad intraabdominal asociada con inflamación y con disminución de la adiponectina.
El tono del sistema nervioso simpático aumenta después de la infusión de insulina en sujetos con peso normal. Por el contrario, en los sujetos con hiperinsulinemia crónica como los obesos, la actividad simpática se mantiene basalmente aumentada. Fundamentalmente en los pacientes obesos, se ha demostrado que la hiperinsulinemia, el resultado de la resistencia a la insulina, estimula el sistema simpático. Este aumento contribuye a la hipertensión estimulando en el corazón el débito cardíaco, a nivel de vasos sanguíneos, produciendo vasoconstricción, y a nivel renal produciendo reabsorción de sodio y agua (Reaven et al, NEJM 1996). Un trabajo muy interesante, que demuestra la actividad simpática en pacientes con resistencia a la insulina es el de Facchini et al. La frecuencia cardíaca en forma normal, disminuye en la noche. Ellos describieron que en pacientes con resistencia insulínica, la frecuencia cardíaca nocturna se correlacionaba muy bien con el grado de sensibilidad a la insulina (Facchini FS et al. AJH 1996; 9:1013-17).
También se ha demostrado que el intervalo QT del electrocardiograma, que es otro marcador del tono adrenérgico, aumenta después de administrar insulina (efecto en el nivel de cationes intramiocárdicos) en los pacientes insulinorresistentes, hecho importante en lo que se refiere a hipertensión y morbilidad cardiovascular, porque el aumento permanente del QT en los obesos insulinorresistentes podría favorecer a la aparición de arritmias ventriculares. Este es un hecho muy importante ya que los pacientes insulinorresistentes son sujetos con una actividad simpática aumentada mantenida, y en los sujetos obesos existe un aumento de la sensibilidad de la grasa a las catecolaminas. En presencia de un intervalo QT prolongado estos sujetos podrían estar más predispuestos a presentar muerte súbita.
Es importante considerar, cuando se habla de la respuesta hiperadrenérgica en la insulinorresistencia, que en condiciones normales la insulina tiene una acción vasodilatadora. Esta acción hace que se confunda la relación entre insulinemia e hipertensión. En humanos, se ha demostrado que la acción vasodilatadora de la insulina es, en parte, contrarrestada por la acción del sistema nervioso simpático. Se ha postulado entonces, que en pacientes obesos e hipertensos la acción dilatadora de la insulina es antagonizada por el sistema simpático. En este mismo sentido, se sabe que la infusión de insulina disminuye la presión arterial diastólica, pero no la sistólica, de manera que podría aumentar la presión de pulso, lo que es muy deletéreo para la función del endotelio. Un efecto importante de la insulina también es el de la retención de sodio, por su efecto antinatriurético.
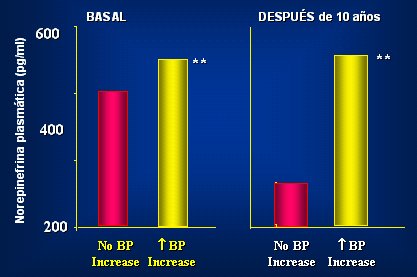
Por último, se sabe que en pacientes obesos insulinorresistentes los niveles plasmáticos de epinefrina y norepinefrina se encuentran elevados y asimismo, los niveles de cortisol son mayores, es decir, se simula la respuesta de “estrés”. Un trabajo que demuestra lo anterior es el de Matsuo et al, en que, en sujetos normotensos en que se midió niveles de norepinefrina, a los diez años de seguimiento, el número de sujetos que se tranformó en hipertenso fue mayor en aquellos que tenían niveles más altos de norepinefrina basales. A su vez, los sujetos hipertensos a los 10 años tenían mayores niveles de esta catecolamina (Fig. 5).
Los mecanismos que generan hipertensión en los pacientes con síndrome de resistencia a la insulina son: a) la hiperactividad del sistema nervioso simpático; b) la alteración del sistema renina-angiotensina; c) el desequilibrio entre los efectos vasodilatadores y el efecto retenedor de sal de la insulina y d) la obesidad intraabdominal asociada con inflamación y con disminución de la adiponectina.
El tono del sistema nervioso simpático aumenta después de la infusión de insulina en sujetos con peso normal. Por el contrario, en los sujetos con hiperinsulinemia crónica como los obesos, la actividad simpática se mantiene basalmente aumentada. Fundamentalmente en los pacientes obesos, se ha demostrado que la hiperinsulinemia, el resultado de la resistencia a la insulina, estimula el sistema simpático. Este aumento contribuye a la hipertensión estimulando en el corazón el débito cardíaco, a nivel de vasos sanguíneos, produciendo vasoconstricción, y a nivel renal produciendo reabsorción de sodio y agua (Reaven et al, NEJM 1996). Un trabajo muy interesante, que demuestra la actividad simpática en pacientes con resistencia a la insulina es el de Facchini et al. La frecuencia cardíaca en forma normal, disminuye en la noche. Ellos describieron que en pacientes con resistencia insulínica, la frecuencia cardíaca nocturna se correlacionaba muy bien con el grado de sensibilidad a la insulina (Facchini FS et al. AJH 1996; 9:1013-17).
También se ha demostrado que el intervalo QT del electrocardiograma, que es otro marcador del tono adrenérgico, aumenta después de administrar insulina (efecto en el nivel de cationes intramiocárdicos) en los pacientes insulinorresistentes, hecho importante en lo que se refiere a hipertensión y morbilidad cardiovascular, porque el aumento permanente del QT en los obesos insulinorresistentes podría favorecer a la aparición de arritmias ventriculares. Este es un hecho muy importante ya que los pacientes insulinorresistentes son sujetos con una actividad simpática aumentada mantenida, y en los sujetos obesos existe un aumento de la sensibilidad de la grasa a las catecolaminas. En presencia de un intervalo QT prolongado estos sujetos podrían estar más predispuestos a presentar muerte súbita.
Es importante considerar, cuando se habla de la respuesta hiperadrenérgica en la insulinorresistencia, que en condiciones normales la insulina tiene una acción vasodilatadora. Esta acción hace que se confunda la relación entre insulinemia e hipertensión. En humanos, se ha demostrado que la acción vasodilatadora de la insulina es, en parte, contrarrestada por la acción del sistema nervioso simpático. Se ha postulado entonces, que en pacientes obesos e hipertensos la acción dilatadora de la insulina es antagonizada por el sistema simpático. En este mismo sentido, se sabe que la infusión de insulina disminuye la presión arterial diastólica, pero no la sistólica, de manera que podría aumentar la presión de pulso, lo que es muy deletéreo para la función del endotelio. Un efecto importante de la insulina también es el de la retención de sodio, por su efecto antinatriurético.
Por último, se sabe que en pacientes obesos insulinorresistentes los niveles plasmáticos de epinefrina y norepinefrina se encuentran elevados y asimismo, los niveles de cortisol son mayores, es decir, se simula la respuesta de “estrés”. Un trabajo que demuestra lo anterior es el de Matsuo et al, en que, en sujetos normotensos en que se midió niveles de norepinefrina, a los diez años de seguimiento, el número de sujetos que se tranformó en hipertenso fue mayor en aquellos que tenían niveles más altos de norepinefrina basales. A su vez, los sujetos hipertensos a los 10 años tenían mayores niveles de esta catecolamina (Fig. 5).
 Tamaño completo
Tamaño completo Figura 5. Comparación de los niveles de norepinefrina en normotensos seguidos a 10 años (Adaptado de Matsuo et al, Am J Hypertension 1997)
Con respecto al papel del sistema renina-angiotensina y su relación con hipertensión en sujetos con resistencia a la insulina, existen evidencias indirectas que apoyan una relación. Una de estas evidencias proviene del estudio HOPE (Heart Outcomes Prevention Evaluation, JAMA 2001;286:1882), en el que el inhibidor de la enzima convertidora de angiotensina (IECA), ramipril, disminuyó el riesgo de desarrollar diabetes en 34%, en una población con alto riesgo cardiovascular. Se debe recordar que la diabetes es la máxima expresión de la resistencia a la insulina, de modo que este hallazgo es muy importante desde el punto de vista de la fisiopatología de la hipertensión arterial en la resistencia insulínica. En la misma dirección, un metaanálisis posterior, de una serie de estudios realizados con antagonistas del receptor de angiotensina II (ARA II), demostró que estos fármacos disminuyen un 22% el desarrollo de diabetes, es decir, de alguna forma evitarían el desarrollo de la resistencia a la insulina en estos pacientes.
Por otra parte, se ha demostrado que los adipocitos, que están aumentados en los pacientes insulinorresistentes, y en máximo grado en los que son obesos, producen angiotensinógeno, producen una mayor cantidad de enzima convertidora de angiotensina y quimasa, que aumenta la conversión de angiotensina I a II, y también estos adipocitos expresan más los receptores AT1. La angiotensina II disminuye la adipogénesis e induce lipólisis, aumentando los ácidos grasos libres e induciendo resistencia insulínica e hiperglicemia. Se ha demostrado que a mayor resistencia insulínica, mayor es la expresión de AT1 en biopsias de sujetos insulinorresistentes. En modelos de ratas insulinorresistentes también se ha demostrado que los IECA y ARA II disminuyen los niveles de insulina, triglicéridos y de ácidos grasos libres. Dada las consecuencias del aumento de angiotensina II en estos pacientes, algunos autores postulan que es esta molécula la que lleva a la hipertensión en la insulinorresistencia.
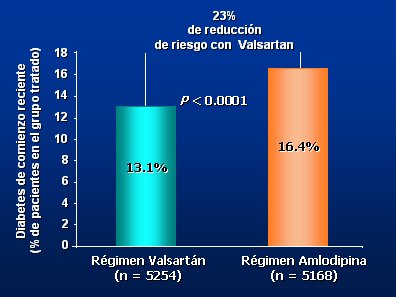
Julius ha afirmado que los grandes estudios multicéntricos apoyan el concepto fisiopatológico de insulinorresistencia en la hipertensión (Stevo Julius, Metabolic Syndrome Simposium 2004). Un ejemplo de esta aseveración es el estudio VALUE (Valsartan Antihypertensive Long-term Use Evaluation), en el que se comparó el ARA II valsartán con un antagonista del calcio dihidropiridínico, amlodipino. Se encontró que en el grupo tratado con el ARA II la aparición de diabetes disminuyó en 23%. Estos resultados son muy importantes desde el punto de vista de la salud pública, porque se prevé que en el año 2020, la prevalencia de diabetes en el mundo habrá aumentado en más de 50% (Fig. 6).
 Tamaño completo
Tamaño completo Figura 6. VALUE: Incidencia de diabetes de comienzo reciente
En una serie de estudios en hipertensión, se ha demostrado que sólo los ARA II y los IECA son eficaces en prevenir la aparición de diabetes (Opie and Schall J. Hyperts 22:1453-1458, 2004). Varios estudios nuevos, sin embargo, están en curso y entregarán más información acerca de la relación entre el sistema renina-angiotensina, la insulinorresistencia y la hipertensión arterial. Entre ellos están el estudipo TRIM (Telmisartan en Reducción de lípidos Intra-Miocelulares) en pacientes con resistencia insulínica, cuyo objetivo es analizar el efecto de este fármaco en el desarrollo de diabetes, hipertensión y morbi-mortalidad cardiovascular, el ONTARGET (Ongoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) y el DREAM (Diabetes Reduction Assessment with ramipril and rosiglitazone Medication), que utilizan ARA II y glitazonas, que probablemente serán el tratamiento del futuro en este síndrome.
Otro mecanismo en la insulinorresistencia y que se relacionan con el sistema renina-angiotensina, es el de la producción de aldosterona, que es mediada por angiotensina II. La aldosterona puede cambiar la estructura y función vascular, alterar el flujo de cationes y activar el sistema nervioso simpático.
Por último, también se ha demostrado que la resistencia insulínica se asocia con alteraciones vasomotoras del lecho coronario, lo que plantea una alteración importante de la función del endotelio. Este efecto puede producir una disminución de la perfusión miocárdica hasta una tercera parte de lo normal (Quiñones MJ et al. Ann Intern Med 2004;140:700-8). En este contexto, se ha demostrado que a medida que el cuadro progresa desde resistencia insulínica a diabetes, las alteraciones vasomotoras coronarias van empeorando en forma progresiva, de modo que la reducción del flujo coronario llega a su máxima expresión en la diabetes, lo que empeora aún más, si se asocia hipertensión arterial (Prior JO et al. Circulation 2005;111:2291-8). Además, la insulinorresistencia eleva el riesgo de desarrollar daño de órganos blanco, es decir, aumenta el número de pacientes con microalbuminuria, que es un marcador de riesgo cardiovascular y de disfunción renal, y aumenta la presencia de hipertrofia ventricular (Leoncini G et al. J Intern Med. 2005;257:454-60).

