Estudios originales
← vista completaPublicado el 5 de julio de 2021 | http://doi.org/10.5867/medwave.2021.06.8231
Factores asociados a mortalidad en pacientes hospitalizados con COVID-19: cohorte prospectiva en un hospital de referencia nacional de Perú
Factors associated with mortality in patients hospitalized with COVID-19: A prospective cohort in a Peruvian national referral hospital
Resumen
Objetivos Describir las características clínicas y evaluar los factores asociados con la mortalidad de los pacientes adultos con la nueva enfermedad causada por coronavirus 2019 (COVID-19) ingresados a un hospital de referencia nacional de Perú.
Métodos Se realizó un estudio de cohorte prospectivo. Se incluyó a pacientes mayores de 18 años hospitalizados con el diagnóstico de infección por coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2). Se excluyó a quienes ingresaron con prueba rápida serológica positiva al ingreso, sin clínica sugestiva ni imágenes compatibles. Los datos se recolectaron a partir de la historia clínica.
Resultados Se incluyó un total de 813 adultos, 544 (66,9%) tuvieron COVID-19 confirmado. La media de la edad fue de 61,2 años (desviación estándar: 15) y 575 (70,5%) fueron de sexo masculino. Las comorbilidades más frecuentes fueron hipertensión arterial (34,1%) y obesidad (25,9%). Los síntomas más frecuentes al ingreso fueron disnea (82,2%) y tos (53,9%). Un total de 114 (14%) pacientes recibieron ventilación mecánica, 38 (4,7%) ingresaron a unidad de cuidados intensivos y 377 (46,4%) fallecieron. Se asociaron a la mortalidad el requerimiento de soporte ventilatorio, el mayor compromiso pulmonar y los marcadores inflamatorios. Encontramos que por cada 10 años que aumentó la edad, el riesgo de morir se incrementó en 32% (riesgo relativo: 1,32; intervalo de confianza 95%: 1,25 a 1,38). Aquellos pacientes que requirieron ingreso a unidad de cuidados intensivos y ventilación mecánica tuvieron 1,39 (intervalo de confianza 95%: 1,13 a 1,69) y 1,97 (intervalo de confianza 95%: 1,69 a 2,29) veces el riesgo de morir, respectivamente.
Conclusión La mortalidad encontrada en nuestro estudio fue alta y estuvo asociada a la edad, marcadores inflamatorios y compromiso respiratorio.
Ideas clave
- La mortalidad hospitalaria por COVID-19 ha sido un tema poco abordado en los países sudamericanos, donde las condiciones particulares de su sistema sanitario, económico y social han jugado un rol importante en esta pandemia.
- Este estudio evaluó los factores asociados a mortalidad de pacientes con COVID-19 hospitalizados en un centro de referencia nacional de Perú.
- A la fecha de redacción de este informe, nuestro estudio registra el mayor número de pacientes enrolados en Perú, en parte debido a que esta investigación se ejecutó durante el periodo de aumento de casos en la curva epidemiológica de pacientes diagnosticados con COVID-19.
- La principal limitación de este estudio radica en los registros incompletos de algunas variables como reacciones adversas a medicamentos, hábitos nocivos e índice de masa corporal, que podrían afectar la validez externa de los resultados obtenidos.
Introducción
Hacia finales del año 2020, la nueva enfermedad por el coronavirus 2019 (COVID-19) había cobrado casi 2 millones de muertes a nivel mundial según los reportes oficiales de la Organización Mundial de la Salud[1]. Perú es uno de los países más afectados por la actual pandemia, con un registro en abril de 2021 de más de mil muertos en exceso por millón de habitantes[2].
La mortalidad hospitalaria asociada a COVID-19, ha sido estudiada en diversas cohortes internacionales[3],[4],[5],[6]. Se ha determinado que factores como la edad y comorbilidades como las enfermedades cardiovasculares, diabetes y obesidad están asociados a mayor mortalidad en pacientes con COVID-19[7],[8]. Sin embargo, existe poca literatura de estudios en países sudamericanos donde las condiciones de su sistema sanitario, económico y social han jugado un rol importante en la mortalidad hospitalaria por COVID-19[9],[10],[11].
Este estudio se realizó con el objetivo principal de determinar los factores asociados a mortalidad de los pacientes adultos con COVID-19 ingresados a un hospital de referencia nacional de Perú. También busca describir sus características clínicas, manejo y evolución para determinar diferencias con otros países y detectar los grupos de pacientes con mayor riesgo de mortalidad.
Métodos
Diseño y población
Se realizó un estudio de cohorte prospectivo en el Hospital Nacional Edgardo Rebagliati Martins perteneciente al Seguro Social de Salud de Perú, EsSalud, el cual adaptó la mayor parte de su capacidad hospitalaria a la atención de pacientes con COVID-19. Este hospital es un centro de referencia nacional.
La población de estudio fue pacientes mayores de 18 años hospitalizados que ingresaron por el servicio de emergencia durante el periodo de un mes (del 22 de mayo al 21 de junio de 2020) con el diagnóstico de infección por coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) sospechosa o confirmada. No se realizó una estimación del tamaño de muestra debido a que se efectuó una selección no probabilística, incluyendo a todo el universo de pacientes en el estudio.
Se consideró como caso sospechoso a los pacientes que presentaban síntomas o imágenes (radiografía o tomografía) sugestivas de infección de COVID-19. Se consideró caso confirmado a los pacientes con una prueba diagnóstica positiva por el test de reacción en cadena de la polimerasa con transcriptasa inversa de hisopado nasofaríngeo (RT-PCR) o prueba serológica rápida (inmunoglobulinas M o G)[12]. Se excluyeron a los pacientes que ingresaron con prueba rápida serológica positiva con RT-PCR negativo o ausente y sin reporte de sintomatología sugestiva ni imágenes compatibles, debido a que se consideraron como posibles casos falsos positivos. Los autores extrajeron la información de la historia clínica (física o electrónica) de los pacientes enrolados desde el ingreso hasta el alta o fallecimiento. La revisión periódica de las historias clínicas facilitó la identificación de participantes y disminuyó las potenciales pérdidas en el estudio.
Variables
Se registraron datos demográficos (edad y sexo), clínicos, de imagen y laboratorio. Se consideraron los antecedentes patológicos más prevalentes: hipertensión arterial, diabetes mellitus, obesidad, enfermedad renal crónica, cardiopatía isquémica, asma, cáncer, enfermedad vascular cerebral, hipotiroidismo, enfermedad pulmonar intersticial difusa, cirrosis hepática, enfermedad pulmonar obstructiva crónica. La obtención del antecedente de obesidad se realizó según dos criterios:
- El índice de masa corporal obtenido mediante el registro disponible en la historia clínica del peso y talla del paciente.
- El diagnóstico de obesidad consignado en la historia clínica por el médico tratante.
Se incluyeron los resultados de las pruebas RT-PCR y rápida serológica (inmunoglobulina M, inmunoglobulina G o ambas). Asimismo, se describió la medicación previa a la hospitalización como tratamiento para COVID-19, los síntomas y las funciones vitales de ingreso.
Dentro de los exámenes auxiliares se consignaron los laboratorios del ingreso (hemograma, análisis bioquímico, hepático, coagulación, marcadores inflamatorios y gases arteriales) y estudios de imágenes. Se clasificó el grado de compromiso pulmonar mediante el porcentaje de afectación y la escala de COVID-19 Reporting and Data System (CORADS)[13].
Respecto a las variables de atención hospitalaria se contemplaron el manejo terapéutico, tipo de oxigenoterapia y complicaciones intrahospitalarias. En el seguimiento se consignó la necesidad de cuidados intensivos, uso de ventilación mecánica y el desenlace (alta o fallecimiento) indicando la fecha del evento.
Consideraciones éticas
El presente estudio representó un riesgo mínimo para los pacientes ya que no se tuvo contacto directo con ellos y no se recolectó información que permitiera identificarlos. Asimismo, solo los investigadores tuvieron acceso a los datos recolectados. El protocolo de investigación fue aprobado por el Comité de Ética en Investigación para COVID-19 del Seguro Social de Salud. Este protocolo se realizó en concordancia con la declaración de Helsinki y con el reporte de Belmont, en los cuales los autores se comprometen a respetar el anonimato del paciente en estudio.
Análisis estadístico
Se registró y almacenó la información en una base de datos en el programa Excel Microsoft 2016, para luego exportarla al programa STATA v14. Para resumir las variables categóricas se utilizaron frecuencias y porcentajes, mientras que para las variables cuantitativas se usaron medidas de tendencia central y dispersión, dependiendo de la distribución de los datos.
Se reportan el porcentaje de datos faltantes para cada variable. Debido a que la proporción de datos perdidos para la mayoría de las variables fue pequeña y a que se consideró que estos fueron al azar, se optó por no realizar argucias estadísticas para tratar los datos perdidos[14].
Para evaluar las asociaciones entre la mortalidad y las variables sociodemográficas, clínicas y de laboratorio, se realizaron pruebas de hipótesis de acuerdo con la naturaleza de las variables independientes. Para variables categóricas se utilizó Chi-cuadrado o prueba exacta de Fisher, mientras que para las variables cuantitativas se utilizó t de Student o U de Mann-Whitney.
Finalmente, se estimó el tamaño de efecto (riesgo relativo e intervalos de confianza al 95%) mediante la creación de modelos de regresión de Poisson con varianza robusta[15]. Creamos modelos crudos y ajustados por edad y sexo. Además, las variables sociodemográficas y clínicas se ajustaron por presión arterial de oxígeno/fracción inspirada de oxígeno al ingreso. Estas variables se incluyeron en los modelos ajustados ya que son potenciales variables confusoras[16]. Al crear los modelos se evaluó el supuesto de linealidad y para los modelos ajustados se evaluó la colinealidad, no hallándose problemas de multicolinealidad. Para todas las pruebas estadísticas se utilizó un nivel de significancia estadística de 0,05.
Resultados
Características al ingreso
Durante el periodo de estudio se hospitalizó a un total de 843 adultos con el diagnóstico de COVID-19 (confirmado o sospecha), de los cuales 30 no cumplieron con los criterios de inclusión y fueron retirados del estudio. Así, en el presente análisis se incluyeron un total de 813 pacientes. De estos, a 711 (87,5%) pacientes se les realizaron pruebas diagnósticas y 544 (66,9%) tuvieron COVID-19 confirmado. De los pacientes con casos confirmados, 192 fueron diagnosticados mediante RT-PCR y 352 por prueba rápida serológica (Figura 1).
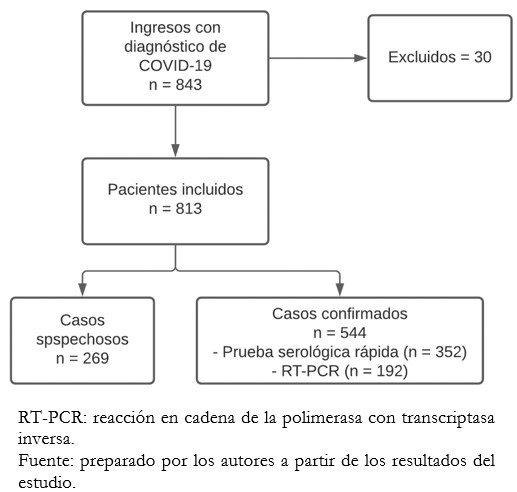 Tamaño completo
Tamaño completo La media de la edad fue de 61,2 años (desviación estándar: 15,0) y 573 (70,5%) fueron de sexo masculino. La comorbilidad más frecuente de los pacientes hospitalizados fue la hipertensión arterial con 34,1% (n = 277). En la Tabla 1 es posible apreciar otros resultados destacados de cada área.
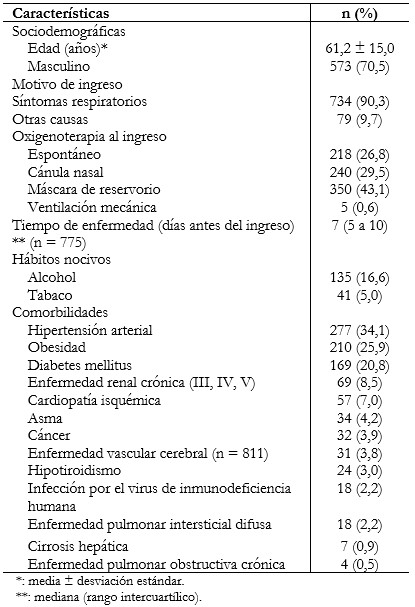 Tamaño completo
Tamaño completo Independientemente del motivo de ingreso, la mayoría de los pacientes arribó a la emergencia con sintomatología respiratoria (90,3%). La mediana de tiempo de enfermedad al ingreso fue de siete días antes del ingreso (rango intercuartílico: 5 a 10). Los síntomas más frecuentes fueron disnea (82,2%), tos (53,9%) y fiebre (51,2%) (Tabla 2).
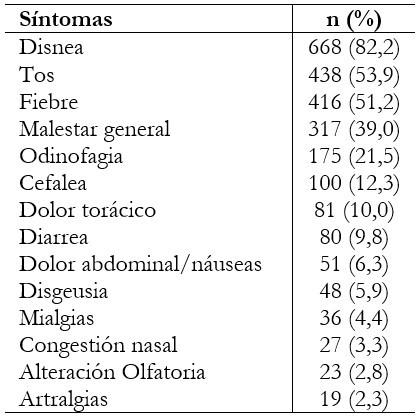 Tamaño completo
Tamaño completo Al momento del ingreso 374 (46,0%) de los pacientes había recibido alguna medicación previa como tratamiento para COVID-19. Así, 286 (35,2%) tomaron azitromicina, 148 (18,2%) ivermectina, 23 (2,8%) hidroxicloroquina y 119 (14,6%) tomaron combinaciones de estos, por una mediana de 4 días (rango intercuartílico: 2 a 5). Con respecto a antiagregantes plaquetarios y anticoagulantes, 24 (3,0%) tomaron aspirina, 38 (4,7%) utilizaron enoxaparina, 6 (0,7%) warfarina y 26 (3,2%) recibieron combinaciones de anticoagulantes, por una mediana de 3 días (rango intercuartílico: 2 a 5). Sobre el consumo de corticoides, 78 (9,6%) consumieron prednisona, 35 (4,3%) dexametasona y 53 (6,5%) alguna combinación durante una mediana fue de 4 días (rango intercuartílico: 3 a 5).
Al evaluar las funciones vitales, se registró que la mediana de frecuencia respiratoria fue de 24 respiraciones por minuto (rango intercuartílico: 22 a 28), la de frecuencia cardíaca fue 92 latidos por minuto (rango intercuartílico: 82 a 104), y la de presión arterial sistólica fue 100 milímetros de mercurio (rango intercuartílico: 100 a 120). La mayoría de los pacientes arribó con requerimiento de máscara de reservorio (43,1%) o cánula nasal (29,5%). La mediana de saturación de oxígeno al ingreso fue 89% (rango intercuartílico: 85 a 92%).
A todos los pacientes hospitalizados se les realizó alguna prueba de imágenes, siendo la tomografía la prueba realizada en 93,7% de los pacientes. Al evaluar el compromiso pulmonar utilizando la clasificación de CORADS se reportó que: 10 (2%) tuvieron imágenes no sugestivas (escala de CORADS 1 y 2), 17 (2,1%) indeterminado (escala de CORADS 3) y 779 (96,0%) un patrón sugestivo (escala de CORADS 4, 5 y 6). La media de porcentaje de parénquima pulmonar comprometido en la tomografía fue de 55,4% (desviación estándar: 18,7). En la Tabla 3 se presentan los exámenes de laboratorio al ingreso.
 Tamaño completo
Tamaño completo Manejo y evolución durante la hospitalización
Durante la hospitalización 462 (56,8%) pacientes recibieron azitromicina, 97 (11,9%) hidroxicloroquina, 168 (20,7%) ivermectina, 498 (61,3%) recibieron enoxaparina profiláctica, 172 (21,2%) enoxaparina terapéutica, 18 (2,2%) heparina no fraccionada, 200 (24,6%) recibieron dexametasona, 243 (29,9%) metilprednisolona en esquema de pulso (125 a 500 miligramos) y 233 (28,7%) a dosis inferiores. La mediana de días de tratamiento con corticoides fue de 3 (rango intercuartílico: 2 a 5).
A 143 (17,6%) de los pacientes se les realizó un electrocardiograma y se registró que 116 tuvieron un hallazgo normal o que se correlacionaba con sus antecedentes y 27 tuvieron un hallazgo nuevo, reportando en 18 pacientes una prolongación del intervalo QT. No se encontró asociación entre la administración de azitromicina e hidroxicloroquina hospitalaria y la prolongación del intervalo QT (valor p = 0,928 Chi-cuadrado y valor p = 0,121 prueba exacta de Fisher, respectivamente).
La mayoría de los pacientes (782 equivalente a 96,2%) recibió antibióticos durante la hospitalización. La frecuencia de antibióticos fue: 486 (59,8%) de los pacientes recibieron ceftriaxona, 118 (14,5%) piperacilina tazobactam, 64 (7,9%) meropenem, 64 (7,9%) vancomicina y 114 (14,0%) recibieron otro esquema antibiótico.
Durante la hospitalización, 215 (26,5%) pacientes en estudio presentaron neumonía intrahospitalaria, 151 (18,6%) tuvieron lesión renal aguda, 79 (9,7%) desarrollaron delirio, 17 (2,1%) tuvieron un proceso trombótico venoso y 20 pacientes presentaron otras complicaciones. La mediana del tiempo de enfermedad en el cual los pacientes aumentaban el requerimiento de oxígeno se presentó al día 10 (rango intercuartílico: 7 a 14).
Con respecto a los desenlaces de interés, 114 (14,0%) de los pacientes hospitalizados recibieron ventilación mecánica, 38 (4,7%) ingresaron a unidad de cuidados intensivos y 377 (46,4%) fallecieron. La mediana del tiempo de estancia en unidad de cuidados intensivos fue de 6 días (rango intercuartílico: 4 a 11) y la mediana del tiempo de estancia en el hospital fue de 10 días (rango intercuartílico: 6 a 17).
Factores asociados a mortalidad por COVID-19
En el análisis bivariado se encontró que la proporción del sexo masculino fue mayor en el grupo que falleció. Además, el grupo que falleció tuvo una mayor media de edad. Con respecto a las características al ingreso, se asociaron a mayor mortalidad el requerir soporte ventilatorio y el mayor compromiso pulmonar en la tomografía. No existió asociación entre el tiempo de enfermedad al ingreso y la mortalidad (valor p = 0,9087 Wilcoxon).
Asimismo, ciertas comorbilidades se asociaron a mortalidad como hipertensión arterial, cáncer, cardiopatía isquémica, enfermedad vascular cerebral e hipotiroidismo. Luego de ajustar por edad, sexo y presión arterial de oxígeno/fracción inspirada de oxígeno, esta asociación se pierde en todas las comorbilidades.
Diversos marcadores inflamatorios como proteína C reactiva, lactato deshidrogenasa, dímero D, ferritina, lactato, entre otros, se asociaron directamente con mortalidad (Tabla 4).
Al evaluar la asociación mediante modelos de regresión de Poisson, se detectó que por cada 10 años que aumentaba la edad, el riesgo de morir se incrementó en 32% (riesgo relativo: 1,32; intervalo de confianza 95%: 1,25 a 1,38). Esta asociación se mantuvo al ajustar por sexo y presión arterial de oxígeno/fracción inspirada de oxígeno al ingreso (riesgo relativo: 1,21; intervalo de confianza 95%: 1,15 a 1,28).
Además, aquellos que ingresaron a unidad de cuidados intensivos y ventilación mecánica, tuvieron 1,39 (intervalo de confianza 95%: 1,13 a 1,69) y 1,97 (intervalo de confianza 95%: 1,69 a 2,29) veces el riesgo de morir en comparación a los que no recibieron ese soporte, luego de ajustar por edad, sexo y presión arterial de oxígeno/fracción inspirada de oxígeno al ingreso (Tabla 4).
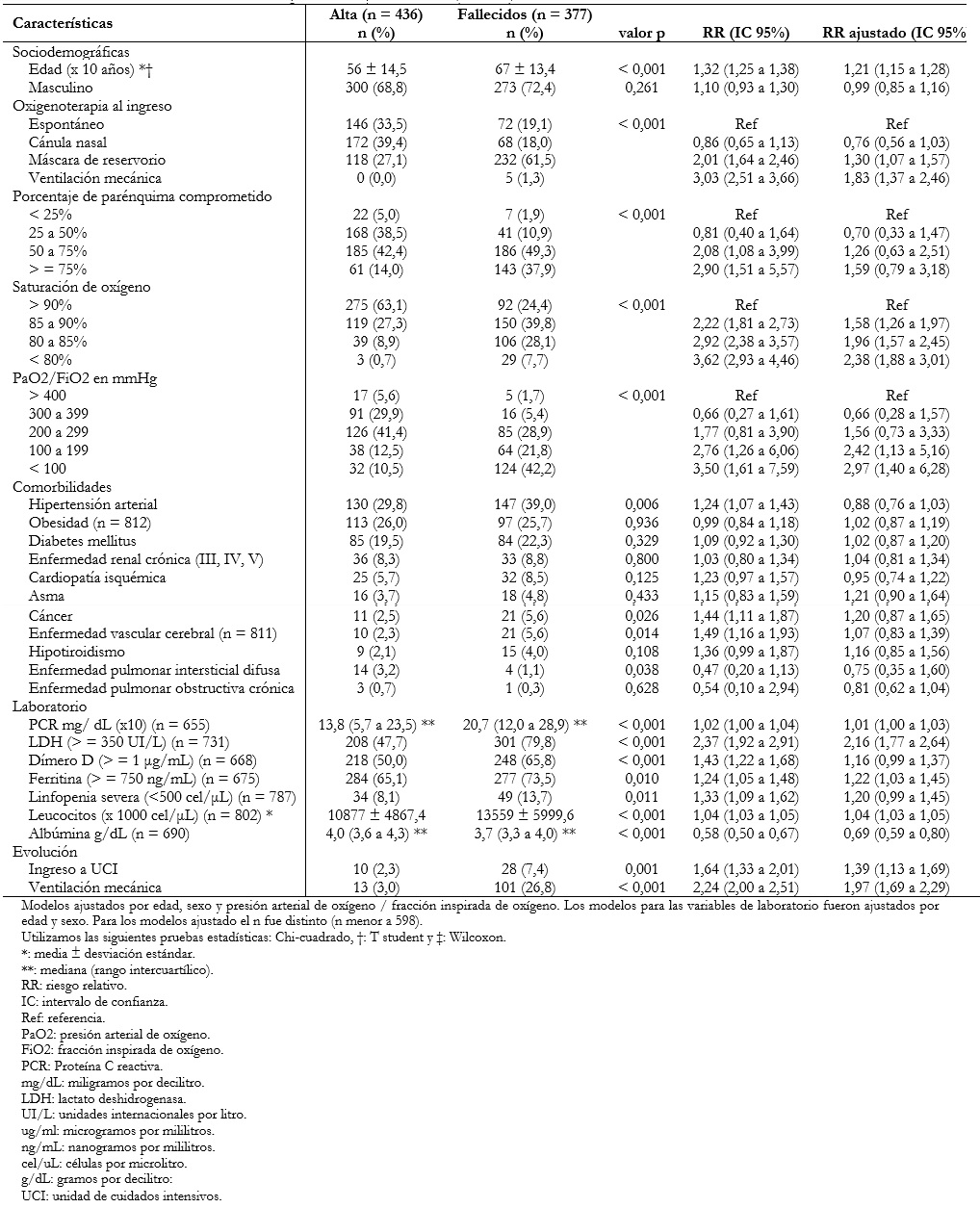 Tamaño completo
Tamaño completo Discusión
Este estudio de cohorte prospectivo se realizó con el objetivo de determinar los factores asociados a mortalidad de los pacientes adultos hospitalizados con el diagnostico de COVID-19 en un hospital de Perú. También buscó describir sus características clínicas, manejo y evolución. El número de pacientes enrolados en nuestro estudio a la fecha de redacción de este reporte es el más grande publicado a nivel nacional[17],[18]. Entre otros factores, esto se debe a la capacidad hospitalaria y a que el estudio se ejecutó durante el periodo de aumento de casos en la curva epidemiológica de pacientes diagnosticados con COVID-19, según lo reportado en la sala situacional del Ministerio de Salud[19].
En nuestro estudio se reportan características demográficas similares a las ya evidenciadas en las otras cohortes realizadas en Perú y el mundo[3],[17],[18], donde el sexo masculino presenta mayor porcentaje de hospitalizados y la media de tiempo de enfermedad es de 7 días al ingreso.
Respecto a las comorbilidades encontradas, la hipertensión arterial es la comorbilidad más frecuente seguida por diabetes y obesidad. Sin embargo, el porcentaje de obesidad descrito es bajo (25,9%) respecto a lo reportado en otros estudios (superiores al 40%) y no se encontró asociación con mayor mortalidad[17],[20]. Una explicación es el subregistro de medición del índice de masa corporal existente en las historias clínicas. La falta de personal y alta demanda de atención durante la pandemia dificultó la toma de las medidas antropométricas habituales en los pacientes hospitalizados. Esto podría explicar por qué, a diferencia de otros estudios, no encontramos una asociación entre obesidad y mortalidad.
En cuanto a los síntomas que se describieron con mayor frecuencia al ingreso fueron disnea, tos y fiebre, en contraste a lo descrito en un estudio de pacientes hospitalizados de China[21] y Reino Unido[5] donde se identificó a la fiebre como el síntoma más prevalente seguido por tos y disnea. La disnea como síntoma al ingreso más frecuente refleja que los pacientes acudieron al hospital de forma más tardía que en otros países.
La tomografía de tórax fue un método rápido de apoyo al diagnóstico en nuestro hospital debido a la falta de disponibilidad de pruebas diagnósticas[22]. Respecto a los resultados de laboratorio se evidenció leucocitosis en 62,12% de los pacientes, de los cuales 76,47% tenían linfopenia relativa con un valor por encima de lo encontrado en un estudio en China (40%)[4]. Por otro lado, en una cohorte en Estados Unidos describieron una media de proteína C reactiva de 8,35 miligramos por decilitro, asociado al resto de marcadores inflamatorios con un valor por debajo al presentado en nuestra población (17,1 miligramos por decilitro)[23]. Estos datos evidencian que la mayoría de nuestros pacientes acuden con una respuesta sistémica mayor.
En el periodo de estudio se observó que la hidroxicloroquina fue menos prescrita (11,9%) respecto a los estudios nacionales publicados. Además, existió un mayor uso de ivermectina (20,7%), esto debido a que desde el inicio de la pandemia el esquema terapéutico ha ido modificándose en las guías de manejo del Ministerio de Salud[24].
Respecto al uso de corticoterapia, más de la mitad de nuestros pacientes recibieron metilprednisolona, sin un esquema único de dosis y días de administración. La dexametasona se utilizó en la cuarta parte de nuestros pacientes. La prescripción de este corticoide se explica debido a que coincidió con el reporte preliminar de un estudio, donde se observó un beneficio en la reducción de la mortalidad a los 28 días en pacientes hospitalizados con requerimiento de ventilación mecánica o que requerían oxígeno[25]. El uso de corticoterapia en estos pacientes se debe a la respuesta inflamatoria sistémica observada en los pacientes con COVID-19. Sin embargo, datos actuales mencionan que el nivel de citoquinas circulantes es mucho menor que la observada en otras entidades como shock séptico, trauma múltiple o arresto cardiaco[26].
El uso de anticoagulación en esta enfermedad se ha justificado en múltiples reportes de eventos tromboembólicos en los pacientes hospitalizados con COVID-19, y a su potencial beneficio en el aumento de la sobrevida en los pacientes críticos. No obstante, también se reporta un número alto de eventos de sangrado mayor, por lo que la indicación debería de ser individualizada[27]. Más de la mitad de nuestros pacientes recibió algún tipo de esquema de anticoagulación y no se reportó ningún evento de sangrado mayor asociado a anticoagulación.
Con relación a las reacciones adversas a medicamentos, el perfil de seguridad de los medicamentos utilizados en nuestra cohorte (como la hidroxicloroquina sola o en combinación con azitromicina), describe el riesgo cardiológico de la prolongación del intervalo QT[28] que se incrementa con el uso concomitante de antibióticos, antiarrítmicos, anestésicos, relajantes musculares, entre otros. Además, se han reportado otros efectos adversos como toxicidad hepática, dolor abdominal, diarreas, náuseas y/o vómitos[29]. La evaluación de las reacciones adversas en el contexto de enfermedades nuevas como COVID-19 requiere de farmacovigilancia intensiva que no fue realizada en el presente estudio. Sin embargo, esta se está realizando por el Centro de Referencia Institucional de Farmacovigilancia y Tecnovigilancia del Seguro Social de Salud[30].
Respecto a las complicaciones intrahospitalarias, se observó que la reportada con más frecuencia fue la neumonía bacteriana en un 26,5%. Este dato contrasta con el porcentaje de pacientes que recibieron algún esquema antibiótico por sospecha de infección intrahospitalaria, que en la mayoría no se logró identificar un germen (36,4%). Una revisión sistemática consignó una baja prevalencia de coinfección bacteriana en pacientes hospitalizados con COVID-19, identificándose en 3,5 % al ingreso y en 15,5% durante hospitalización. Dicho estudio concluyó que el uso de tratamiento antibiótico empírico no está justificado en la mayoría de pacientes hospitalizados con COVID-19[31].Este es un aspecto que debemos tener presente, ya que la resistencia bacteriana podría ser uno de los principales problemas en el futuro cercano.
En nuestro estudio se reporta que solo 4,7% de nuestros pacientes ingresaron a unidad de cuidados intensivos y 14% recibieron soporte ventilatorio. Esto podría explicarse por la disponibilidad de ventilador mecánico en áreas que no corresponden a unidad de cuidados intensivos dentro del área de emergencia del hospital de estudio. Aun así, sólo el 14 % de nuestros pacientes recibió soporte de ventilación mecánica. Este reporte es similar a lo reportado en estudios nacionales (10,18% y 16,1%)[17],[18] e inferior a lo reportado en los estudios internacionales realizados en países de altos ingresos[3],[4],[5],[6]. La explicación a esto es que, debido al colapso de nuestro sistema sanitario, no todos los pacientes que requirieron ingreso a unidad de cuidados intensivos pudieron acceder a soporte ventilatorio.
La mortalidad encontrada es alta (46,4%) y muy superior a la reportado en las cohortes de New York (39%), Wuhan (28%) y Londres (29%)[3],[4],[5]. Este fenómeno puede atribuirse al estado crítico de ingreso, la falta de acceso a ventiladores, insuficientes camas de unidad de cuidados intensivos y por otros potenciales factores asociados a mortalidad que se han tratado de identificar en estudios previos[17],[18],[32].
Entre los factores asociados a mortalidad, se describe que hubo mayor proporción de fallecidos del sexo masculino (72,4%). Lo descrito coincide con una revisión sistemática que mostró un riesgo de mortalidad significativo para el sexo masculino respecto al femenino (riesgo relativo: 1,86)[16]. Un estudio de cohorte en China reportó un riesgo menor de muerte en el sexo femenino (Odds ratio: 0,44; intervalo de confianza 95%: 0,34 a 0,58) después de ajustar por edad y comorbilidades[33]. Sin embargo, al realizar el análisis ajustado no se encontró asociación. Una posible explicación es que la proporción entre ambos sexos es disímil entre los distintos grupos etarios, tal como lo planteado en el estudio de Bhopal SS y Bhopal R[34].
La edad se asoció a mayor mortalidad. En nuestra serie la mayor proporción de fallecidos correspondieron a los grupos etarios mayores de 60 años. Por cada 10 años que aumentaba la edad, el riesgo de morir se incrementó en 32%. Esto también fue descrito en una serie grande de datos poblacionales chinos en la cual los grupos etarios de 60 a 69, de 70 a 79 y mayores de 80 años tuvieron 3,6, 8 y 14,8% de mortalidad respectivamente[35].
El presente estudio encontró asociación entre la mortalidad y distintos marcados proinflamatorios (proteína C reactiva, ferritina, lactato deshidrogenasa, leucocitosis), los que pueden servir como biomarcadores tempranos de severidad en COVID-19[36]. Además, hallamos una asociación entre mortalidad y la hipoxemia al ingreso y con el requerimiento de oxigenoterapia, sobre todo en aquellos pacientes que necesitaron máscara de reservorio o ventilación mecánica. Esto se evidencia en una cohorte retrospectiva en la que 68% de pacientes con valores de saturación periférica de oxígeno de 90% o menos, no sobrevivieron después de la suplementación con oxígeno. En tanto, 98% de aquellos pacientes con valores de saturación parcial de oxígeno superiores al 90% sí sobrevivieron (log-rank P < 0,001)[37].
La saturación parcial de oxígeno al ingreso también fue un predictor de mortalidad. En nuestra serie aquellos pacientes que ingresaron con saturación parcial de oxígeno inferior a 80% tuvieron mayor mortalidad que aquellos que entraron con mayor a 90%. En otros estudios no se describen saturaciones parciales de oxígeno tan bajas al ingreso, lo cual podría ser explicado por el retraso de los pacientes en acudir al servicio de emergencia y el colapso de este servicio con altas demoras en la atención[38].
Es importante realizar estudios adicionales en nuestra región que concentren mayor cantidad de pacientes y analicen los factores asociados a mortalidad en COVID-19. Con esos resultados es posible realizar una reorganización del sistema de atención de salud, direccionando un manejo diferenciado en los pacientes con mayores factores de riesgo de mortalidad. El establecimiento de estas medidas es fundamental en las regiones de Latinoamérica donde aún hay baja cobertura de los programas de vacunación, producto de la escasez de este medio de prevención.
Nuestro estudio tiene diversas fortalezas. Este se realizó en el hospital referencial de atención de pacientes con COVID-19 que cuenta con la mayor capacidad hospitalaria de la seguridad social de Perú. Asimismo, se efectuó un registro sistemático con los datos de los pacientes desde su ingreso a emergencia hasta su destino final, mediante el sistema electrónico de historia clínica. Dicho sistema contiene el registro de los datos clínicos, exámenes de laboratorio e imagenológicos realizados. Sin embargo, tiene ciertas limitaciones ya que al ser un estudio en que los datos se obtuvieron del sistema electrónico, existió un registro incompleto de algunas variables (reacciones adversas a medicamentos, hábitos nocivos e índice de masa corporal) que podrían afectar la validez externa de los resultados obtenidos respecto de ellas.
Conclusión
Se reporta la serie más grande de pacientes hospitalizados con COVID-19 en Perú. La población evaluada presentó una alta mortalidad (46,4%), lo que difiere a lo reportado previamente en países desarrollados.
La mortalidad se asoció a la edad (mayores de 60 años), a marcadores inflamatorios y al compromiso respiratorio.
Por último, es necesaria una reorganización del sistema de atención hospitalario direccionando un manejo diferenciado en los pacientes con mayores factores de riesgo de mortalidad.

