Acta de reunión clínica
← vista completaPublicado el 1 de diciembre de 2008 | http://doi.org/10.5867/medwave.2008.11.3659
Nutrición en parálisis cerebral infantil
Nutrition in cerebral palsy
Resumen
Este texto completo es la transcripción editada y revisada de una conferencia dictada en el marco de las reuniones clínicas del Servicio de Pediatría del Complejo de Salud San Borja-Arriarán. La publicación de estas actas científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Servicio de Pediatría. El jefe de Servicio es el Dr. Francisco Barrera y el Coordinador de las Reuniones Clínicas es el Dr. Luis Delpiano.
Problemas nutricionales en la parálisis cerebral
La parálisis cerebral (PC) es una patología compleja, que se puede presentar de diferentes formas y con grados variables de compromiso. Los pacientes con daño neurológico ocupan, en algunas épocas del año, alrededor de 30% de las camas en el Servicio de Pediatría del Hospital San Borja Arriarán; su promedio de días de hospitalización es mayor que el de los niños sin daño neurológico, de hecho algunos de estos pacientes prácticamente viven en el hospital, y sus hospitalizaciones suelen ser más costosas debido a que con frecuencia requieren fármacos o estudios de laboratorio e imágenes de mayor complejidad, fórmulas lácteas especiales, bombas de infusión, cuidados de enfermería y kinesiterapias respiratorias o motoras. La mejoría del estado nutricional de los pacientes portadores de PC permite reducir la frecuencia de hospitalizaciones e infecciones y mejorar su calidad de vida y la de sus familias o cuidadores.
Los problemas nutricionales que los niños con PC presentan son:
- desnutrición;
- falla en el crecimiento (longitud);
- sobrepeso u obesidad;
- deficiencia de micronutrientes, sea por ingesta insuficiente y/o por alguna interacción entre fármacos y nutrientes que impide un metabolismo adecuado;
- osteopenia y osteoporosis;
- dificultad para realizar una evaluación nutricional adecuada, tanto para efectuar el diagnóstico como en el seguimiento.
Existe una serie de factores que favorecen el desarrollo de alteraciones nutricionales en los niños con PC, entre ellos: alteraciones motoras gruesas y finas; trastornos de la deglución y disfunción motora oral; reflujo gastroesofágico, que causa aspiraciones, infecciones respiratorias secundarias e ingesta alimentaria insuficiente debido a la hiperemesis; falta de deambulación; dependencia de cuidadores, que no siempre son adecuados; alteraciones sensoriales; deformaciones óseas de columna y tórax que dificultan el drenaje de las secreciones bronquiales, la administración de los alimentos y el cuidado de las escaras; tiempo de evolución: a mayor tiempo de evolución del compromiso neurológico, mayor es el compromiso nutricional; ingesta alimentaria, que muchas veces es insuficiente debido a los trastornos mencionados; uso de sondas de alimentación o gastrostomías; uso de fármacos, en especial los anticonvulsivantes, que tienen un efecto deletéreo sobre la densidad ósea; capacitación en cuidados de enfermería en el hospital, en las instituciones o en el hogar; y finalmente está el factor costo, ya que muchas veces el cuidador debe renunciar a su trabajo para cuidar al niño.
En un estudio que se efectuó para evaluar las dificultades de alimentación de un grupo de niños con PC que tenían falla en el crecimiento, tanto en longitud como en ganancia de peso y déficit en la calidad de vida, los autores efectuaron antropometría y clasificaron las dificultades para la alimentación según la presencia de disfunciones de deglución, alteraciones motoras, alteraciones posturales, daño neurológico, disminución marcada de la actividad, presencia de constipación y grado de retardo del vaciamiento gástrico. También aplicaron una encuesta de calidad de vida de los cuidadores (1). En este estudio se observó que el aumento de las dificultades para alimentar a estos niños se asocia a mayor alteración del crecimiento lineal y de la ganancia de peso, menor reserva grasa, medida por pliegues tricipitales, mayor cantidad de hospitalizaciones, mayor frecuencia de infecciones respiratorias y peor calidad de vida de los cuidadores (Fig. 1).
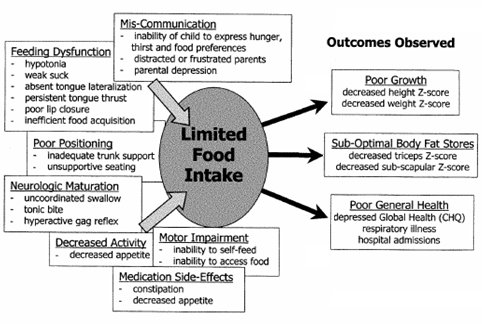 Tamaño completo
Tamaño completo El objetivo del manejo nutricional en los niños con PC es lograr un estado nutricional adecuado, que permita mantener las siguientes funciones: cardiorrespiratoria, mediante el tono adecuado de las musculaturas diafragmática y cardiaca; inmunológica, para control de las infecciones; motoras y cognitivas, a través de un adecuado funcionamiento del sistema neurológico; cicatrización y reparación tisular, de modo de evitar escaras o permitir que se resuelvan rápidamente. Estos objetivos se logran si se mantiene la curva de peso para la talla (P/T) en el percentil 10 (p10) del sistema NCHS, en los casos de PC grave.
Evaluación nutricional en el niño con PC
La evaluación nutricional del niño con PC incluye:
- Anamnesis remota y actual, de la que se puede deducir el tiempo de evolución.
- Evaluación de la curva de crecimiento.
- Observar el acto de la alimentación y las dificultades que surgen durante éste: grado de autovalencia, trastornos motores, deglución, presencia de reflujo, postura, escoliosis, duración, tos, etc.
- Evaluar la ingesta.
- Precisar el uso de fármacos y obtener la descripción de la red de apoyo familiar-social.
En el examen físico se debe evaluar la actividad motora y tono muscular. Finalmente, se debe realizar la antropometría, considerando que puede ser difícil pesar a estos niños, puesto que muchas veces no se pueden poner de pie y no siempre se cuenta con sillas de evaluación antropométrica; además del peso se debe medir la longitud o talla; el perímetro cefálico, aunque no es un buen parámetro para el seguimiento; la circunferencia braquial y los pliegues, de los cuales el pliegue tricipital es el más representativo de la composición corporal.
Los niños con PC poseen un patrón de crecimiento distinto al de los niños normales debido a que tienen distinta composición corporal, con disminución de la densidad ósea, la masa muscular, la masa grasa y el crecimiento lineal y patrones de desarrollo puberal y de edad ósea diferentes. En 2007 se publicaron tablas para evaluar el crecimiento de niños y adolescentes con PC, con base en estudios multicéntricos en los que se incluyó a 24.920 niños y adolescentes de 2 a 20 años de edad en quienes se realizaron 141.961 mediciones de peso y talla (2). Los autores clasificaron a los pacientes con PC en cinco grupos, de acuerdo con las habilidades motoras gruesas:
- Grupo 1: camina solo, mínimo seis metros y se balancea bien.
- Grupo 2: camina con apoyo o inestable por un mínimo de tres metros.
- Grupo 3: gatea o se arrastra, pero no camina.
- Grupo 4: postración, no se puede alimentar por sí mismo, pero no posee gastrostomía.
- Grupo 5: características motoras del grupo 4, pero se alimenta por gastrostomía. El hecho de poseer gastrostomía mejora el estado nutricional y por lo tanto, el crecimiento lineal.
En la Fig. 2 se muestran las tablas mencionadas. La de la izquierda corresponde a la relación peso/edad en mujeres; la línea continua corresponde a ciertos niños con PC y la que está punteada es la del NCHS. Se puede ver que el percentil 10 difiere, no así el percentil 90, en el que ambas curvas son similares, debido a que estos niños ya son capaces de caminar. La tabla de la derecha corresponde al grupo 5, es decir, niños postrados que se alimentan por gastrostomía; la línea punteada corresponde a la del NCHS y la línea continua a la nueva. Se observa que el percentil 10 de la línea NCHS corresponde al percentil 90 de la nueva curva, es decir, el tipo de crecimiento que ellos logran es muy diferente, tanto en peso/edad como talla/edad (2, 3). En el grupo 4, que no usan gastrostomía y que no aparece en este gráfico, la curva es aún menor (Fig. 2).
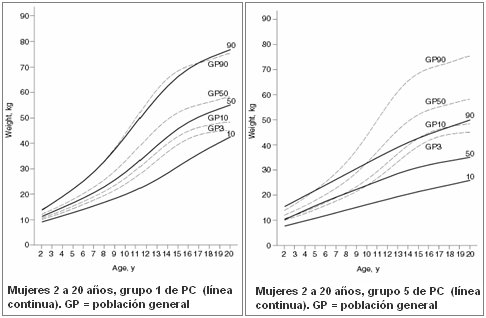 Tamaño completo
Tamaño completo Los niños portadores de PC con frecuencia presentan rigidez e hipertonía, por lo tanto hay que medirlos por segmentos y comparar las mediciones con las tablas en uso actualmente, que se publicaron en 1995 y se confeccionaron con base en un grupo pequeño de 170 niños y solamente 211 mediciones de la longitud de la tibia, la que permite obtener la longitud total mediante una fórmula (4). Lamentablemente estas tablas sirven sólo hasta los 12 años de edad (Fig. 3).
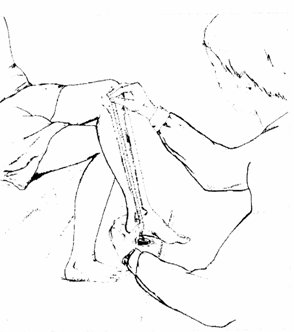 Tamaño completo
Tamaño completo Existen varios métodos para identificar la desnutrición en los niños con PC. Fang y colaboradores, en un estudio que se cita con mucha frecuencia, definieron la desnutrición como el hecho de tener un porcentaje de área grasa humeral menor de 5% para la edad y sexo en las tablas de niños sin daño neurológico (5). Ellos midieron peso, talla y pliegues y concluyeron que el pliegue tricipital bajo p10 es mejor herramienta de screening que la relación P/T, debido a su alta sensibilidad, para evaluar la desnutrición definida como bajo p5 en área grasa del perímetro braquial según sexo y edad (reserva grasa disminuida), en niños con PC (Tabla I).
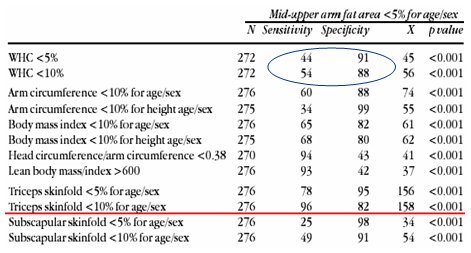 Tamaño completo
Tamaño completo
Laboratorio en la evaluación nutricional
Los parámetros de laboratorio útiles para la evaluación nutricional incluyen:
- serie roja para descartar anemia
- albuminemia
- nitrógeno ureico, que puede estar en niveles bajos debido a disminución de la ingesta o de la masa muscular
- fosfemia, fosfatasas alcalinas, vitamina D y densitometría ósea para evaluar la masa ósea
- videofluoroscopía para estudio de la deglución
- pHmetría de 24 horas para estudio del reflujo
- oximetría durante la alimentación y
- creatininuria de 24 horas, que sirve como indicador de masa muscular y reserva proteica.
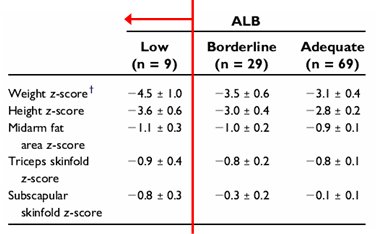
En un trabajo en el que se midió prealbuminemia y albuminemia en 107 niños con PC de grado moderado a grave, con el objetivo de evaluar el grado de desnutrición en función de la albuminemia, se encontró que la mayoría de los pacientes tenían niveles de albúmina mayores de 3,5 a 3,9 e incluso, mayores de 4 g/dl, a pesar de tener -4 desviaciones estándares en la relación P/E; solamente 8% tenía niveles de albúmina menores de 3,5 (6). Por lo tanto, los niveles de albúmina plasmática no reflejan el estado nutricional en los niños con PC (Tabla II).
 Tamaño completo
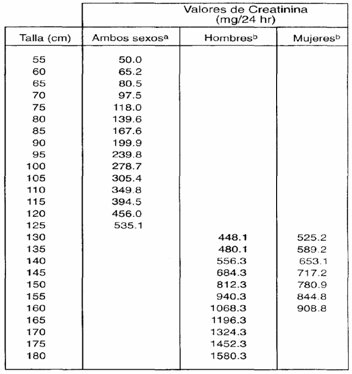
Tamaño completo En 1981 se publicaron tablas que correlacionan la creatininuria de 24 horas con la talla, pero se basaron en personas sin daño neurológico (7). Como la creatinina es una proteína muscular, para evaluar la cantidad de masa muscular del niño se puede calcular el porcentaje de lo normal de la creatinina que excreta cada paciente. No se encuentra en la literatura la descripción de valores normales para niños con PC (Tabla III).
 Tamaño completo
Tamaño completo
Manejo nutricional del niño con PC
Los requerimientos energéticos se pueden calcular mediante distintas fórmulas, lo importante es que después se realice un seguimiento del peso y la talla para evaluar si el aporte es adecuado; el objetivo es lograr P/T en el percentil 10 del NCHS. El aporte de proteínas se debe hacer siguiendo las recomendaciones para niños normales, al igual que el aporte de minerales y vitaminas. Se ha observado que aun cuando se entregue un suplemento a los niños con PC, de todos modos presentan deficiencia de hierro, folato, niacina, calcio y vitamina E y D y que el aporte enteral mejora los niveles plasmáticos de estos micronutrientes (8).
El requerimiento de energía se calcula mediante una ecuación que entrega la energía total multiplicando el gasto energético basal por el tono muscular y por el grado de actividad, a lo que se suma el crecimiento normal esperado. Al tono muscular se le asigna valor 1 si es normal, 0,9 si tiene hipotonía y 1,1 si el niño está hipertónico (9). El requerimiento de energía suele ser mucho menor de lo normal debido a que estos pacientes tienen alteración de la composición corporal y de la curva de crecimiento y su actividad es mucho menor que la de un niño sano.
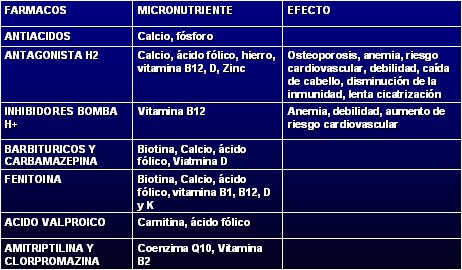
En la Tabla IV se observan las interacciones entre fármacos y metabolismo de micronutrientes: los antiácidos, antagonistas H2, inhibidores de la bomba de protones y anticonvulsivantes interfieren con este metabolismo, de ahí que los pacientes que usan fenitoína o fenobarbital deben recibir suplementos de vitamina D y los que se tratan con ácido valproico, de carnitina.
 Tamaño completo
Tamaño completo La administración de la alimentación, en los niños con PC, se puede efectuar por vía oral, lo que muchas madres logran cambiando la consistencia de los alimentos. La alternativa es la vía enteral, mediante sonda naosgástrica o nasoyeyunal o mediante gastrostomía; puede ser en bolos o continua (total o nocturna) y se puede requerir el agregado de fármacos para tratar el reflujo y/o la constipación.
En los pacientes con patología neurológica, se debe considerar la nutrición enteral frente a uno o más de los siguientes factores: incapacidad para ingerir por boca el 80% de su requerimiento; tiempo total de alimentación mayor de cuatro horas al día; paciente menor de dos años con crecimiento o ganancia de peso insuficientes por más de un mes; paciente mayor de dos años con pérdida de peso o ausencia de ganancia de peso por un período de tres meses; cambio en dos canales de crecimiento en curvas (P/E o P/T), o pliegue tricipital menor de p5 en forma persistente. Si estas situaciones se mantienen por más de un mes se debe considerar gastrostomía.
El metabolismo óseo de los niños con PC se caracteriza por alta prevalencia de osteopenia, que se asocia al grado de desnutrición, de hecho, el factor más predictivo de osteopenia es el compromiso marcado de la curva P/E. Otros factores que favorecen este fenómeno son: la edad (a mayor edad, menor densidad ósea), la gravedad del daño neurológico, la dificultad para alimentarse, el antecedente de fractura previa y el uso de anticonvulsivantes, que causan osteopenia por múltiples mecanismos: alteraciones en el metabolismo del calcio, hipofosfatemia, fosfatasas alcalinas elevadas, PTH elevada, disminución de los niveles de vitamina D activa, evidencias radiológicas de raquitismo y evidencias histológicas de osteomalacia (10).
Conclusiones
- La PC es una enfermedad compleja, por lo tanto debe ser manejada por un equipo multidisciplinario que incluya un especialista en nutrición.
- El tipo y vía de alimentación dependerá de las habilidades motoras, dificultades para alimentarse y de si el paciente se atiende en forma ambulatorio o está institucionalizado.
- Se debe contar con un equipo multidisciplinario organizado, coordinado y algunos recursos específicos, como pesas, silla, gastrostomías, visitas domiciliarias.
- La PC es motivo de continua investigación sobre aspectos que aún falta aclarar, como la mejor forma de determinar la composición corporal y los requerimientos de micronutrientes.
- La actividad física (movimiento) es parte importante de la terapia, ya que se ha demostrado que mejora el crecimiento lineal y la densidad ósea.
- La nutrición puede ser el foco de un dilema ético en aquellos casos en que es la única terapia que sostiene la vida del paciente. En esta situación, la indicación de apoyo nutricional debe ser discutida por el equipo tratante, la familia o cuidadores y la comunidad.

