Consenso
← vista completaPublicado el 1 de enero de 2010 | http://doi.org/10.5867/medwave.2010.01.4358
Revisión de la literatura sobre alto riesgo de cáncer de mama y estrategias de prevención
High-risk for breast cancer and prevention strategies: a literature review
Contenidos
Introducción
Objetivos Específicos
Metodología y Resultados de la Búsqueda de la Literatura
Síntesis de la Evidencia y Recomendaciones
1. Identificación de Mujeres de Alto Riesgo
1.1 ¿Cuáles son y Cómo se Clasifican los Factores de Riesgo de Cáncer de Mama según su Magnitud?
1.2 ¿Cuáles son las Lesiones Histopatológicas de Alto Riesgo y de qué Magnitud es el Riesgo Asociado a Ellas?
1.3 ¿Cuáles son las Diferencias entre Riesgo de Cáncer Familiar y Riesgo de Cáncer Hereditario?
2. Objetivando el Riesgo de Cáncer de Mama
2.1 ¿Cuáles son los Modelos Matemáticos que han Demostrado Utilidad en la Cuantificación del Riesgo de Cáncer de Mama y que Parámetros Utilizan?
2.2 ¿Cómo Seleccionar a las Mujeres que Necesitan un Estudio del Riesgo Genético de Cáncer de Mama?
2.3 ¿Qué Debe Analizar el Estudio Genético?
2.4 ¿Cómo se Clasifican las Mujeres según el Nivel de Riesgo de Cáncer de Mama después de la Aplicación de los Distintos Modelos Matemáticos y Estudios Genéticos?
3. Estrategias de Vigilancia y Seguimiento
3.1 ¿Cuál es el Valor del Auto-Examen y Examen Clínico en el Seguimiento de Mujeres de Alto Riesgo?
3.2 ¿Con qué Frecuencia se Debe Realizar el Estudio de Imágenes (Mamografía y Ecotomografía) en el Seguimiento de Mujeres de Alto Riesgo de Cáncer de Mama?
3.3 ¿Qué Tipo de Mamografía Debe Utilizarse: Convencional o Digital?
3.4 ¿Cuál es la Utilidad de la Resonancia Magnética Mamaria (RM) en la Vigilancia de Mujeres de Alto Riesgo?
3.5 ¿Cuál es la Utilidad de las Muestras de Epitelio Mamario (Lavado Ductal, Ductoscopía) en la Vigilancia de Mujeres de Alto Riesgo?
4. Estrategias de Prevención de Cáncer de Mama
4.1 Cambios de Estilo de Vida: ¿Cuáles han Demostrado Utilidad en la Prevención del Cáncer de Mama?
4.2 Métodos de Quimioprevención. ¿A Quiénes Pueden Beneficiar, Cuándo y por Cuánto Tiempo?
4.3 Cirugías Profilácticas: (Mastectomía-Ooforectomia), a Quienes Puede Beneficiar? Cuándo Debiesen Indicarse?
Referencias
Introducción
Hasta hace poco tiempo atrás, los esfuerzos médicos se concentraban en el diagnóstico precoz y tratamiento oportuno del cáncer de mama. La incorporación de programas de pesquisa precoz o “screening” o “tamizaje” por mamografía ha permitido diagnosticar tumores cada vez más pequeños, lo que ha permitido una disminución en aproximadamente 30% de la mortalidad por cáncer de mama en mujeres mayores de 50 años. En la actualidad se han identificado diferentes factores de riesgo que están presentes en mujeres sanas que las hacen aumentar en distinto grado su probabilidad de desarrollar un cáncer mamario en el futuro. La ventaja de conocer estos factores, es que permite distinguir diferentes grupos de mujeres de mayor riesgo de cáncer mamario, lo que contribuye a elaborar estrategias de vigilancia en el tiempo de estas mujeres, como también permite establecer estrategias para disminuir el riesgo aumentado y de esta forma, prevenir el desarrollo de un cáncer de mama. El manejo clínico racional de mujeres de alto riesgo constituye un desafío que deberá incorporarse en todos los centros de diagnóstico y tratamiento de cáncer de mama.
Objetivos Específicos
- Conocer y clasificar los diferentes factores de riesgo de cáncer de mama para identificar a las mujeres de alto riesgo y agruparlas según el nivel de riesgo
- De las mujeres con alto riesgo por historia familiar de cáncer de mama, conocer las estrategias para seleccionar aquellas que requieran estudio genético por sospecha de riesgo hereditario
- Establecer protocolos de vigilancia a mujeres de riesgo que dependerán del nivel de riesgo
- Establecer diferentes estrategias de prevención de cáncer de mama y su aplicación según el nivel de riesgo
Metodología y Resultados de la Búsqueda de la Literatura
Revisión de la literatura relevante de mayor impacto. Se incluyeron estudios prospectivos aleatorizados, estudios de cohorte, ensayos de distribución aleatoria, revisiones sistemáticas, revisiones narrativas, metanálisis, estudios descriptivos de corte transversal, estudios de casos y controles y series de casos prospectivas.
Síntesis de la Evidencia y Recomendaciones
1. Identificación de mujeres de alto riesgo
1.1 ¿Cuáles son y cómo se clasifican los factores de riesgo de cáncer de mama según su magnitud?
Síntesis de la evidencia:
Riesgo es un término relativo derivado de la comparación de la incidencia de una enfermedad en un grupo de personas que tienen un factor de riesgo particular, con relación a otro grupo de iguales características pero que no tienen dicho factor de riesgo. En este documento, factor de riesgo se considera a cualquier variable que aumente el riesgo de cáncer de mama a individuos. Se revisaron la mayoría de los factores importantes de riesgo y su contribución a la probabilidad de desarrollar cáncer de mama.
Estudios observacionales han permitido identificar estos factores y estimar la magnitud del riesgo asociado a ellos. Se han clasificado en factores de riesgo mayores aquellos que aumentan en 2 o más veces el riesgo y factores de riesgo menores los que aumentan en menos de 2 veces el riesgo (Schwartz, 2007; Gomez, 2006; Worsham, 2007; Vogel, 2003; Peralta, 2006; Fournier, 2005; Parvin, 2009; Zuzuki, 2005; Begum, 2009; Chlebowski, 2006; Hartmann, 2005; Li, 2007; Travis, 2005).
Se han establecido los riesgos absolutos y relativos para la mayoría de los factores de riesgo mayores; sin embargo, para los factores de riesgo menores, los riesgos relativos son estimativos, especialmente cuando se asocian a factores mayores. Como ejemplo, si una mujer es de alto riesgo por ser portador de mutaciones genéticas o de hiperplasia atípica (factores mayores), conocer la edad de la menarquia o la edad del primer parto agrega poca información adicional.
Nivel de evidencia II
Factores de Riesgo Mayores:
- Portadores de mutaciones de alta penetrancia en los genes BRCA1 y BRCA2. Además de otras mutaciones en otros genes, aún desconocidos.
- Historia familiar. Familiares de 1° o 2º grado con cáncer de mama bilateral, cáncer mamario antes de los 50 años sin mutaciones demostradas, familiares con cáncer de mama en dos generaciones, cáncer de mama y ovario. Familiar varón con cáncer de mama. Se recomienda investigar la historia familiar de cáncer en tres generaciones sucesivas.
- Radioterapia de tórax antes de los 30 años de edad por cáncer, usualmente de origen linfático.
- Antecedentes de lesiones histológicas precursoras: hiperplasias atípicas, neoplasia lobulillar in situ, atipia plana.
- Antecedente personal de cáncer de mama. En mujeres mayores de 40 años con antecedente personal de cáncer de mama, el riesgo relativo de un nuevo cáncer fluctúa entre 1,7 y 4,5. Si la mujer es menor de 40 años el riesgo relativo se eleva a 8,0
- Densidad mamográfica aumentada (controvertido). El aumento de la densidad mamográfica mamaria ha sido identificada como factor de riesgo de cáncer de mama en diferentes publicaciones. Sin embargo, existe controversia con relación a la cuantificación del riesgo según la magnitud de la densidad. Existe necesidad de ensayos clínicos prospectivos para definir el grado de riesgo de cáncer de mama según el tipo o extensión del aumento de densidad mamográfica (Schwartz, 2007).
Factores de Riesgo Menores:
- Edad. Como factor aislado es muy importante en el riesgo de cáncer de mama. A mayor edad, mayor riesgo. La incidencia de cáncer de mama a los 80-85 años es 15 veces más alta que a los 30-35 años (Vogel, 2003). En estudios de prevención se considera alto riesgo a partir de los 60 años (Peralta, 2006; Fisher, 2005).
- Historia familiar en parientes de 1º, 2° o 3° grado, después de los 60 años de edad.
- Factores reproductivos. 1- Menarquia precoz y menopausia tardía. Ello conlleva a una mayor exposición a ciclos menstruales durante la vida de la mujer lo que aumenta en alrededor de 30% el riesgo de cáncer de mama. Por la misma razón, la ooforectomía bilateral antes de los 40 años disminuye el riesgo en aproximadamente 50%. 2- Nuliparidad y 1º parto después de los 30 años se asocia con aumento del riesgo en un tercio (Vogel, 2003).
- Enfermedades mamarias benignas proliferativas. Adenosis esclerosante, lesiones esclerosantes radiales y complejas (cicatriz radiada), hiperplasia epitelial ductal florida, lesiones papilares y fibroadenomas complejos.
- Sobrepeso después de la menopausia. Existe relación entre Índice Masa Corporal (IMC) elevado y riesgo de cáncer de mama en mujeres postmenopáusicas. El riesgo relativo es 1,26 con IMC sobre 21.
- Ingesta crónica de alcohol. La ingesta de alcohol produce un aumento de 7% de riesgo de cáncer de mama por cada 10 grs. de alcohol adicional consumido diariamente (McTiernan, 2003). El consumo de alcohol se asocia a mayor riesgo de desarrollar tumores RE (+). Una ingesta mayor o igual a 10 gr/dia representa un RR=1,35, 95% CI 1,02 – 1,80, p<0,049 para tumores RE +RP+; y RR 2,96, 95% CI=1,56-3,56, p<0,001 para tumores RE+RP- (Suzuki, 2005).
- Algunas terapias de reemplazo hormonal en la menopausia. El aumento del riesgo de cáncer de mama con el uso de terapias de reemplazo hormonal ha variado en el transcurso de los últimos años de acuerdo a los diferentes preparados estudiados. El riesgo relativo oscila entre 0,7 y 2,0 dependiendo del estudio y de las formulaciones empleadas. Resumiendo la bibliografía revisada se puede concluir que el aumento del riesgo de cáncer de mama con tratamiento de estrógenos solos es mínimo o ninguno. El mayor riesgo observado con terapias de reemplazo hormonal combinadas, es de responsabilidad de ciertas progestinas (Peralta, 2006).
Recomendaciones:
- Es necesario conocer los factores de riesgo mayores y menores para la identificación de mujeres de alto riesgo de cáncer de mama y de familias con predisposición genética a la enfermedad.
- Conociendo el nivel de riesgo de cada mujer, es posible planificar estrategias de vigilancia y prevención.
1.2 ¿Cuáles son las lesiones histopatológicas de alto riesgo y de qué magnitud es el riesgo asociado a ellas?
Síntesis de la evidencia:
Esta pregunta se analiza desde dos puntos de vista diferentes:
A- Lesiones histopatológicas de alto riesgo de desarrollar un cáncer de mama en el futuro (lesiones precursoras).
B- Lesiones histopatológicas de alto riesgo en cáncer de mama recientemente diagnosticado.
Este punto se discutirá en el artículo de Diagnóstico Patológico.
La evidencia en ambos casos deriva fundamentalmente de estudios observacionales (principalmente cohortes retrospectivas), estudios transversales y series de casos.
Nivel de evidencia II-III
A- Lesiones histopatológicas de alto riesgo de desarrollar cáncer de mama en el futuro (lesiones precursoras)
La clasificación patológica de lesiones benignas de la mama incluye entidades que representan un leve riesgo de subdiagnóstico o de desarrollo de cáncer de mama (RR: 1,2-2,0). Ellas son la adenosis esclerosante, lesiones esclerosantes radiales y complejas (cicatriz radiada) y fibroadenomas complejos.
Lesiones precursoras son aquellas lesiones proliferativas benignas que presenta relación demostrada con riesgo aumentado de desarrollo posterior de carcinoma. Según la Organización Mundial de la Salud se aceptan como precursoras, la neoplasia lobulillar in situ, las lesiones proliferativas intraductales, hiperplasia ductal atípica, atipia plana, el carcinoma microinvasor y a las neoplasias papilares intraductales.
Neoplasia lobulillar in situ (NLIS): se considera como marcador pronóstico de baja frecuencia (0,5 a 3,9%; 1,2% en la serie de Liberman) porque en forma pura rara vez se encuentra asociado a carcinoma invasor (Jacobs, 2002). Es considerada un marcador de riesgo con una frecuencia de multicentricidad de 85% y bilateralidad de 35% (Zagouri, 2007). Carece de clínica o imagenología característica siendo su hallazgo incidental en el estudio histológico de otras lesiones. Para el carcinoma lobulillar in situ se acepta un riesgo relativo (RR) de 5 a 10 (Ben-David, 2005; Zagouri, 2007). Sólo la variante pleomórfica se asemeja fenotípica y genotípicamente al carcinoma ductal in situ de alto grado (Honrado, 2005). Los estudios revisados describen una incidencia de carcinoma de 10-31% después de una biopsia escisional. (Liberman, 1999; Shin, 2002; Middleton, 2003; Dershaw, 2003; Arpino, 2004; Elsheikh, 2005; Anderson, 2006; Karabakhtsian, 2007).
Clasificación Neoplasias Lobulillares (WHO, 2003):
- NL grado 1: Hiperplasia lobulillar atípica
- NL grado 2: Carcinoma lobulillar in situ clásico (CLIS)
- NL grado 3: Carcinoma lobulillar in situ pleomórfico y/o con sobredistensión
Hiperplasia ductal atípica (HDA): se define como una lesión proliferativa intraductal en que coexisten patrones de hiperplasia ductal usual y carcinoma ductal in situ de bajo grado. El criterio cuantitativo aplicado como límite superior corresponde a un tamaño ≤ 2 milímetros y tiene un RR = 4 - 5; hasta RR 9,7 si se asocia a historia familiar. Frecuentemente está asociada a carcinomas de bajo grado (Jacobs, 2003).
Atipia plana (AP): se define como una lesión intraductal de 1 a 5 capas de células levemente atípicas, cuboidales o columnares, micropapilares sin eje conectivo y con distensión variable de la unidad túbulo lobulillar. Su RR no está aún bien establecido y se asume 4 veces mayor (WHO, 2003). Se considera más un precursor de carcinoma ductal in situ (CDIS) de bajo grado, así como de neoplasia lobulillar y carcinoma tubular, por lo tanto no se ha asociado claramente a cánceres de alto riesgo.
Papilomas intraductales: suelen provocar sangrado por el pezón. No tienen traducción radiológica exclusiva. Al ultrasonido puede aparecer como nódulo sólido en el interior de un conducto galactóforo. Se debe establecer el diagnóstico diferencial con el carcinoma papilar. El tratamiento es la resección del galactóforo comprometido. Los papilomas únicos no tienen riesgo de malignizarse. Los papilomas múltiples en mujeres jóvenes tienen mayor riesgo de carcinoma posterior.
Carcinoma ductal in situ (CDIS): lesión neoplásica intraductal caracterizada por aumento de la proliferación epitelial con leve a marcada atipia celular que puede progresar a cáncer invasor y que se caracteriza por una distensión de las unidades tubulares de más de 2 milímetros con células de bajo grado nuclear. También se define como cualquier lesión intraductal con células atípicas de grado nuclear 2 ó 3. Puede estar acompañada o no de necrosis y microcalcificaciones (Bethwaite, 1998). La multicentricidad varía entre 9 y 75% en la literatura. Se le acepta un riesgo relativo de 8-10. El 50% de las pacientes portadoras de CDIS desarrolla un cáncer invasor. El tipo histológico es relevante pues el carcinoma tipo comedocarcinoma progresa más frecuentemente y más rápido a carcinoma invasor (Zagouri, 2007).
Históricamente, en tumores agresivos no se han reconocido lesiones precursoras. Se sugiere que el crecimiento acelerado de este grupo de tumores puede explicar la baja frecuencia de hallazgo de lesiones precursoras. El aumento del uso de técnicas para la detección precoz y profilaxis ha permitido encontrar lesiones precursoras en estadios precoces de tumores triple negativo o de tipo basal.
Recomendaciones:
- Lesiones histopatológicas benignas que representan leve aumento del cáncer de mama (RR 1,5-2,0) son aquellas proliferativas sin atipias: adenosis esclerosante, lesiones esclerosantes radiales y complejas, hiperplasia epitelial ductal florida, papiloma intraductal y fibroadenomas complejos.
- Lesiones histológicas benignas con alto grado de riesgo de desarrollar cáncer de mama (RR 4,0-10,0) son aquellas proliferativas con atipias: neoplasia lobulillar in situ (HLA, CLIS), hiperplasia ductal atípica y atipia plana.
- Si la biopsia percutánea muestra lesiones de alto grado de riesgo, se recomienda resección quirúrgica (mastectomía parcial) por posibilidad de subdiagnóstico de cáncer de mama.
- Se recomienda también resección quirúrgica en las siguientes situaciones: discordancia clínica/radiológica/patológica; asociación con otras lesiones de riesgo como cicatriz radiada o tumores papilares y severidad del compromiso del material de biopsia.
1.3 ¿Cuáles son las diferencias entre riesgo de cáncer familiar y riesgo de cáncer hereditario?
Síntesis de la evidencia:
Aproximadamente 10% de los casos de cáncer de mama y 25%–40% de los casos en mujeres menores de 35 años tienen predisposición genética. Las mutaciones de los genes BRCA1 y BRCA2 son responsables de 3-8% de todos los casos de cáncer de mama y 15% a 20% de los casos de cáncer familiar. Además contribuye a aumento del riesgo de cáncer epitelial de ovario. 10% de todos los casos de cáncer de ovario tienen predisposición genética a través de mutaciones BRCA1/2 (Lux, 2006).
Los primeros trabajos luego de la secuenciación de los genes BRCA1 y BRCA2 describían cáncer hereditario con criterios básicos que fueron los que se utilizaron en la selección de las familias con cáncer de mama y de alto riesgo. Este criterio de hereditario ha sido mayoritariamente utilizado en numerosos manuscritos publicados en los que se realizó el tamizaje de los genes BRCA1 y BRCA2. El término cáncer familiar ha sido poco empleado en la selección de familias de alto riesgo de cáncer de mama, y se refiere a la presencia de un familiar (aparte del caso índice) sin importar el grado de parentesco y la edad de aparición del cáncer de mama.
En cáncer hereditario se han identificado al menos dos oncogenes supresores denominados BRCA1 y BRCA2 relacionados con el control de proliferación, expresión génica y reparación del daño producido en el DNA (Schwartz, 2007; Lux, 2006). Se transmiten por herencia autosómica dominante. La pérdida de su funcionalidad requiere de la alteración de ambos alelos del cromosoma. Las alteraciones corresponden a mutaciones puntuales, inserciones, deleciones, etc. La mutación que inactiva funcionalmente a estos genes supresores de tumor suele corresponder a una deleción de una región del gen lo que produce la pérdida de heterozigocidad. Cuando estos genes están mutados y son heredados, se asocian a un riesgo de 50% a 80% de desarrollar cáncer de mama y de 20% a 40% de cáncer de ovario durante toda la vida. Esto debido a que las proteínas codificadas por estos genes mutados influyen en la reparación del DNA y en el control de la replicación de las células epiteliales de la mama (Lux, 2006; Berliner, 2007; Veltman, 2008). Las portadoras de las mutaciones descritas desarrollarán la enfermedad a edades más tempranas que lo observado en casos de cánceres esporádicos. Como se trata de herencia autonómica dominante, cada hijo tiene 50% de probabilidades de heredar la mutación, es transmitido igualmente por ambos sexos y lo habitual es que no se salten generaciones.
Los genes BRCA1 y BRCA2, representan un tercio de los casos de cáncer hereditario de la mama. Los casos restantes estarían ligados a la presencia de mutaciones en genes diversos, la mayoría aún desconocidos.
En el cáncer de mama familiar existe afectación de una mujer con 2 ó más familiares de 1º y 2º grado con cáncer de mama a cualquier edad. Se debe probablemente a interacción de factores medioambientales con factores genéticos (no identificados). Se han realizado intentos de cuantificar el riesgo de desarrollar cáncer de mama en función del número y de la edad de familiares afectos con riesgo relativo de cáncer de mama de 1,8 a 3,8 (Cuzick, 2006; Sivell, 2007).
Nivel de evidencia II-III
Recomendaciones:
- El cáncer de mama familiar es aquél en que existe afectación de una mujer con 2 o más familiares a cualquier edad debido a interacción de factores medioambientales con factores genéticos no identificados. El riesgo depende del número y de la edad de los familiares afectos (RR 1,8–3,8).
- El cáncer de mama hereditario es debido a diversas mutaciones de los oncogenes supresores BRCA1 y BRCA2 relacionados con el control de proliferación celular. Las mutaciones son transmitidas por herencia autosómica dominante. Los genes mutados, cuando son heredados se asocian a un riesgo de 50–80% de desarrollar cáncer de mama y 20–40% de desarrollar cáncer de ovario durante toda la vida.
2. Objetivando el riesgo de cáncer de mama
2.1 ¿Cuáles son los modelos matemáticos que han demostrado utilidad en la cuantificación del riesgo de cáncer de mama y que parámetros utilizan?
Síntesis de la evidencia:
Los modelos matemáticos cuantifican y objetivan el riesgo de desarrollar cáncer de mama a una edad determinada. Esto permite expresar el riesgo en forma cuantitativa con datos numéricos. Los distintos modelos han sido evaluados a través de estudios observacionales y modelos de simulación.
Nivel de evidencia II
1. Modelo de Gail modificado por Costantino (Gomez, 2006; Decarli, 2006; Bondy, 2006; Crispo, 2008).
Predice el riesgo a 5 años y hasta el final de la vida. Se considera riesgo alto cuando el riesgo de desarrollo de cáncer de mama es > 1,7% en los siguientes 5 años. Incluye las variables: edad, raza, edad de menarquia, edad del primer parto, historia familiar de primer grado con cáncer de mama, antecedentes de biopsias mamarias previas y la presencia de hiperplasias atípicas en biopsias previas. La inclusión de la densidad mamaria radiológica en el modelo de Gail junto a otros factores modificables parecen promisorios pero aun no existe evidencia suficiente. El modelo de Gail ha identificado grupos de mujeres de alto riesgo para estudios de quimioprevención, pero subestima el grado del riesgo en mujeres con historia familiar (Crispo, 2008). El modelo ha sido validado por numerosos estudios demostrando una relación entre los cánceres esperados y los observados de 1,03.
Limitaciones del Modelo de Gail:
- No considera la edad del diagnóstico de los familiares con cáncer de mama.
- No considera a los familiares de segundo grado con cáncer de mama, tampoco los cánceres bilaterales.
- No considera el antecedente de cáncer de ovario en la familia.
- Sobreestima en 30% el riesgo de mujeres que no están en un programa de tamizaje.
- No es sensible para mujeres menores de 35 años, con historia familiar sugerente de mutaciones genéticas, historia previa de cáncer de mama, CLIS o CDIS, o para mujeres que no están en un programa de tamizaje.
- No es preciso para calcular el riesgo individual de una mujer. La precisión individual ha sido estimada en 0,58 a cinco años. Sólo 44% de los cánceres que se diagnostican en estos programas tienen estimado riesgo mayor a 1,67% a cinco años.
Considerando las limitaciones del modelo, éste otorga en forma rápida la estimación del riesgo de cáncer de mama en muchas mujeres. Es una herramienta útil y ha sido utilizado en los estudios de prevención NSABP P-1 y NSABP P-2 o STAR.
2. Modelo de Claus
Publicado en 1994 con los datos del estudio CASH, diseñado para mujeres con antecedentes familiares de cáncer de mama, incluye antecedentes familiares de primer y de segundo grado y la edad de diagnóstico de ellos. El modelo calcula la probabilidad de desarrollar cáncer de mama en un período de tiempo determinado o a una edad determinada. Es buen complemento del modelo de Gail en mujeres con antecedentes familiares de cáncer de mama. Tanto el modelo de Gail modificado por Costantino como el modelo de Claus, no deben ser utilizados en pacientes con antecedentes personales de cáncer de mama o en portadoras conocidas de mutaciones genéticas de alta penetrancia (Gómez, 2006).
3. Otros programas computacionales
Existen diversos programas computacionales para evaluación de pacientes de alto riesgo de cáncer de mama. Uno de ellos es el creado por Parmigiani y colaboradores llamado el BRCA Program o BRCA-PRO®, diseñado para determinar la probabilidad de mutación en los genes BRCA1 y BRCA2. Presenta correlación en la predicción de mutaciones. Si aparece una probabilidad mayor de 10% se recomienda la realización de estudio genético, ya que estas mujeres tienen 100 veces más riesgo de mutaciones al compararlas con la población general cuyo riesgo es de 0,1%.
Otro programa es el CancerGene®, diseñado para construir el árbol genealógico de las mujeres. Calcula los riesgos y probabilidades en función de datos ingresados en la construcción del pedigrí. Además incorpora a los otros modelos, como el Gail, Claus, BRCA-PRO, Myriad I y Myriad II.
La objetivación del riesgo según modelos matemáticos se revisa según cada modelo con énfasis en las fortalezas y debilidades de cada método. Es fundamental combinar los diferentes modelos para la mejor cuantificación del riesgo de cada mujer (Gómez, 2006; Consenso Italiano, 2008).
Ventajas de los modelos matemáticos:
- Establecen en forma rápida y objetiva (dato numérico) el riesgo de cáncer de mama de las mujeres.
- El poder objetivar el riesgo permite educar a las pacientes y establecer un manejo racional en la disminución de éste.
Desventajas de los modelos matemáticos:
- Calculan el riesgo en base a datos poblacionales; existe una variación individual que no se puede calcular.
- No usan todas las variables que se relacionan con el aumento de riesgo.
Recomendaciones:
- La estimación del riesgo es competencia del médico especialista y se basa en la evaluación de la historia oncológica personal y familiar.
- Existen modelos de cálculo estadístico que ayudan a la cuantificación del riesgo de cáncer de mama y a la evaluación de la probabilidad de mutación en los genes BRCA1 y BRCA2.
- Los modelos que han demostrado utilidad son principalmente los modelos de Gail modificado por Costantino, Claus, BRCA-PRO y CANCER-GENE.
- Si el riesgo, estimado por modelos matemáticos y programas computacionales, de ser portador de una mutación de alta penetrancia en los genes BRCA1 e BRCA2 es mayor de 10%, se recomienda realizar el examen genético.
- Se recomienda disponer de laboratorios adecuados para estudio genético en que estén validadas las técnicas metodológicas
2.2 ¿Cómo seleccionar a las mujeres que necesitan un estudio del riesgo genético de cáncer de mama?
Síntesis de la evidencia:
La identificación de mujeres y hombres para realizar el estudio genético ha sido controvertida. Se han diseñado numerosos sistemas para cuantificar el riesgo genético, muchos de ellos difíciles y que requieren de tiempo adecuado para estudiar detalladamente los antecedentes oncológicos familiares de al menos tres generaciones.
Existen criterios clínicos para definir cáncer de mama hereditario debido a probables mutaciones en los genes BRCA1 y BRCA2, que corresponden a los criterios de historia familiar con los que se han seleccionado familias a las que se les ha realizado el estudio de ligamiento genético para la identificación de los genes (Schwartz, 2007; Lux, 2006; Berliner, 2007; Veltman, 2008). La edad recomendada es sobre 25 años.
Estos criterios son:
- Tres familiares de 1° o 2° grado con cáncer de mama, en dos generaciones sin importar la edad de aparición del cáncer,
- Dos familiares con cáncer de mama de 1° o 2° grado, uno con diagnóstico antes de los 40 años.
- Dos familiares de 1° o 2° grado con cáncer, uno de mama y otro de ovario.
- Dos familiares de 1° o 2° grado con cáncer de mama, uno de ellos en un hombre.
- Familiar con cáncer de mama bilateral sincrónico.
- Familiar de 1°/2° grado con cáncer de mama antes de los 35 años.
- Familiar con cáncer de mama y ovario.
- Familiar con cáncer de mama antes de los 50 años con características histológicas de “triple negativo”, ya que tienen mayor probabilidad de mutación BRCA1.
Las mutaciones BRCA1 y BRCA2 presentan alta probabilidad de cáncer mamario de aparición en edades precoces, de cáncer de mama bilateral y de multifocalidad/multicentricidad.
Los modelos matemáticos ayudan a seleccionar mujeres para el estudio genético. El BRCA-PRO®, diseñado para determinar la probabilidad de mutación en los genes BRCA1 y BRCA2, presenta correlación en la predicción de mutaciones. Sobre 10% de probabilidad sugiere test genético, ya que estas mujeres tienen 100 veces más riesgo de mutaciones al compararlas con la población general de 0,1% (Schwartz, 2007; Lux, 2006). La indicación del examen genético debe ser siempre evaluada por el médico y ofrecerse al individuo afectado; si ello es imposible, al familiar asintomático con grado de parentesco más cercano (Consenso Italiano, 2008).
Nivel de evidencia II-III
La American Society of Clinical Oncology (ASCO) recomienda realizar el estudio de mutaciones en los genes BRCA1 y 2 en las siguientes situaciones (Vogel, 2003):
- Antecedentes familiares significativos de cáncer de mama a edades tempranas.
- Cuando el resultado del estudio es correctamente interpretado.
- Cuando el resultado influirá en el manejo clínico del paciente o de los familiares.
Nivel de evidencia IV
Recomendaciones:
- El estudio genético se debe recomendar cuando el resultado del estudio es correctamente interpretado y cuando el resultado influirá en el manejo clínico del paciente o de los familiares.
- Se debe realizar primeramente al individuo afectado; si ello es imposible, al familiar con más próximo grado de parentesco.
A. Selección en base a criterios clínicos de historia familiar:
- Tres familiares de 1° grado con cáncer de mama a cualquier edad.
- Dos familiares con cáncer de mama, uno diagnosticado antes de los 41 años.
- Dos familiares con cáncer; uno de mama y el otro epitelial de ovario.
- Dos familiares con cáncer de mama en la familia, uno de ellos en un hombre.
- Un familiar con cáncer de mama bilateral.
- Un familiar con cáncer de mama antes de los 35 años.
- Un familiar con cáncer de mama y epitelial de ovario.
- Familiares con cáncer de mama antes de los 50 años con características histológicas de “triple negativo”.
B. Selección apoyado por modelos matemáticos
- BRCA-PRO sobre 10% de probabilidad.
2.3 ¿Qué debe analizar el estudio genético?
Síntesis de la evidencia:
El estudio de mutaciones genéticas que aumentan el riesgo de cáncer de mama se ha desarrollado progresivamente en los últimos años. Los factores genéticos se han dividido en forma arbitraria en genes de baja penetrancia y genes de alta penetrancia.
Genes de baja penetrancia. Cada vez se están conociendo más. Las mutaciones de estos genes confieren un leve a moderado aumento del riesgo de cáncer de mama. Dependiendo de la sensibilidad de cada individuo, pueden interactuar con otros factores de riesgo ambientales, uso de alcohol, terapia de reemplazo hormonal, etc. Desgraciadamente, aún no se conoce exactamente la interacción de estas mutaciones con otros factores de riesgo por lo que, hasta el momento, no se recomienda su estudio y detección (Schwartz, 2007).
Genes de alta penetrancia. Son genes supresores de tumor que regulan la proliferación celular creando proteínas que reparan el DNA previniendo la carcinogénesis. Son conocidos el BRCA1, BRCA2, PTEN y Tp53, cuyas mutaciones son responsables de los síndromes de cáncer de mama hereditario. Mutaciones de los genes PTEN y Tp53 conllevan a los síndromes de Cowden y Li-Fraumeni.
Las mutaciones BRCA1 y BRCA2, aunque diferentes en sus características, se consideran juntas para todos los estudios debido a que sus consecuencias son similares, 50%-80% de riesgo de desarrollar cáncer de mama y 20%-40% de riesgo de cáncer epitelial de ovario a lo largo de la vida. El cáncer de mama en portador de mutación BRCA1 tiende a desarrollarse en mujeres jóvenes, es de alto grado histológico y con frecuencia de tipo “triple negativo”. El cáncer en portador de BRCA2 es frecuentemente de tipo luminal, es decir, receptores de estrógenos y progesterona positivos. El papel de estas dos mutaciones en el desarrollo del “cáncer ductal in situ” es incierto.
Entre aproximadamente 10 y 15% de los individuos testeados se puede detectar una mutación de significado incierto (VUS) que causa dificultades en la consejería y en la estimación del riesgo. El manejo clínico de mujeres con mutaciones VUS debe ser personalizado y considerar factores de riesgo personales y familiares. Se necesita mayor investigación para reclasificar este tipo de mutaciones. El hecho de no encontrar una mutación conocida en el examen no descarta la posibilidad que existan algunas otras mutaciones aún no determinadas.
La alteración genética indica alto riesgo de presentar cáncer de mama (50-80%) y cáncer de ovario (20-40%) en el transcurso de la vida (hasta los 75-80 años) (Schwartz, 2007; Lux, 2006). Si bien no hay estudios de riesgo realizados en Chile, se puede asumir que el riesgo en nuestro país es similar al reportado en los estudios de los Estados Unidos de América y Europa. La prevalencia estimada de mutaciones BRCA1 y 2 es de 1 por 250-500 individuos en poblaciones no judías. Mientras menor es la edad del familiar afectado y mayor el número de familiares enfermos, mayor es la probabilidad de ser portador de las mutaciones. En judíos Ashkenazi, 1% portan la mutación 185delAG (BRCA1), 0,5% portan la mutación 5382insC (BRCA1) y 1% la mutación 6174delT (BRCA2). En esta población judía, la frecuencia de las tres mutaciones es 1 en 40 individuos.
Análisis. En los pacientes con cáncer de mama no de origen Ashkenazi el estudio debe incluir la secuenciación completa del DNA de los genes BRCA1 y 2. Si a un individuo enfermo de cáncer mamario se le detecta una determinada mutación, en los familiares se recomienda buscar sólo esa mutación y no secuenciar todo el gen. Si se trata de un paciente judío Ashkenazi la sugerencia es realizar el estudio de las tres mutaciones propias de esta población. Si ellas son negativas, se sugiere entonces la secuenciación completa (Schwartz, 2007; Lux, 2006)
Información.
Antes del estudio: asegurar la confidencialidad del examen y de sus resultados. Informar que el resultado demora varias semanas debido a lo complejo de la metodología para secuenciar el DNA. Informar que la probabilidad de encontrar una mutación en el gen BRCA1 o BRCA2 es alrededor de 20%. En aproximadamente 10 a 15% de los individuos testeados se puede detectar una mutación de significado incierto (VUS) que causará dificultades en la consejería y en la estimación del riesgo. Finalmente, el hecho de no encontrar una mutación conocida en el examen no descarta la posibilidad que existan algunas otras mutaciones aún no determinadas (Schwartz, 2007).
Presencia de mutación en el familiar con cáncer de mama: explicar que en la familia existe una mutación en el gen BRCA y que la alteración genética indica alto riesgo de presentar cáncer de mama (50-80%) y cáncer de ovario (20-40%) en el transcurso de la vida. Como no hay estudios de riesgo realizados en Chile, se debe informar que este riesgo es una estimación según estudios europeos y de Norteamérica.
Presencia de una mutación en BRCA1/2 en una persona sana: informar que la mutación encontrada es responsable del cáncer de mama (u ovario) en su familiar, y que puede causarle a ella un cáncer de mama con riesgo de 50-80% y/o cáncer de ovario con riesgo de 20-40% en el transcurso de la vida (hasta los 75-80 años). Se debe informar que el riesgo es una estimación según estudios europeos y de Norteamérica. Además se debe referir a su médico especialista para una adecuada vigilancia y prevención.
Recomendaciones:
- El estudio genético puede detectar mutaciones específicas de los genes BRCA1 y 2, de transmisión autonómica dominante, mutaciones de significado incierto (VUS) o ausencia de mutaciones demostrables.
- El estudio genético incluye la secuenciación completa del DNA de los genes BRCA1 y 2. Si al paciente se le detecta una determinada mutación, en los familiares se recomienda buscar sólo esa mutación y no secuenciar todo el gen.
- En la población judía Ashkenazi se sugiere realizar el estudio de las tres mutaciones propias de esta población. Si ellas son negativas, se sugiere entonces la secuenciación completa.
2.4 ¿Cómo se clasifican las mujeres según el nivel de riesgo de cáncer de mama después de la aplicación de los distintos modelos matemáticos y estudios genéticos?
Síntesis de la evidencia:
Según los factores de riesgo, las mujeres se pueden clasificar en 4 grupos según su categoría de riesgo (Schwartz, 2007; Gómez, 2006; Worsham, 2007; Vogel, 2003):
- Riesgo similar al de la población general.
- Riesgo moderado. Riesgo mayor al de la población general pero su riesgo relativo es < 5. Incluye uno o más factores de riesgo menores.
- Alto riesgo. Riesgo relativo => 5. Incluye antecedentes de carcinoma lobulillar in situ, hiperplasias atípicas, cicatriz radiada y mujeres con dos parientes de 1° grado con cáncer de mama sin mutaciones demostradas.
- Altísimo riesgo. Riesgo relativo > 10. Portadoras de mutaciones de alta penetrancia o antecedente de irradiación de tórax antes de los 30 años.
Nivel de evidencia II
3. Estrategias de vigilancia y seguimiento
3.1 ¿Cuál es el valor del auto-examen y examen clínico en el seguimiento de mujeres de alto riesgo?
Las estrategias actualmente disponibles basadas exclusivamente en el examen clínico y autoexamen para la detección temprana del cáncer de mama en la población en general no son suficientes para la vigilancia de mujeres con alto riesgo y riesgo hereditario de cáncer de mama y/o de ovario. No se encontró evidencia científica para responder a esta pregunta.
3.2 ¿Con qué frecuencia se debe realizar el estudio de imágenes (mamografía y ecotomografía) en el seguimiento de mujeres de alto riesgo de cáncer de mama?
Síntesis de la evidencia:
La mamografía continúa siendo la base del tamizaje de cáncer de mama (Berg, 2008), aunque la tasa de cáncer de intervalo con mamografía es alta, entre 36 y 56%.
Nivel de evidencia I
Un estudio de cohorte con seguimiento clínico y mamográfico en pacientes de riesgo moderado, alto y portadoras de mutaciones BRCA1 y 2, encuentra en estas últimas altas tasas de detección, ratio observado-esperado y menor sensibilidad, con un estadio tumoral desfavorable al momento del diagnóstico, sugiriendo la necesidad de seguimiento más intensivo, especialmente en menores de 40 años (Brekelmans, 2001).
Nivel de evidencia II
En una serie de casos en mujeres de altísimo riesgo por irradiación previa por linfoma de Hodgkin el tiempo de desarrollo del cáncer fue de 8 a 34 años con un promedio de 18 años. La mamografía demostró el 90% de los canceres (Dershaw, 1992).
Nivel de evidencia III
El ultrasonido (US) tiene algunas ventajas sobre la resonancia magnética (RM). Es bien tolerado, ampliamente disponible y relativamente barato. La sensibilidad es mejor con mamografía + US que con mamografía sola (52%-77%), pero inferior al uso suplementario de resonancia magnética. (Berg, 2008; Berg, 2009).
Nivel de evidencia I-II
A partir de la evidencia disponible se han recomendado distintos esquemas de seguimiento para grupos de alto riesgo (Dershaw, 2000; Berg, 2009), que sirven de base a las recomendaciones de este consenso:
- En mujeres con riesgo moderado o alto riesgo (familiares de primer grado con cáncer de mama), mamografía anual comenzando 10 años antes de la edad de presentación del cáncer en el familiar. No se recomienda antes de los 30 años, a menos que se conozca o sospeche una mutación BRCA.
- En mujeres de alto riesgo por antecedentes de biopsia previa con neoplasia lobular, HDA, HLA, CLIS o cicatriz radiada, se recomienda mamografía anual.
- En mujeres de altísimo riesgo por mutaciones BRCA1 y 2, mamografía anual desde los 25 años.
- En mujeres de altísimo riesgo por irradiación de tórax y/o mediastino mayor o igual a 20 Gy, mamografía anual después de 8 años de finalizada la radioterapia o desde los 25 años.
Tamizaje con Ultrasonido (O’Driscoll, 2001; Berg 2009):
- Mujeres de altísimo riesgo que no toleren o se encuentre contraindicada la resonancia magnética mamaria (claustrofobia, clips aneurismales, marcapasos, implantes metálicos, disfunción renal).
- Mujeres de alto riesgo con mamas densas.
Recomendaciones:
Se recomienda realizar mamografía anual desde la siguiente edad de la mujer de alto riesgo:
- Altísimo riesgo:
a) Entre 20 y 25 años de edad: pacientes con mutación demostrada BRCA1 o BRCA2.
b) Después de los 25 años de edad u 8 años de finalizada la radioterapia en pacientes con irradiación de tórax por cáncer. - Alto riesgo:
a) 10 años antes del diagnóstico de cáncer de mama del familiar de primer de grado, con un tope de 30 años.
b) Independiente de la edad: en mujeres de alto riesgo por antecedente personal de cáncer de mama, antecedentes de HDA, HLA, CLIS o C. radiada en biopsias previas. - Ultrasonido complementario de tamizaje en:
a) Mujeres con riesgo intermedio con mamas densas.
b) Mujeres con muy alto riesgo que no toleren la resonancia magnética mamaria. - El seguimiento mediante imágenes a mujeres de alto riesgo se recomienda mientras exista expectativa de vida de 5 a 7 años, siempre que se pueda efectuar tratamiento adecuado en caso de diagnóstico de cáncer (hasta 90 años según expectativa de vida actual.
3.3 ¿Qué tipo de mamografía debe utilizarse: convencional o digital?
Síntesis de la evidencia:
La evidencia de ensayos aleatorios y estudios diagnósticos ha demostrado que la mamografía digital tiene igual o mayor detección de cáncer y mayor especificidad que la técnica convencional. En especial ha demostrado mayor sensibilidad en mujeres con mamas densas y/o menores de 50 años (Berg, 2008).
Nivel de evidencia I
Recomendaciones:
- La mamografía se debe realizar en forma digital cuando sea posible en mujeres con mamas densas, y/o menores de 50 años.
3.4 ¿Cuál es la utilidad de la resonancia magnética mamaria (RM) en la vigilancia de mujeres de alto riesgo?
Síntesis de la evidencia:
Tamizaje suplementario con resonancia magnética mamaria:
Una revisión sistemática de 11 estudios prospectivos no aleatorios en mujeres de alto riesgo, emplea resonancia magnética además de mamografía con o sin ultrasonido y examen físico. Los cánceres de intervalo fueron menos de 10% en los estudios con más de una ronda de tamizaje.
En trabajos con mayor tasa de detección de carcinoma ductal in situ, la mayoría de estos fueron detectados por resonancia magnética. Del total de cánceres detectados, más de 50% correspondieron a cáncer in situ o menores de 1 cm. Sólo entre 12 y 21% de los tumores infiltrantes se acompañaron de linfonodos positivos. En los pocos estudios en que existen datos por año de tamizaje, el estadio tumoral fue similar para prevalencia e incidencia. La sensibilidad de la resonancia magnética fue mayor que la de la mamografía en todos los estudios y la especificidad de la resonancia fue menor que la de la mamografía en todos excepto uno (Kuhl, 2007). En dos de tres estudios que reportaron especificidades por ronda, ésta fue superior en las rondas posteriores.
Definiendo positivo sólo a los BI-RADS 4 o 5, la resonancia magnética asociada a mamografía se asoció al mayor OR diagnóstico y asumiendo una probabilidad de enfermedad pretest de 2%, hallazgos negativos en mamografía y resonancia reducen la probabilidad de lesiones biopsiadas sospechosas a 0,3%, mientras que una mamografía sola la reduce a 1,4%.
Resultados combinados:
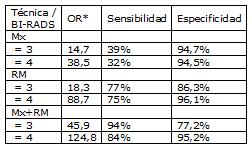 Tamaño completo
Tamaño completo *OR=Razón entre la posibilidad de Ca si el test es (+) entre quienes tienen la enfermedad, y la posibilidad de Ca si el test es (+) entre quienes no tienen la enfermedad. Mide la exactitud global del test. A mayor OR, mayor poder discriminatorio del test (mayor posibilidad de que el resultado sea cierto si efectivamente la persona tiene cáncer).
Aunque los 11 estudios usaron intervalo de 1 año para tamizaje, puede no ser lo mejor para todos los grupos de alto riesgo. Algunas limitaciones de la investigación son las diferencias en la población de pacientes, experiencia del centro y criterios para resultados positivos de tamizaje que resultan en heterogeneidad entre los estudios incluidos (Warner, 2008).
Nivel de evidencia II
No existen estudios con datos de supervivencia total o libre de enfermedad al agregar resonancia magnética mamaria a la mamografía en el grupo de alto riesgo, pero se asume que al detectar más cánceres con linfonodos negativos, reduciría la mortalidad por cáncer de mama (Warner, 2008; Berg, 2009). La Sociedad Americana de Oncología Clínica (ASCO) y la Guía Clínica Europea de Panel de Expertos acerca de tamizaje con resonancia magnética como complemento de mamografía (Saslow, 2007) sugieren las siguientes recomendaciones:
Resonancia magnética anual, basada en evidencia derivada de ensayos de tamizaje no aleatorios y estudios observacionales:
- Mutaciones BRCA.
- Familiar de primer grado con BRCA, no examinada o estudiada.
- Riesgo en la vida mayor o igual a 20-25% según BRCAPRO u otro modelo basado en historia familiar.
Resonancia magnética anual, basada en opinión de consenso de expertos, a partir del riesgo estimado de desarrollar cáncer a lo largo de la vida en cada grupo:
- Radioterapia de tórax entre los 10 y 30 años de edad.
- Síndrome Li-Fraumeni y sus familiares de primer grado.
- Síndromes de Cowden y Bannayan-Riley-Ruvalcaba y sus parientes de primer grado.
Evidencia insuficiente a favor o en contra de resonancia magnética como tamizaje (recomienda decisiones caso a caso):
- Riesgo en la vida <15-20% según BRACA-PRO u otro modelo basado en historia familiar.
- Carcinoma lobulillar in situ o hiperplasia lobulillar atípica.
- Hiperplasia ductal atípica.
- Mamas heterogéneas o extremadamente densas en mamografía.
- Mujeres con antecedente personal de cáncer, incluyendo carcinoma ductal in situ.
Recomendación contraria a resonancia magnética como tamizaje, basada en opinión de consenso de expertos:
- Mujeres con riesgo en la vida <15%.
Un estudio de serie de casos en pacientes con cáncer e historia familiar, seleccionadas a partir de un estudio de cohorte prospectivo, encuentra que los fenotipos de imágenes difieren entre las categorías de riesgo. Del total de cánceres infiltrantes, 20% apareció como impregnación del tipo no masa y 33% tuvo características cinéticas benignas. 23% de los cánceres infiltrantes se presentaron como masas bien delimitadas, sin calcificaciones, como frecuentemente aparece en los fibroadenomas, pero sin los signos típicos de realce de estos.
Las portadoras de mutación BRCA1 exhibieron 80% de estas lesiones con morfología benigna y ninguno de sus cánceres presentó microcalcificaciones ni fue carcinoma ductal in situ. En cambio, los cánceres de las portadoras de mutación BRCA2 y mujeres en riesgo moderado presentaron características similares a los cánceres esporádicos. Con respecto a la ubicación, 67% de los tumores en mujeres de alto riesgo y con mutaciones (p<0,009) (Schrading, 2008) se encontró en localización posterior y prepectoral.
Otro estudio retrospectivo que evaluó el aspecto en mamografía y resonancia magnética de lesiones malignas en pacientes portadoras de mutación BRCA1 y 2, encontró diferencias significativas como mayor índice de actividad mitótica y tumores más redondeados y bien definidos en comparación con los cánceres esporádicos. Además, en resonancia magnética se aprecia frecuentemente realce en anillo. No hubo diferencias significativas en la cinética de impregnación (Veltman, 2008).
Nivel de evidencia III
Recomendaciones:
- En mujeres de altísimo riesgo se recomienda resonancia magnética de la mama anual junto a mamografía anual.
a) Entre los 25 y 30 años de edad en portadoras o sospechosas de mutación BRCA2.
b) Entre los 20 y 25 años de edad en portadoras o sospechosas de mutación BRCA1.
c) 8 años después de radioterapia a tórax y/o mediastino o a partir de los 25 años. - En mujeres con mutación BRCA, considerar fenotipos de imágenes diferentes a las habituales, ya que presentan frecuentemente cánceres con patrones morfológicos redondeados y bien delimitados.
- En mujeres de alto riesgo se recomienda evaluar caso a caso la resonancia magnética mamaria como método de tamizaje.
3.5 ¿Cuál es la utilidad de las muestras de epitelio mamario (lavado ductal, ductoscopía) en la vigilancia de mujeres de alto riesgo?
Síntesis de la evidencia:
El fundamento de estas técnicas se basa en que el cáncer de mama se genera a partir de cambios en el epitelio de los conductos mamarios (Gomez, 2006). Las técnicas propuestas para ello son principalmente la aspiración periareolar con aguja fina, el lavado ductal y la ductoscopía (Arun, 2007; Khan, 2004; Sarakbi, 2006). El lavado ductal consiste en la obtención de células mediante la canulación de conductos mamarios y lavado de ellos con suero fisiológico. La ductoscopía utiliza fibra óptica que canaliza los conductos mamarios y visualiza endoscópicamente el árbol ductal.
La comparación entre aspiración periareolar con aguja fina y lavado ductal aparece reportada en un estudio en 86 mujeres de alto riesgo y reporta que ambos procedimientos son bien tolerados con obtención de muestras adecuadas, siendo levemente superior la aspiración con aguja fina. Sin embargo, se necesitan más estudios para validar las técnicas (Arun, 2007).
Otro estudio analiza en 39 mujeres el lavado ductal con el estudio de la pieza de mastectomía después de cirugía de cáncer de mama. La sensibilidad del lavado ductal fue 17%, la especificidad de 100% y la correlación sólo de 19% (Khan, 2004).
Un estudio colaborativo en Reino Unido y Australia en mujeres de alto riesgo reporta que la citología aspirativa fue exitosa en 38% con sensibilidad de 4 a 21%. El lavado ductal es suficiente en 27% y detecta atipias en 6% de los casos. La ductoscopia puede detectar lesiones precoces pero colabora en reducir márgenes positivos sólo en 5 a 23% (Locke, 2004).
Otra serie de 26 mujeres de alto riesgo con ductoscopía reporta sensibilidad del método de 16% y pudiera ser útil para guiar la cirugía conservadora (Sarakbi, 2006).
Nivel de evidencia III
Recomendaciones:
- La obtención de muestras de epitelio de los conductos mamarios se puede realizar mediante aspiración periareolar con aguja fina, lavado ductal y ductoscopía.
- La evidencia actual demuestra baja sensibilidad de los métodos, especificidad variable y baja correlación con la anatomía patológica.
- Se necesita mayor evidencia para validar estos métodos en la vigilancia de mujeres de alto riesgo de cáncer de mama.
4. Estrategias de prevención de cáncer de mama
4.1 Cambios de estilo de vida: ¿cuáles han demostrado utilidad en la prevención del cáncer de mama?
Síntesis de la evidencia:
Numerosos estudios observacionales han evaluado cambios en el estilo de vida con relación a prevención del cáncer de mama. Un factor de estilo de vida es la actividad física ya que produce tardanza de la menarquia, mayor porcentaje de ciclos anovulatorios y menor cantidad de hormonas sexuales endógenas. Los ejercicios aeróbicos influyen en la recurrencia y en la progresión de la enfermedad después del diagnóstico de cáncer de mama (Rock, 2009). Las mujeres que realizan 3 a 4 horas semanales de ejercicios moderados a vigorosos tienen entre 30 y 40% menor riesgo de desarrollar cáncer de mama que las mujeres sedentarias (McTiernan, 2003). La resistencia a la insulina es un biomarcador de riesgo para cáncer de mama al favorecer el desarrollo tumoral estimulando la proliferación celular o inhibiendo la apoptosis. El ejercicio crónico aumenta la sensibilidad a la insulina, pero tiene mayor efecto el ejercicio intenso que el de mayor duración. La obesidad y sobrepeso también están asociadas a la resistencia a la insulina y a hiperinsulinemia (Campbell, 2007).
Nivel de evidencia II
Un ensayo aleatorio evaluó si era efectivo introducir cambios en la dieta para reducir el consumo de grasa hasta llegar al 20% de total de energía, aumentado el consumo de vegetales y frutas al menos 5 veces al día y cereales 6 veces al día (Ross, 2006). A pesar de no existir diferencia significativa, hubo disminución del riesgo de cáncer de mama en el grupo intervenido. Aunque la evidencia es inconsistente, otros estudios observacionales sugieren que las mujeres sometidas a dieta baja en grasa tienen disminución del riesgo y la dieta podría influir en las características de los receptores hormonales del tumor.
Nivel de evidencia I-II
Estudios observacionales muestran que niveles moderados y altos de consumo de alcohol se asocian a mayor riesgo de cáncer de mama. La ingesta de alcohol produce un aumento de 7% de riesgo de cáncer de mama por cada 10 grs. de alcohol adicional consumido diariamente (McTiernan, 2003).
Nivel de evidencia II
Recomendaciones:
- Se recomienda la actividad física en mujeres en edad fértil. En postmenopáusicas se sugiere además evitar el sobrepeso para disminuir el riesgo de cáncer de mama.
- Se recomienda también energía balanceada, aumento de la ingesta de vegetales y frutas, peso estable con IMC bajo 25.
- En mujeres postmenopáusicas, aumentar la actividad física 60 minutos diarios.
- Menos consumo de alcohol.
4.2 Métodos de quimioprevención. ¿A quiénes pueden beneficiar, cuándo y por cuánto tiempo?
Síntesis de la evidencia:
La quimioprevención es la administración de preparados químicos, naturales o sintéticos, para impedir o revertir la carcinogénesis evitando el desarrollo de un cáncer (Peralta, 2006). Los preparados más estudiados son los que actúan por competencia como los moduladores selectivos de receptores de estrógenos que incluye tamoxifeno y raloxifeno.
A- Tamoxifeno. Cuatro estudios prospectivos randomizados en mujeres de alto riesgo de cáncer de mama (Powles, 2007; Veronesi, 2006; Fisher, 2005; Cuzick, 2007) suman 28.419 mujeres que se randomizan a tamoxifeno 20 mg/día vs placebo durante 5 años. En los dos primeros estudios (Powles, 2007;Veronesi, 2006) si bien no reportan clara prevención de cáncer de mama, el estudio italiano sugiere beneficio para el subgrupo de mujeres que usaron concomitantemente terapia de reemplazo hormonal en la menopausia y tamoxifeno (6 de 793 mujeres vs 17 de 791).
El estudio P1 (Fisher, 2005) reporta disminución del riesgo relativo de cáncer de mama infiltrante de 43% y de cáncer in situ de 37%. La incidencia acumulada de cáncer de mama fue 2,5% para el grupo de tamoxifeno y 4,3% para el grupo placebo. La reducción de la incidencia se observa sólo para tumores receptores estrógenos positivos (RR 0,31 CI 0,22-0,45). El efecto beneficioso es levemente superior en mujeres sobre 60 años.
El estudio IBIS I (Cuzick, 2007) reporta prevención con tamoxifeno de 32%; odds ratio de 0,68 (95% CI 0,50-0,92) en mujeres con riesgo de cáncer de mama RE positivo, confirmando y validando los resultados del P1. Si se suman los 4 estudios de prevención con tamoxifeno se reporta un efecto protector de 38%, hazard ratio de 0,62 (Cuzick, 2003).
Nivel de evidencia I
B - Raloxifeno. Se identifican dos estudios aleatorios.
- El Estudio More (Martino, 2004) de 7.704 mujeres con osteoporosis tratadas con raloxifeno 60 o 120 mg/día vs placebo, que demuestra reducción de la incidencia de cáncer de mama RE positivo de 84% (RR 0,16 (0,09-0,30)).
- El Estudio STAR o NSABP P2 (Vogel, 2006) que randomiza 19.747 mujeres de alto riesgo de cáncer de mama para comparar tamoxifeno 20 mg/día versus raloxifeno 60 mg/día durante 5 años. Se demuestra que el raloxifeno es tan efectivo como el tamoxifeno en reducir el riesgo de cáncer de mama infiltrante y con menos efectos adversos
En cuanto a los efectos adversos, tanto el tamoxifeno como el raloxifeno aumentan entre 2 y 3 veces el riego de eventos venosos tromboembólicos. El tamoxifeno aumenta también 2 a 3 veces el riesgo de cáncer de endometrio en mujeres postmenopáusicas.
Nivel de evidencia I
Otros agentes quimiopreventivos.
- Quimioprevención por supresión: muy escasos estudios con retinoides como la fenretidina (Peralta, 2006) con resultados inciertos no significativos.
- Inhibidores de aromatasas: estudio IBIS II. Estudio prospectivo en marcha aún sin resultados (Cuzick, 2005).
Recomendaciones:
- Es posible prevenir el cáncer de mama receptores hormonales positivo en mujeres de alto riesgo de cáncer de mama (RR > 5) y en menor forma en mujeres de altísimo riesgo (RR > 10).
- Este efecto se logra mediante cambios en el ambiente hormonal estrogénico de la mujer como lo demuestran los estudios con tamoxifeno y raloxifeno.
- Grupos de mujeres de alto riesgo se benefician con estos tratamientos pero los posibles efectos adversos desaconsejan su uso indiscriminado.
- La quimioprevención se puede realizar en mujeres de alto riesgo premenopáusicas y postmenopáusicas.
- Los estudios realizados emplean los preparados por 5 años. No hay evidencia de quimioprevención por períodos más prolongados.
- No existe evidencia de quimioprevención del cáncer de mama receptores hormonales negativos ni de mujeres premenopáusicas de alto riesgo no elegibles para tamoxifeno o raloxifeno.
4.3 Cirugías profilácticas: (mastectomía-ooforectomia), A quienes puede beneficiar? cuándo debiesen indicarse?
Síntesis de la evidencia:
Se distinguen tres tipos de cirugías de reducción de riesgo (profilácticas) en mujeres de alto riesgo de cáncer de mama (Zakaría, 2007):
- Mastectomía total bilateral.
- Mastectomía total contralateral en mujeres con cáncer de mama unilateral.
- Ooforectomía bilateral.
La mastectomía profiláctica es la exéresis completa de la glándula mamaria con o sin conservación del complejo areola-pezón. La ooforectomía profiláctica es la extirpación de ambos ovarios en ausencia de cáncer de mama u ovario. Estos procedimientos se pueden realizar por separado o en conjunto a fin de aumentar el efecto preventivo.
Mastectomía de reducción de riesgo bilateral
Seis estudios de casos-controles o de cohorte, han evaluado el rol de la mastectomía profiláctica en la incidencia de cáncer de mama, tres de ellos en mujeres portadoras de mutación BRCA1-2 (Meijers, 2001; Hartman, 2001; Rebbeck, 2004) y tres en mujeres de alto riesgo por antecedentes familiares marcados (Zakaria, 2007; Hartman, 1999).
En portadoras de mutaciones BRCA1-2, la mastectomía total logra 85-90% de reducción de riesgo con seguimiento promedio de 8 años (Meijers, 2001; Hartman, 2001; Rebbeck, 2004). Al combinar mastectomía con ooforectomía profiláctica, el riesgo relativo de cáncer de mama baja a 0,05 (IC 95% 0,01-0,22) evaluada a 6 años (Rebbeck, 2004).
En mujeres con marcados antecedentes familiares y considerados de muy alto riesgo, la reducción de riesgo alcanza a 89-94% (Hartman, 1999; Zakaria, 2007). No hay evidencia respecto al impacto en la supervivencia global. Un trabajo reporta menor mortalidad por cáncer de mama, con reducción de riesgo de 81-94% (Hartman, 1999).
Nivel de evidencia II
Mastectomía de reducción de riesgo contralateral
Se identificaron seis estudios de cohorte en portadoras de BRCA 1-2 y en mujeres con antecedentes familiares importantes (van Sprundel, 2005; McDonnell, 2001; Herrington, 2005; Peralta, 2000; Kass, 2008; Burke, 2008). En portadoras de mutaciones BRCA1-2 se describe disminución significativa de la incidencia de cáncer mamario contralateral, HR: 0,09 (IC 95% 0,01-0,78) con seguimiento de 4 años. No hay diferencia en supervivencia global (Sprundel, 2005), pero si se asocia a ooforectomía profiláctica, la supervivencia global mejora con HR de 0,12 y la supervivencia especifica asociada a cáncer de mama HR: 0,16. Ambas diferencias alcanzan significación estadística. En mujeres con antecedentes familiares disminuye la incidencia de cáncer contralateral HR: 0,03-0,05. No existen datos concluyentes respecto a supervivencia (Herrington, 2005).
Nivel de evidencia II
Ooforectomía
Cinco estudios, tres de ellos de cohorte, analizan la reducción de riesgo de la ooforectomía profiláctica en mujeres BRCA1-2 (Eisen, 2005; Rebbeck, 2002-1999; Kauff, 2002-2008; Rebbeck, 2009). Existe reducción significativa del riesgo de cáncer de mama con HR: 0,49 IC 95% (0,37-0,65) con seguimiento promedio de 8 años. No hay evidencia respecto al impacto en supervivencia global de las pacientes sometidas a ooforectomía profiláctica.
Nivel de evidencia II
Recomendaciones:
- En mujeres de altísimo riesgo portadoras de mutación BRCA1-2 o de alto riesgo por fuerte historia familiar, la mastectomía de reducción de riesgo bilateral y la mastectomía de reducción de riesgo contralateral disminuyen el riesgo de cáncer de mama en un 90%.
- En portadoras de mutación BRCA1-2, la ooforectomía profiláctica realizada en mujeres antes de los 45 años, disminuye la incidencia de cáncer de mama en 50% y de cáncer de ovario en 90%.
- La combinación de mastectomía de reducción de riesgo con ooforectomía profiláctica parece reducir aún más el riesgo de cáncer de mama a 95%, pero falta evidencia para recomendarlo.
- No existe evidencia con relación a la edad a realizar las cirugías profilácticas. Se recomienda la mastectomía de reducción de riesgo al comprobar portación de mutaciones BRCA1-2. Respecto a la ooforectomía, ésta debe ser recomendada previo a la menopausia, en especial antes de los 45 años.
Notas y Agradecimientos
Este artículo fue redactado en su versión final después de haber recibido las contribuciones y comentarios de los delegados que asistieron a la III Jornada Nacional de Diagnóstico y Tratamiento de Cáncer de Mama, realizada en Coquimbo, Chile, en agosto de 2009. A su vez, las ponencias que se presentaron en esa jornada fueron la síntesis del artículo completo de revisión de la literatura y trabajo previo de la comisión correspondiente. Este trabajo de formulación duró un año, comenzó en junio de 2008 y se llevó a cabo bajo la asesoría de Medwave Estudios Ltda., en el marco del proyecto denominado “Asesoría en la Formulación de Consenso y Recomendaciones en Cáncer de Mama Basados en la Evidencia”. El financiamiento para la ejecución de la asesoría provino de la Sociedad Chilena de Mastología.
La coordinación de la asesoría fue realizada por Vivienne Bachelet; el metodólogo jefe fue Miguel Araujo; y la metodóloga adjunta fue Gabriela Moreno. Colaboró en la sistematización bibliográfica y en el formato final de los documentos, Matías Goyenechea. El artículo definitivo es el resultado del trabajo final presentado a las jornadas de consenso, donde fue conocido, revisado y discutido por los concurrentes, y luego fue revisado por un comité editorial de pares constituido por la misma Sociedad Chilena de Mastología, tras lo cual fue enviado a Medwave para su publicación.

