Artículo de revisión
← vista completaPublicado el 27 de noviembre de 2018 | http://doi.org/10.5867/medwave.2018.07.7354
Síntesis de información biomédica: revisiones narrativas, revisiones sistemáticas y estructuras emergentes
Syntheses of biomedical information: narrative reviews, systematic reviews and emerging formats
Resumen
La divulgación de información biomédica se expande de manera exponencial, lo que representa un desafío para aquellos profesionales de la salud que deseen obtener información integrada de alta calidad y relevancia. Las revisiones, en sus distintos formatos, son herramientas que pueden abordar este problema. Este artículo describe los principales tipos de síntesis de información biomédica, sus estructuras, la utilidad de cada una de ellas, y presenta los últimos formatos desarrollados por las diferentes organizaciones que se dedican a la síntesis de información.
Introducción
El número de artículos que un médico debe leer para mantenerse actualizado, tal como citaba David Sackett en su libro[1], ha crecido de manera exponencial[2]. Para ese entonces, Archie Cochrane ya había previsto que para que un médico se mantuviera actualizado se necesitarían “resúmenes periódicos por especialidad” que asistan al profesional de la salud para la toma de decisiones[3]. Teniendo en cuenta la complejidad cognitiva que implica la tarea de leer de forma adecuada los artículos científicos, en términos del desarrollo de una capacidad crítica y constructiva, como también de conocimientos acerca de la metodología con la cual se realizan las investigaciones biomédicas y la posible existencia de fuentes importantes de sesgos, incluida la manipulación y ocultamiento de datos; hacen que la “valoración crítica de la evidencia científica” sea una tarea ardua para el profesional de salud a la hora de responder sus dudas clínicas y mantenerse actualizado. Las revisiones de la literatura intentan acercar el conocimiento de la evidencia biomédica en sus distintos formatos.
Las revisiones son artículos que sintetizan la información científica utilizando como fuente, en su mayoría, publicaciones primarias de investigaciones originales. Siguiendo el esquema de la medicina basada en evidencia[4],[5], algunos pasos fundamentales para una revisión incluirían:
1) La formulación de una pregunta clínica estructurada bajo el esquema PICO (Patient, Intervention, Comparison, and Outcome,) /tópico de revisión.
2) La búsqueda bibliográfica de información científica.
3) La valoración crítica de los hallazgos.
4) La formulación de conclusiones con base a la evidencia sintetizada.
Considerando lo previamente descrito, existe una amplia gama de artículos denominados indistintamente “revisiones”, pero con diferencias sustanciales en cuanto a los métodos de elaboración y objetivos propuestos[6]. De esta manera, el objetivo de este análisis es esquematizar algunas diferencias entre los diferentes tipos de revisiones y describir los aspectos básicos de cada una de ellas. También señalaremos el rol de algunas organizaciones involucradas en el desarrollo de síntesis y metodología para la síntesis de información biomédica.
Tipos de revisiones
La rigurosidad y la reproducibilidad con la que se realizan los pasos anteriormente señalados, permiten subclasificar a las revisiones en narrativas y sistemáticas.
1. Revisiones narrativas
Son revisiones que sintetizan un tema, sin metodología específica ni declarada previamente. A diferencia de las revisiones sistemáticas, las revisiones narrativas seleccionan la evidencia a sintetizar de un modo no reproducible y sin una búsqueda exhaustiva, por cuanto el lector o investigador no podría seguir los pasos que el autor ejecutó para llegar a las mismas conclusiones. Además, al no utilizar una metodología definida existe un alto riesgo de que la información seleccionada para la síntesis resulte estar sesgada o manipulada, lo que limita las conclusiones y resta confianza en los resultados de este tipo de estudio.
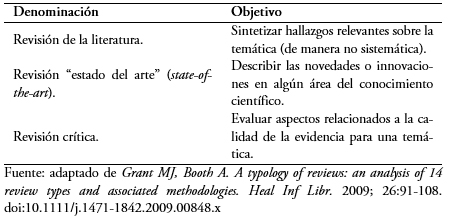
Sin embargo, las revisiones narrativas ocupan un importante lugar en la educación continua, pues actualizan a los lectores respecto de temáticas específicas. Pueden tener distintas denominaciones en virtud de su objetivo específico[6] (Tabla 1), y se diferencian de las revisiones sistemáticas en múltiples aspectos estructurales y procedimentales[7] (Tabla 2).
Las revisiones narrativas pueden ser útiles cuando se requiere responder a preguntas amplias (preguntas tipo “déficit global”)[8] relacionadas con conceptos básicos, por ejemplo, ¿qué es el síndrome de Ehlers-Danlos?, ¿cuál es el curso natural de la infección por varicela? También pueden ser una forma de relevar la opinión de individuos o grupos referentes en una determinada temática. En este sentido, un ejemplo típico de revisión narrativa son los capítulos de los libros de medicina. No obstante, a la hora de responder preguntas más específicas mediante el uso de revisiones narrativas (preguntas tipo “grieta”, por ejemplo ¿el uso de antivirales en adultos con varicela reduce la incidencia de complicaciones secundarias?)[8], la evidencia sintetizada puede ser incompleta, seleccionada de manera sesgada (cherry picking)[9] y difícil de interpretar, debido a la falta de valoración de su calidad y aplicabilidad.
Frecuentemente están desarrolladas por los expertos disciplinares del tema, pero no suelen incluir metodólogos en el desarrollo de este tipo de trabajos. Una única revisión narrativa puede incorporar diferentes poblaciones de estudio, estudios en humanos, modelos animales o estudios in vitro. Puede abordar tópicos sobre etiología, diagnóstico, tratamiento y/o pronóstico.
Con el advenimiento de las revisiones sistemáticas (ver abajo), a veces se ha dado preeminencia a este tipo de revisiones por sobre las narrativas, especialmente en revistas biomédicas. Sin embargo, las revisiones narrativas proveen un entendimiento profundo, reflexivo e interpretativo de las problemáticas con las que el profesional de la salud se encuentra en su cotidianeidad[10]. Esto es especialmente importante cuando se reflexiona sobre los elementos que constituyen la complejidad de la pregunta clínica. Por ejemplo, una pregunta terapéutica puede ser “acotada” en su espectro, pero necesitará sintetizar la información de decenas de ensayos clínicos (para lo cual una revisión sistemática cuenta con métodos para garantizar la transparencia y reproducibilidad de sus hallazgos). Sin embargo, una pregunta sobre las implicancias de una determinada terapéutica puede ser “acotada” en la evidencia que sustenta su respuesta, pero puede requerir una gran elaboración reflexiva y crítica basada en fuentes filosóficas, sociales y nosológicas, entre otras.
 Tamaño completo
Tamaño completo  Tamaño completo
Tamaño completo 2. Revisiones sistemáticas
Estas revisiones permiten responder a una duda clínica específica o sintetizar un tópico utilizando una metodología reproducible, consignada al cumplimiento estricto de un protocolo de investigación previamente establecido y en muchos casos publicado en bases de datos especializadas. Este protocolo incorpora criterios de elegibilidad para los estudios a incluir, un apartado de métodos y análisis estadístico. Este tipo de revisión asimila los cuatro pasos de la medicina basada en evidencia y vincula herramientas específicas para su adecuado y riguroso desarrollo[4]. En la Tabla 3 se muestra un resumen de la relación entre medicina basada en evidencia y la metodología de las revisiones sistemáticas.
Un aspecto central en las revisiones sistemáticas de la literatura, es que se sustentan sobre los hallazgos de búsquedas sistemáticas de todas las fuentes posibles (búsqueda exhaustiva de evidencia publicada y no publicada), lo que intenta minimizar el sesgo de selección, a diferencia de las revisiones narrativas, en las que, la intuición del autor, su experiencia y aún las opiniones de experto podrían influenciar los hallazgos mediante el fenómeno de cherry picking mencionado arriba[11]. Esto no implica que la visión de un experto en la temática puede ser de vital importancia en los métodos y conducción de revisiones sistemáticas, si bien existe cierto debate sobre el rol de estos expertos y la posibilidad de introducir sesgos en el proceso de revisión[12].
 Tamaño completo
Tamaño completo Las revisiones sistemáticas son muy útiles para las preguntas clínicas tipo “grieta” antes mencionadas. Estas preguntas pueden asociarse, por ejemplo, a la evaluación de la efectividad y seguridad de opciones terapéuticas/preventivas, la evaluación de la precisión de métodos diagnósticos o la identificación de los factores pronósticos de una enfermedad (en la Tabla 4 se indican algunos ejemplos). De esta manera, las revisiones sistemáticas surgieron dentro del marco de la medicina basada en evidencia, integrando todos los pasos necesarios para la de información científica en la toma de decisiones en salud.
 Tamaño completo
Tamaño completo Las revisiones sistemáticas utilizan como fuente de información los datos primarios de investigación científica relevante para la pregunta clínica, publicada o no publicada (literatura gris). Así, se prioriza la información proveniente de los ensayos clínicos para las preguntas terapéuticas, de los estudios de cohortes para las preguntas pronósticas y de estudios de corte transversal para aquellas relacionadas con la precisión diagnóstica.
2.1 Calidad de las revisiones sistemáticas
Nos referimos a calidad en revisiones sistemáticas cuando se responde a la pregunta ¿Cuán adecuadamente fue realizada esta revisión?. El instrumento más utilizado para valorar esta pregunta es AMSTAR (A Measurement Tool to Assess Systematic Reviews)[13], que ha sido recientemente actualizado a su versión AMSTAR 2[14] (Tabla 4). También existe otra herramienta llamada ROBIS (Risk of bias in systematic reviews)[15],[16], que intenta determinar si las revisiones sistemáticas pueden haber incurrido en sesgos durante su conducción, los denominados “meta-sesgos”[17] que pudiesen afectar sus conclusiones.
 Tamaño completo
Tamaño completo 2.2 Revisiones sistemáticas y Cochrane
En 1993 se fundó la organización originalmente llamada Cochrane Collaboration, ahora denominada Cochrane. Esta organización está integrada por más de 43 000 profesionales de la salud voluntarios y su misión es “promover la toma de decisiones informada en salud mediante la producción de revisiones sistemáticas accesibles, actualizadas, relevantes y de alta calidad, y otros datos de la investigación resumidos”[18]. Las revisiones sistemáticas realizadas por esta colaboración habitualmente tienen mejor calidad que las revisiones sistemáticas que se realizan por fuera de la misma (revisiones no-Cochrane)[19]. Cochrane cuenta con dos guías metodológicas que asisten al proceso de revisión: el Manual Cochrane[4] y el Manual de Expectativas Metodológicas (MECIR)[20]. Aun así, las revisiones no-Cochrane que utilizan esta rigurosa metodología para la síntesis de información pueden tener igualmente alta calidad. Las revisiones Cochrane, a pesar de tener un proceso de evaluación riguroso durante su elaboración, pueden sufrir también de limitaciones metodológicas[19],[21],[22],[23],[24],[25].
Cochrane tiene una organización geográfica en centros de diversa jerarquía localizados en distintas partes del mundo, que tienen como objetivo contribuir a la misión y las metas de Cochrane. En los países hispanoparlantes se destaca la Red Cochrane Iberoamericana, muy activa en la producción y diseminación de revisiones sistemáticas. La red cuenta con proyectos de trabajo colaborativo entre países, como el proyecto de búsqueda manual[26] que intenta identificar ensayos clínicos no publicados o de difícil acceso con el objetivo de disminuir el sesgo de diseminación.
Una de las innovaciones metodológicas más importantes que ha incorporado Cochrane en sus revisiones es la metodología GRADE[27]. GRADE es un sistema de valoración crítica de la evidencia que permite sintetizar la confianza en los hallazgos con una metodología estructurada y transparente, y mediante un lenguaje simplificado, lo que permite la integración de la calidad de la evidencia con los resultados, resumiéndola en calidad como alta, moderada, baja y muy baja. Esta gradación de la evidencia tiene implicancias tanto en el ámbito clínico (que se relaciona con el nivel de incertidumbre que se tiene al momento de adoptar una decisión clínica), como investigativo (al analizar el área en que esta incertidumbre requiera de estudios esclarecedores).
2.3 Otras organizaciones que desarrollan revisiones sistemáticas
Existen otras organizaciones similares a Cochrane que promueven la producción de revisiones sistemáticas de alta calidad en diversos tópicos. Algunos ejemplos incluyen a la Colaboración BEME (www.bemecollaboration.org), enfocada en temáticas de educación médica, y la Colaboración Campbell (www.campbellcollaboration.org), enfocada en tópicos sociales. Las revisiones sistemáticas han cobrado relevancia también en otros campos como el de la investigación básica y traslacional[28]. Dos organizaciones que han promovido iniciativas para el desarrollo de revisiones sistemáticas en estas áreas son CAMARADES (Collaborative Approach to Meta-Analysis and Review of Animal Data from Experimental Studies – www.dcn.ed.ac.uk/camarades/) y SYRCLE (Systematic Review Center for Laboratory animal Experimentation – www.syrcle.nl).
3. Otras formas de síntesis de información emergentes
Existen otros formatos de revisión que utilizan métodos sistemáticos (reproducibles) para formular documentos que asisten a la toma de decisiones en salud:
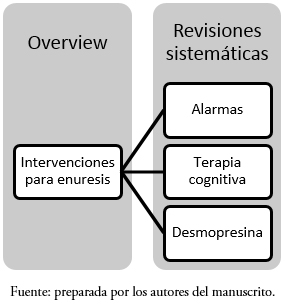
3.1. Umbrella Reviews (“revisiones paraguas”) u Overviews: son revisiones que compilan hallazgos de un grupo de revisiones sistemáticas. Habitualmente no siguen un formato PICO, sino que se abocan a un tópico más general, por ejemplo intervenciones para enuresis[29]. Esta umbrella review compila los datos de varias revisiones sistemáticas que abarcan distintas estrategias para el manejo de una condición (Figura 1).
 Tamaño completo
Tamaño completo 3.2 Scoping reviews (“revisiones panorámicas”): son revisiones que compilan la evidencia sobre una temática, generalmente con un alcance amplio, sin valoración crítica de la evidencia incluida[30]. Sin embargo, existe gran variabilidad en los métodos utilizados para realizarlas y éstos podrían ser flexibles[31].
3.3 Global Evidence Mapping (“mapeo de la evidencia”): es una herramienta que permite identificar los estudios o revisiones dentro de un determinado tópico, pero no realiza una síntesis de los hallazgos, sino que localiza la evidencia en preguntas individuales de una temática[32]. Es particularmente útil para identificar “vacíos en la evidencia” (“evidence gaps”) en los cuales no hay estudios que evalúen una determinada intervención[33] (Figura 2).
 Tamaño completo
Tamaño completo 3.4 Rapid reviews (“revisión rápida”): son similares a las revisiones sistemáticas en su estructura, no obstante, sus métodos son simplificados para lograr la formulación de un informe dentro de un periodo limitado de tiempo (habitualmente 10 a 12 semanas), a razón de asistir a la toma de decisiones[34].
3.5. Realist reviews (“revisiones realistas”): incorporan conceptos de investigación cualitativa, lo que comprende la complejidad de determinados fenómenos en salud (educación, comunicación y otras intervenciones complejas). Se enfocan en el componente contextual de las intervenciones y los mecanismos que llevan a un determinado resultado (contexto + mecanismo = resultado). Para construir este enfoque explicativo, estas revisiones utilizan un marco teórico de referencia para el análisis cualitativo[35].
Conclusiones
Existen distintos tipos de revisiones en salud. Las revisiones narrativas, que no usan métodos sistemáticos, suelen tener gran valor en la información sobre temáticas amplias o de background. Pueden proveer una mirada interpretativa y reflexiva sobre una determinada problemática nutriéndose de diversas fuentes bibliográficas. Por otro lado, las revisiones sistemáticas responden una pregunta focalizada mediante una metodología reproducible que intenta minimizar y transparentar sesgos en el cuerpo de la evidencia. Éstas y otras nuevas formas de revisión, junto a la información del contexto y del paciente, asisten al proceso de toma de decisiones en salud.
Notas
Rol de los autores
JF, EM, DS: conceptualización. JF y MA: escritura del manuscrito original. EM y DS: revisión y edición del manuscrito. MA: administración del proyecto. EM y MA: financiamiento de la publicación.
Conflictos de intereses
Los autores declaran no tener conflictos de interés.
Fuente de financiamiento
Este proyecto no contó con fuentes de financiamiento específicas. El costo de la publicación estuvo a cargo de la Universidad de Valparaíso. Las instituciones mencionadas en la filiaciones contribuyeron con el tiempo de trabajo de cada uno de los autores.
Aprobación ética
Este proyecto no requiere de revisión por comité de ética.

