Publicado el 1 de julio de 2008 | http://doi.org/10.5867/medwave.2008.06.500
Adaptaciones hemodinámicas y renales en el embarazo normal y patológico
Hemodynamic and renal adaptations in normal and pathological pregnancy
Resumen
Este texto completo es una transcripción editada y revisada de una conferencia que se dictó en el Congreso Conjunto de Nefrología, Hipertensión y Trasplante realizado en Pucón entre el 26 y el 29 de septiembre de 2007. El congreso fue organizado por las Sociedades Chilenas de Nefrología, Hipertensión y Trasplante. El presidente de la Sociedad Chilena de Nefrología fue el Dr. Alejandro Cotera, la secretaria ejecutiva fue la Dra. María Eugenia Sanhueza y la directora del curso precongreso fue la Dra. Gloria Valdés.
Introducción
A continuación se analizarán los cambios hemodinámicos y en función renal que ocurren en la gestación normal, y también las alteraciones hemodinámicas que se presentan en el embarazo patológico, así como el aporte de los trabajos con animales de experimentación a los avances en el conocimiento de estas materias.
En un estudio publicado en 1986, se observó que durante el embarazo normal el volumen plasmático aumenta en forma significativa. Estos hallazgos han sido corroborados en diversos estudios realizados en mujeres embarazadas y en animales de experimentación (Fig. 1).
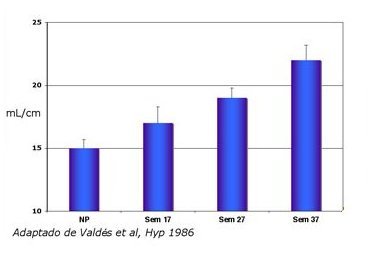 Tamaño completo
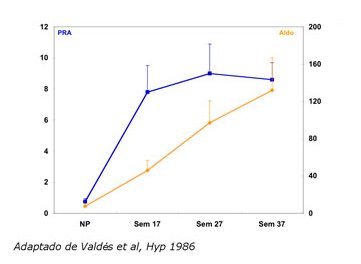
Tamaño completo Asimismo, hay importantes cambios hormonales: aumenta la actividad de renina plasmática alrededor de unas 8 veces, lo cual alcanza un plateau relativamente precoz, mientras que el incremento de aldosterona plasmática es porcentualmente mayor y es sostenido en el tiempo (Fig. 2).
 Tamaño completo
Tamaño completo También aumenta la calicreína urinaria, hecho que se observa en etapas precoces de la gestación humana, tendiendo a disminuir hacia el final de la gestación (Fig. 3).
Estudios hemodinámicos realizados por distintos autores en mujeres embarazadas confirman que el embarazo normal se caracteriza por disminución significativa de la presión arterial (PA), aumento del débito cardiaco y disminución de la resistencia vascular sistémica (RVS), cambios que se pueden detectar a partir de la sexta semana de gestación. Además, el volumen plasmático aumenta en forma relativamente precoz y también aumenta el volumen sanguíneo, sin grandes cambios en la masa de glóbulos rojos. Con respecto a la función renal, se produce un aumento importante de la velocidad de filtración glomerular y del flujo plasmático renal, con disminución de la resistencia vascular renal.
La rata tiene ventajas sobre otros modelos experimentales, porque presenta casi los mismos cambios hemodinámicos que se observan en la mujer, pero en un período corto de tiempo. En un trabajo publicado en 1998, se demostró que en este animal se produce un aumento sostenido del débito cardiaco hasta el final del embarazo, que dura tres semanas, con disminución significativa en la RVS (Fig. 4). Otros estudios en animales han demostrado que la curva de presión/natriuresis está disminuida durante el embarazo, lo que indica que hay retención importante de sodio, sin que haya cambios significativos en la PA.
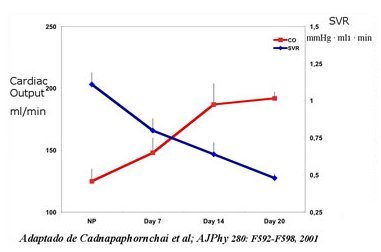 Tamaño completo
Tamaño completo En 1987, estudiamos el perfil temporal de los cambios hemodinámicos y de PA en la rata preñada, demostrando que si bien este modelo presenta varias similitudes con los eventos que ocurren en la mujer embarazada, se diferencia en que la disminución de la PA en la rata ocurre más bien al término de la gestación, coincidiendo con el aumento de la actividad de renina plasmática. Por otra parte, se observó un aumento precoz de la calicreína urinaria, lo que nos llevó a postular que el aumento de la renina plasmática es consecuencia de la gran vasodilatación sistémica asociada con el aumento de vasodilatadores.
Evidencias del aumento de la vía NO-NOS en la preñez
Diversas experiencias internacionales han demostrado que la calicreína no es el único vasodilatador que aumenta durante el embarazo y hay mucha evidencia sobre el aumento de la vía de la óxido nítrico sintetasa (NOS) en la gestación normal, tanto en humanos como en animales de experimentación. Este aumento del óxido nítrico cumpliría algún papel en los cambios hemodinámicos, tanto sistémicos como renales. La inhibición de la NOS durante el embarazo produce aumento de la PA, disminución del débito cardíaco, aumento de la RVS y cambios renales, donde la inhibición de la vía del óxido nítrico hace que la situación vuelva a ser la que se encuentra en la rata no preñada, es decir, se suprime el aumento de la velocidad de filtración glomerular y el aumento del flujo plasmático renal.
Para comprobar la hipótesis de que dichos cambios hormonales y sistémicos se deben a influencia materna o dependen de la unidad fetoplacentaria se utilizó el modelo de pseudo preñez en ratas, en el cual se cruza a la hembra con un macho vasectomizado. Ese coito no fecundante desencadena una serie de estímulos hormonales que remedan, alrededor de los 10-12 días, una gestación normal, hasta el punto de que la rata sube de peso, porque come como si estuviera preñada, a pesar de que no existe una unidad feto-placentaria. En el estudio se demostró que en la pseudo preñez se presentan muchos de los cambios hormonales propios de la gestación normal, como aumento de aldosterona, prostaciclina, calicreína e incluso de cGMP, el segundo mensajero del óxido nítrico.
En resumen: en la gestación normal, tanto en mujeres como en ratas, se producen importantes cambios hemodinámicos, que se traducen en menor RVS, menor PA, aumento del volumen y del débito cardíaco, además de cambios renales y hormonales, todos ellos independientes de la unidad feto-placentaria ya que también están presentes en el modelo de pseudo preñez.
Relación entre cambios hemodinámicos y crecimiento fetal
Cuando la demanda de nutrientes excede el aporte al feto se produce desnutrición fetal, la que puede ser causada por insuficiencia en la dieta materna, disminución del flujo sanguíneo útero-placentario, alteración de la transferencia placentaria o alteraciones del genoma fetal, entre otras etiologías. Los estudios al respecto sugieren que el factor principal es el cambio en el flujo sanguíneo útero-placentario, tal vez influenciado por cambios en la dieta materna, lo que traería como consecuencia alteraciones en la transferencia placentaria de nutrientes.
La distribución del débito cardíaco en la embarazada se caracteriza por un incremento importante del flujo hacia el territorio útero-placentario, por lo que era lógico suponer que las alteraciones en el débito cardíaco deberían estar correlacionadas con el crecimiento fetal. Los estudios iniciales al respecto, efectuados en embarazadas normotensas y normopeso, portadoras de fetos con restricción de crecimiento fetal (RCF) entregaron las primeras evidencias de que en este estado disminuye el volumen plasmático y el débito cardíaco y aumenta significativamente la resistencia vascular sistémica (Fig. 5).
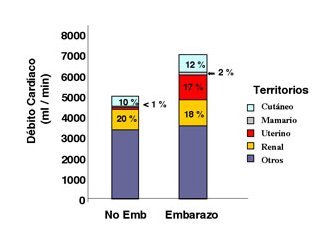 Tamaño completo
Tamaño completo Para determinar si el menor volumen plasmático que se observa al término de la gestación se debe a menor expansión del volumen durante este proceso o a menor volumen previo al embarazo, se estudió a un grupo de mujeres embarazadas en el tercer trimestre y se comprobó que aquellas que tenían restricción del crecimiento fetal tenían menor volumen plasmático que las del grupo control; luego se midió este volumen en el postparto alejado y se demostró que era idéntico en ambos grupos. Se concluyó que cuando existe restricción fetal hay menor expansión del volumen plasmático que en embarazos normales (Fig. 6).
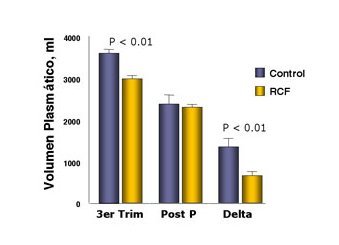 Tamaño completo
Tamaño completo Luego se planteó que entre los posibles mecanismos involucrados en esta menor expansión del volumen plasmático podría estar una menor vasodilatación, secundaria a alteraciones en algunas hormonas vasoactivas. Para comprobar esta hipótesis, se determinó el nivel de aldosterona, calicreína, hormonas sexuales y GMPc, con el fin de precisar el balance que existe entre hormonas vasodilatadoras y vasocontrictoras durante el embarazo. Se observó que en las embarazadas con restricción del crecimiento fetal había disminución de la actividad de renina plasmática y de aldosterona y disminución de la actividad de calicreína urinaria (Fig. 7). También se comprobó disminución de prostaciclina y tromboxano, pero con un desequilibrio a favor de este último (Fig. 8).
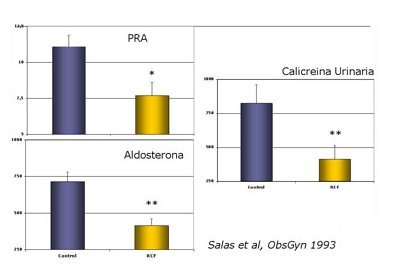 Tamaño completo
Tamaño completo 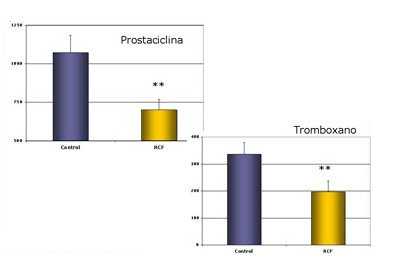 Tamaño completo
Tamaño completo Puesto que los resultados observados en restricción del crecimiento fetal son similares a las alteraciones descritas en la preeclampsia, se planteó que la restricción del crecimiento fetal de causa desconocida y la preeclampsia podrían compartir algunos mecanismos. Para comprobar esto se estudió a tres grupos de embarazadas en tercer trimestre: con restricción del crecimiento fetal, con preeclampsia y grupo control y se demostró que los dos primeros tenían menor expansión del volumen plasmático y disminución de renina, aldosterona y calicreína (Tabla I).
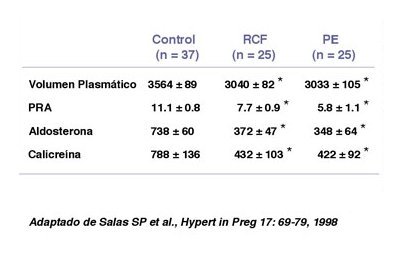 Tamaño completo
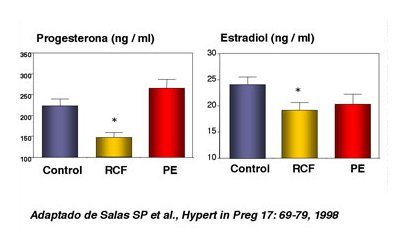
Tamaño completo Las embarazadas con restricción del crecimiento fetal tenían niveles disminuidos de progesterona, mientras que las mujeres preeclámpticas tenían niveles mayores que los del grupo control. El estradiol estaba disminuido en las embarazadas con restricción del crecimiento fetal (Fig. 9).
 Tamaño completo
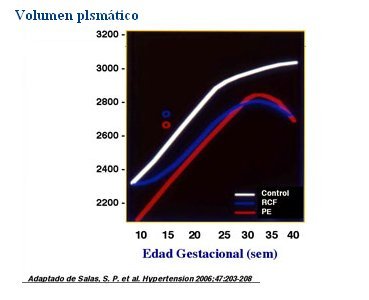
Tamaño completo En otros trabajos se había demostrado que el ARNm del receptor de progesterona está aumentado en las placentas de las mujeres con preeclampsia y que existe predominancia funcional de la progesterona sobre el estrógeno en esta patología, lo que se podría relacionar con un aumento de la reactividad vascular. Sobre esta base se elaboró una hipótesis de trabajo, en la que se consideró que lo central era el daño endotelial; la isquemia placentaria también sería importante y podría desempeñar un papel en provocar este daño. Para comprobar esta serie de episodios, dispuestos en forma de círculo vicioso, era preciso entender el perfil temporal de los cambios. Con tal propósito se hizo un seguimiento secuencial de mujeres embarazadas a partir de la semana 10 de embarazo, las cuales formaron tres grupos: mujeres que desarrollaron preeclampsia; mujeres con restricción del crecimiento fetal y presión arterial normal; y mujeres0cuyos niños tenían peso adecuado para la edad gestacional, pero bajo para la talla, lo que hizo suponer que no estaban expresando todo su potencial de crecimiento. El trabajo fue largo y complejo y no fue fácil lograr un número elevado de pacientes, pero finalmente se demostró que en las embarazadas con restricción del crecimiento fetal y con preeclampsia, la expansión de volumen plasmático es menor y su comienzo es relativamente precoz, alrededor de la semana 17 de gestación, (Fig. 10).
 Tamaño completo
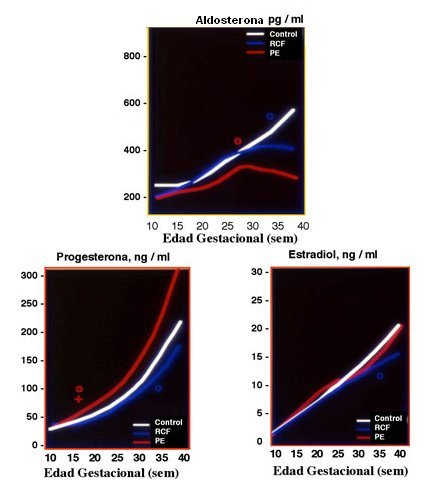
Tamaño completo Las alteraciones de la aldosterona en las mujeres preeclámpticas y en las mujeres con restricción del crecimiento fetal son posteriores a la alteración del volumen plasmático y, en cuanto a los cambios hormonales, la embarazada con preeclampsia presenta aumento de progesterona alrededor de la semana 17, mientras que la embarazada con restricción del crecimiento fetal muestra disminución más bien al término. El estradiol, en cambio, no se modifica en las mujeres con PE y disminuye al término en aquéllas con RCF (Fig. 11).
 Tamaño completo
Tamaño completo Con respecto al curso temporal de los cambios, se demostró que el evento más precoz es la menor expansión del volumen plasmático, el cual antecede a algunos de los factores que antes se pensaba que eran responsables de la menor expansión del volumen. Seguía en pie la tesis de que la disminución de la síntesis de óxido nítrico o de calicreína, o ambos, si predominaban a nivel local, producirían aumento de la resistencia vascular uterina, y si predominaban a nivel sistémico conducían a aumento de la RVS. La traducción clínica de este último fenómeno sería la preeclampsia, mientras que los cambios locales se expresarían como disminución del crecimiento fetal. Lo anterior pondría en marcha una serie de otras alteraciones y, por lo tanto, el eje central de ambas patologías podría ser una disminución de vasodilatadores.
Para demostrar esto, se trabajó con modelos de ratas preñadas y no preñadas, controles y experimentales, a las que, en distintas épocas, se administró un precursor de serotonina, un importante vasocontrictor. También se utilizaron modelos de deshidratación materna, de restricción del flujo útero-placentario mediante un clip mecánico, de inhibición de la síntesis de óxido nítrico, de desnutrición materna, de diabetes materna y de insuficiencia renal crónica, por nefrectomía 5/6. Los objetivos de estos estudios eran: probar la hipótesis de que el riñón es un órgano fundamental para los cambios hemodinámicos propios de la gestación, por lo tanto se esperaba que la nefrectomía 5/6 afectara significativamente la expansión del volumen plasmático; probar que la deprivación acuosa alteraría los mecanismos de ajuste hemodinámico del embarazo y que la rata preñada sería más sensible a la deprivación acuosa que aquella no preñada, además de causar CRF; y probar la hipótesis de que la serotonina, amina vasoactiva, pudiera participar en algunas de las alteraciones de la preeclampsia y en la restricción del crecimiento fetal.
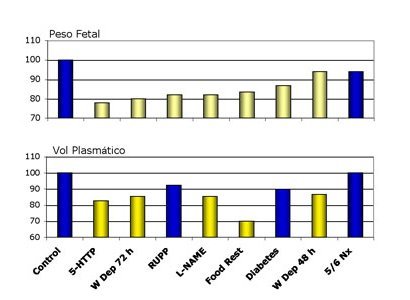
Estos trabajos se realizaron a lo largo de varios años, por lo que, en lugar de valores absolutos, cada uno de los modelos se relaciona con el cambio porcentual de su propio control. Todos los protocolos mencionados, salvo el de nefrectomía 5/6, se caracterizan por menor crecimiento fetal. En relación con el volumen plasmático, varios de los modelos: serotonina, deprivación acuosa, administración de óxido nítrico y restricción de alimentos maternos, muestran una disminución significativa del volumen plasmático; sin embargo, si bien en todas las situaciones en que hay menor volumen plasmático hay menor crecimiento fetal, no ocurre lo mismo en el sentido inverso (Fig. 12).
 Tamaño completo
Tamaño completo En cuanto a la actividad de renina plasmática, en algunos modelos ésta estaba aumentada; como era esperable, la privación acuosa aumentó los niveles de renina varias veces sobre los valores de la gestación normal, que ya están aumentados. En los modelos de restricción del flujo útero-placentario, inhibición de la síntesis de óxido nítrico y nefrectomía 5/6 los niveles de renina estuvieron significativamente disminuidos con respecto al control. En cuanto a la calicreína, en ciertas situaciones se mantuvo igual al grupo control, aun cuando la renina estaba disminuida; en otros modelos la calicreína estaba disminuida y la renina, aumentada; algunos de los modelos que cursaron con renina disminuida y calicreína normal, cursaron con hipertensión. En presencia de renina y calicreína bajas, siempre hubo hipertensión (Fig. 13).
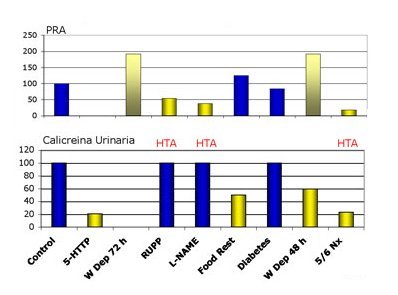 Tamaño completo
Tamaño completo
Conclusiones
- La suma de los resultados de todos estos modelos experimentales confirma que la menor expansión de volumen plasmático se asocia con restricción del crecimiento fetal.
- Sin embargo, no toda restricción del crecimiento fetal cursa con menor volumen materno, ya que esto dependerá de los mecanismos participantes.
- Los resultados sugieren que el menor volumen plasmático sería independiente de los cambios de renina y calicreína.
- En muchos de estos modelos, que presentan importantes alteraciones en renina o calicreína, se logra observar la vasodilatación propia de la gestación normal, incluso en situaciones de calicreína disminuida.
- No todo daño renal, como lo demuestra el modelo de nefrectomía 5/6, en que hay disminución significativa de la función renal, limita la expansión del volumen plasmático en la rata preñada, es decir, ésta desencadena mecanismos hemodinámicos compensatorios que garantizan un adecuado crecimiento fetal, a pesar del daño renal.
En la actualidad se ha iniciado un nuevo estudio, dirigido a determinar cuál es el evento que desencadena esta serie de cambios hemodinámicos, aunque los mecanismos de ajuste que dispone el reino animal para asegurar su preservación son tan numerosos, que probablemente no existe un único episodio iniciador. La investigación se centra en las consecuencias a largo plazo de las alteraciones fetales causadas por la hipoxia intrauterina y la restricción del crecimiento fetal.

