Congresos
← vista completaPublicado el 1 de abril de 2008 | http://doi.org/10.5867/medwave.2008.03.901
Búsqueda de biomarcadores y nuevas estrategias terapéuticas en EPOC
Search for biomarkers and new therapeutic strategies in COPD
Resumen
Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del Congreso de Enfermedades Respiratorias 2007, realizado en Pucón los días 7 al 10 de noviembre de 2007. El evento fue organizado por la Sociedad Chilena de Enfermedades Respiratorias.
Presidente Sociedad Chilena de Enfermedades Respiratorias: Dr. Raúl Corrales.
Biomarcadores en EPOC
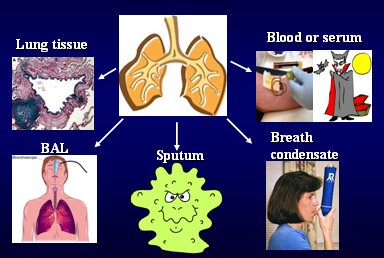
Los resultados del estudio TORCH han llevado a plantear la necesidad de desarrollar nuevas estrategias para el manejo de los pacientes con EPOC. En este contexto se ha iniciado la búsqueda de biomarcadores, con el objetivo de encontrar una señal característica de la enfermedad, que se pueda medir antes y después de una intervención terapéutica y, de esta forma, determinar en forma objetiva el resultado de ésta.El Instituto Nacional de Salud (NIH) de los Estados Unidos define el concepto de biomarcador como “una característica que se puede medir en forma objetiva y que permite evaluar un proceso biológico normal, un proceso patogénico o una respuesta farmacológica a intervenciones terapéuticas”. Existen diferentes posibilidades para obtener biomarcadores desde el pulmón de pacientes con EPOC: biopsia pulmonar; lavado broncoalveolar; análisis del esputo; condensado respiratorio; y mediciones en plasma o sangre periférica (Fig. 1).
 Tamaño completo
Tamaño completo Figura 1. Biomarcadores: ¿Dónde?
El condensado es una técnica en la cual se hace respirar al paciente dentro de un tubo plástico congelado a -70º: el paciente inhala y exhala una y otra vez y el aire exhalado se congela y se deposita en la parte inferior, desde donde se retira para ser analizado; por otra parte, los análisis en sangre tienen la ventaja de que se pueden hacer en forma repetida. Barnes publicó una revisión sobre la utilidad de diversos biomarcadores presentes en esputo, condensado y lavado broncoalveolar y concluyó que ninguno de ellos se usa en forma rutinaria y que se necesita más investigación, con buena fenotipificación.
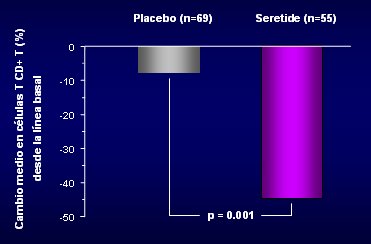
En cuanto al tejido pulmonar, Barnes publicó, en 2006, un estudio en que utilizó la biopsia pulmonar como un biomarcador, porque se efectuó al inicio y a las 16 semanas en cada paciente, para determinar los cambios que se producían en distintas subpoblaciones de linfocitos T CD+ con el uso de Seretide®, comparado con placebo. En dicho estudio se comprobó que la terapia producía una disminución marcada de estas células a nivel tisular (Fig. 2).
 Tamaño completo
Tamaño completo Figura 2. Efecto de Salmeterol/Fluticasona sobre la inflamación bronquial en EPOC
Sin embargo, esto no dice nada acerca del efecto en la evolución clínica de los pacientes o su tasa de mortalidad; de hecho, en el TORCH, los pacientes que recibieron Fluticasona sola no tuvieron mayor sobrevida y tuvieron mayor incidencia de neumonía. El hecho de que se observe un efecto sobre éstas células no significa que eso mejore la evolución de la enfermedad.
Biomarcadores genéticos en tejido
El estudio de los genes involucrados en el desarrollo de las enfermedades, que es un campo fértil para la búsqueda de biomarcadores, está más avanzado en patologías como el cáncer. En la Fig. 3 se muestran los resultados de un estudio efectuado en una cohorte de 63 pacientes portadores de cáncer pulmonar de células pequeñas (NSCLC). Cada carril horizontal es un gen y cada uno de los puntos representa a un paciente; los genes que están “regulados hacia arriba” (up regulated), es decir, sobre-regulados o sobre-expresados, aparecen en rojo y los genes sub-expresados, en azul. Los genes que están sobre-expresados en los pacientes portadores de la enfermedad se denominan genes de riesgo y los que están sub-expresados son los genes protectores. Los autores encontraron 16 genes correlacionados con la supervivencia y seleccionaron 5 de ellos para predecir el resultado de los pacientes; posteriormente validaron estos resultados en otros 60 pacientes.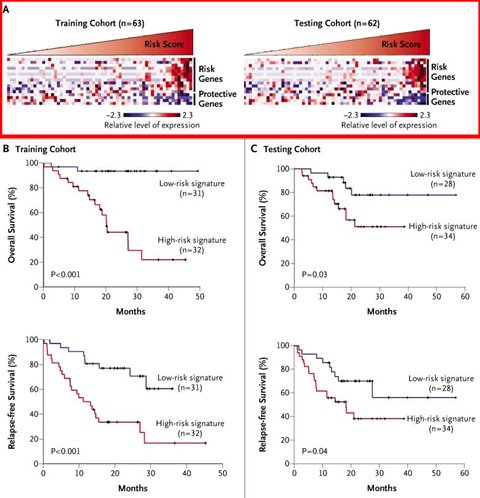 Tamaño completo
Tamaño completo Figura 3. Marcadores genéticos y resultados en pacientes con cáncer pulmonar de células pequeñas
Posteriormente estos autores publicaron un trabajo en el que demostraron que el patrón genético determina la respuesta a la quimioterapia.
En la EPOC no se ha logrado el mismo nivel de desarrollo, en cuanto a marcadores genéticos, que en el cáncer. En un trabajo del Pulmonary Center and Department of Medicine, Boston University School of Medicine, encabezado por Spira, en conjunto con nuestro grupo, se estudió tejido pulmonar de pacientes con enfisema grave, que se obtuvo por cirugía de reducción de volumen, y de pacientes con enfisema leve, que se extrajo de pacientes portadores de nódulos o cáncer y se encontró el mismo patrón de genes sobre-regulados y genes sub-regulados, con predominio de los primeros en los pacientes con enfisema grave (Fig. 4).
 Tamaño completo
Tamaño completo Figura 4. Patrón genético según gravedad del enfisema pulmonar.
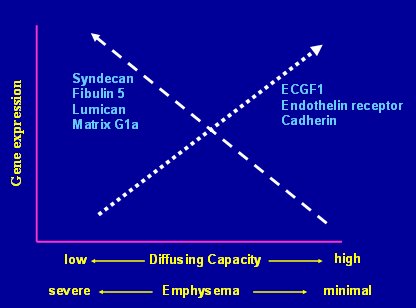
Esto no es suficiente si se correlaciona con una función. En el gráfico de la Fig. 5, a la izquierda están los genes que se asocian con baja capacidad de difusión y, por lo tanto, con enfisema grave y a la derecha, los que se asocian con alta capacidad de difusión y, por lo tanto, con enfisema mínimo.
 Tamaño completo
Tamaño completo Figura 5. Expresión genética y capacidad de difusión en pacientes con enfisema pulmonar
Esto significa que es posible predecir el resultado de un paciente con enfisema mediante el estudio de su tejido pulmonar; sin embargo, todavía no se ha llegado al nivel de los oncólogos, en el sentido de encontrar intervenciones que reviertan el deterioro de la capacidad de difusión en los pacientes con enfisema grave. Esto se debe, en gran medida, a que no es posible extraer tejido pulmonar en forma seriada para hacer los estudios: tal como dicen los americanos, “tissue is the issue”, el tejido es el problema.
Biomarcadores en sangre
El único órgano que se encuentra bañado por la sangre en forma continua es el pulmón; de modo que es lógico pensar en la posibilidad de encontrar marcadores en ésta. Uno de estos posibles marcadores es la Proteína C Reactiva (PCR), que es ampliamente utilizada en reumatología, infectología y cardiología. Sin and Man analizó tres estudios sobre la relación entre los niveles de PCR y VEF1 promedio (% del predicho) y encontró una correlación de 0,95 entre ambos parámetros: a mayor obstrucción, mayor nivel de PCR, lo que no indica causa y efecto, pero es sugerente.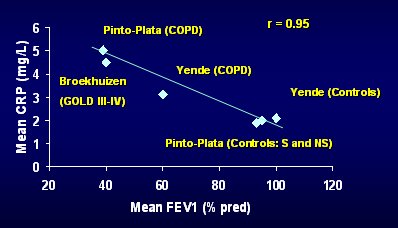 Tamaño completo
Tamaño completo Figura 6. Inflamación, Proteína C Reactiva y EPOC
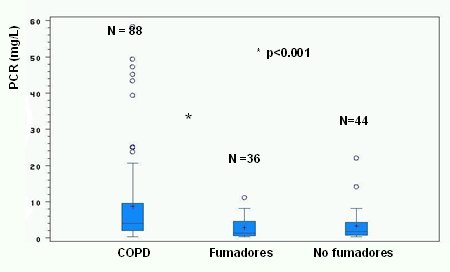
En el estudio de nuestro grupo se hizo dos mediciones de PCR, separadas por un año, en 88 pacientes con EPOC, 36 fumadores sin EPOC y 44 no fumadores, y se encontró un aumento significativo de la PCR en el primer grupo (Fig. 7).
 Tamaño completo
Tamaño completo Figura 7. Proteína C Reactiva en pacientes con EPOC y en controles
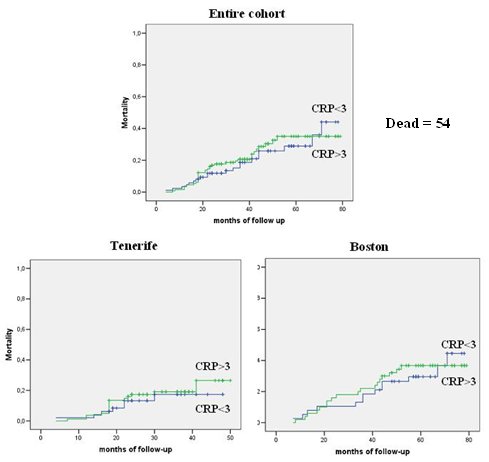
En un estudio poblacional, cuyos resultados se publicaron en 2007, se hizo un seguimiento a 1.302 pacientes durante ocho años; en ese lapso, 14% de los pacientes requirió hospitalización y 6% falleció. Los autores encontraron que, ajustando por edad, VEF1, tabaquismo y enfermedad coronaria, la PCR predice la mortalidad por problemas respiratorios, ya que el hazard ratio (HC) fue 40% más alto en personas con PCR mayor de 3, que en personas con PCR igual o menor de 3. Sin embargo, en los estudios de nuestro grupo, en Boston, del grupo de Tenerife y de la cohorte total, que suma 218 pacientes, la PCR no predijo la mortalidad. Es probable que se necesiten 2000 pacientes para encontrar cambios significativos en la PCR, de modo que es probable que este parámetro no sea útil para los neumólogos (Fig. 8).
 Tamaño completo
Tamaño completo Figura 8. PCR como predictor de mortalidad en EPOC (n = 218)
Terapia dirigida a marcadores de EPOC
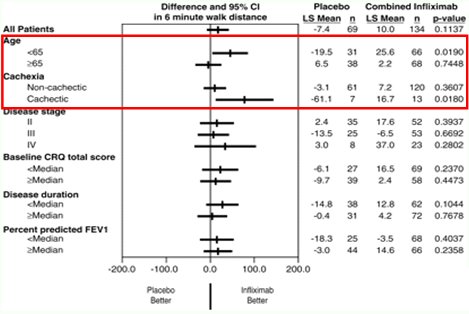
Se han utilizado anticuerpos monoclonales contra marcadores específicos en pacientes con EPOC. Mahler publicó, en 2004, un estudio sobre anticuerpos monoclonales contra interleuquina 8 (IL-8), en el que no se encontraron diferencias significativas en pruebas funcionales pulmonares, calidad de vida, caminata de 6 minutos o efectos colaterales en pacientes con EPOC tratados y no tratados. En otro estudio se analizó el efecto de Infliximab, un anticuerpo contra factor de necrosis tumoral alfa (TNF alfa), sobre la calidad de vida de los pacientes, medida por CRQ (Chronic Respiratory Questionnaire), según edad, caquexia, CRQ basal, estadio de la enfermedad, duración de ésta y VEF1 (porcentaje del predicho) y no se encontró una mejoría significativa en ninguno de estos parámetros.De expuesto se podría concluir que los anticuerpos contra moléculas específicas no tienen utilidad en los pacientes con EPOC; sin embargo, hay que considerar que en los dos estudios descritos los pacientes se escogieron con base en el VEF, no porque tuvieran aumento del la IL- o del TNF alfa. De hecho, si se observan los resultados de la caminata en 6 minutos en el segundo estudio, que se muestran en la Fig. 9, en los pacientes menores de 65 años y con caquexia sí hubo mejoría (recuadro rojo). Por lo tanto, es posible que en este tipo de pacientes el TN alfa se encuentre elevado y éste sea el grupo específico que se va a beneficiar con este tipo de tratamiento.
 Tamaño completo
Tamaño completo Figura 9. Infliximab (anticuerpo anti TNF alfa) en EPOC
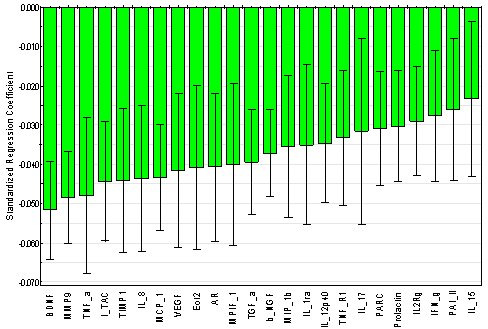
Sir William Osler (1849-1919), un gran clínico en John Hopkins, es el autor de una sabia sentencia: “Si no fuera por la gran variabilidad entre los individuos, la Medicina podría ser una ciencia y no, como lo es, un arte”. En efecto, aunque los individuos compartan un porcentaje muy alto de los genes, ninguno es exactamente igual a otro. Pensando en esto se planteó la posibilidad de utilizar un “panel” de biomarcadores. En un estudio de nuestro grupo, que se acaba de publicar, se utilizó una técnica de análisis proteómico en suero para determinar la asociación entre diversos marcadores sospechosos de estar involucrados en la patogenia de la EPOC y el VEF1; y se encontró un grupo de proteínas relacionadas con menor VEF-1 (Fig. 10).
 Tamaño completo
Tamaño completo Figura 10. Asociación de marcadores con VEF-1 (análisis proteómico del suero). Análisis de regresión parcial de cuadrados mínimos
La exacerbación como modelo
Con la hipótesis de que la exacerbación, definida por la presencia de tos, expectoración y disnea, debería tener una expresión citoquímica, nuestro grupo hizo un estudio sobre citoquinas sistémicas, cambios fisiológicos y clínicos en pacientes hospitalizados por exacerbación de la EPOC. Se midió la disnea, utilizando la escala analógica visual y se determinó la función pulmonar, el hemograma y los niveles plasmáticos de IL-6, IL-8, leucotrieno B4 (LTB4), TNF e inhibidor de la proteasa secretora de leucocitos (SLPI) en 20 pacientes que ingresaron a un hospital por exacerbación de la EPOC, 48 horas después y 8 semanas después del alta hospitalaria. Se encontró una correlación significativa entre los cambios en IL-6, IL-8 y LTB4 y los cambios en el VEF1. Esto no necesariamente implica una relación causa-efecto, pero sugiere esa posibilidad. Siguiendo esta línea, Hurst utilizó el mismo panel y demostró que varias proteínas, entre ellas la PCR, pueden ser útiles para medir durante la exacerbación y determinar si se pueden modificar con el tratamiento (Fig. 11).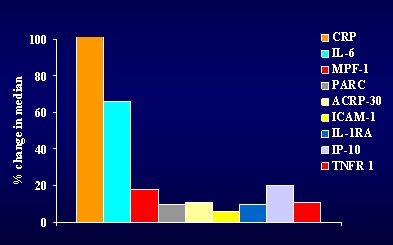 Tamaño completo
Tamaño completo Figura 11. Panel plasmático de biomarcadores en exacerbaciones de EPOC
Lecciones de la experiencia cardiológica
Wang publicó un estudio en que se hizo seguimiento, durante un lapso de 7,4 años, a 3.209 pacientes en los que se determinaron los siguientes marcadores convencionales: edad, sexo, presión arterial, colesterol, tabaquismo, índice de masa corporal y uso de medicamentos, como estatinas o antihipertensivos; y los siguientes biomarcadores, cuya asociación con mortalidad se había demostrado previamente: PCR, péptido natriurético (BNP, B-type natriuretic peptide), Nap-homocisteína, aldosterona, renina, dimero D, proteínas en la orina, PAI -1 y fibrinógeno, con el objetivo de establecer cuál de los dos grupos de marcadores es mejor para predecir la mortalidad, mediante el análisis de las curvas ROC (Receiver Operating Characteristics). Se encontró que las curvas eran muy parecidas, es decir, la medición de biomarcadores, según los resultados de este estudio, no tiene mayor utilidad que los marcadores convencionales para predecir la mortalidad (Fig. 12).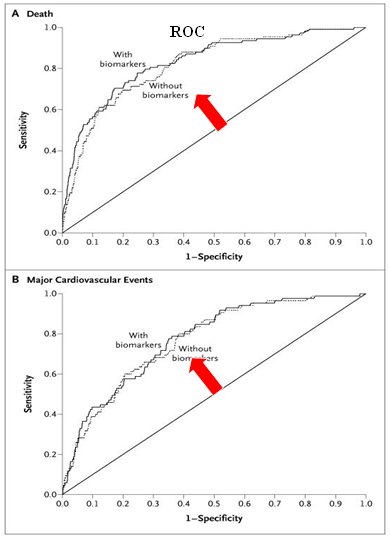 Tamaño completo
Tamaño completo Figura 12. Biomarcadores y resultados en pacientes con EPOC
Esto no quiere decir que los biomarcadores no tengan utilidad en el área de la farmacoterapia y, por otra parte, el colesterol se debió considerar en el grupo de los biomarcadores, y se sabe que si se modifica el colesterol, cambia el pronóstico. Si los neumólogos pudieran encontrar un equivalente al colesterol, quizás podrían desarrollar “las estatinas” de la EPOC.
Conclusiones
- El descubrimiento de biomarcadores es un proceso complejo y difícil, a causa de múltiples problemas técnicos y “ruidos biológicos”.
- Los pacientes con EPOC deben ser fenotipificados para así poder determinar la relación con biomarcadores; el gran error de los neumólogos ha sido quedarse sólo con la espirometría.
- El estudio Eclipse (Evaluation of COPD Longitudinally to Identify Predictive Surrogate Endpoints) puede ofrecer esperanzas. Financiado por GLAXO, incluye a 3.000 personas, 2.000 con EPOC y 1.000 sin EPOC en las que se está evaluando biomarcadores en sangre, condensado y tomografía computada.
- La exacerbación es un buen modelo para evaluar los biomarcadores.

