Congresos
← vista completaPublicado el 1 de agosto de 2002 | http://doi.org/10.5867/medwave.2002.07.3608
Radicales libres y antioxidantes en salud humana
Free radicals and antioxidants in human health
Resumen
Este texto completo es la transcripción editada y revisada de una conferencia dictada en el Simposio Internacional "Dietas Mediterráneas", realizado los días 26 y 27 de octubre de 2001.
Organizan: Proyecto Ciencia, Vino y Salud, Programa Bases Moleculares de las Enfermedades Crónicas, Facultad de Ciencias Biológicas, Pontificia Universidad Católica de Chile. Editor Científico: Dr. Federico Leighton.
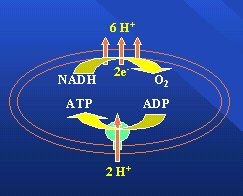
Los seres humanos son máquinas químicas que utilizan la energía de la oxidación de los alimentos, funcionan a presión y temperatura constantes y obtienen una cantidad más o menos precisa y conocida de energía por cada mol de oxígeno utilizado. Este proceso ocurre en las mitocondrias, que generan ATP mediante un mecanismo por cuyo descubrimiento Peter Mitchell, en 1978, recibió el Premio Nobel. Consiste en un bombeo de protones que al volver a la matriz mitocondrial generan ATP (Figura 1).
 Tamaño completo
Tamaño completo Figura 1.
Los alimentos son la base para la obtención de la energía, y con ésta los seres humanos viven y se mueven. Todo esto gracias a la respiración y la reducción del oxígeno. Se podría pensar en la respiración como la producción de anhídrido carbónico, como la reducción del oxígeno o como la oxidación de los alimentos y daría lo mismo, pero nosotros preferimos referirnos a ella como la reducción del oxígeno.
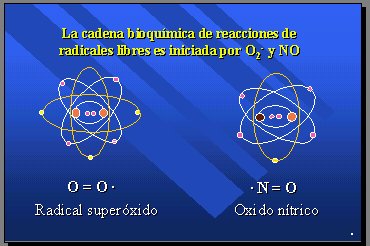
Cuando se efectúa la reducción del oxígeno en la respiración celular, a nivel de las mitocondrias, se producen en forma secundaria dos radicales libres: el radical superóxido (O2-) y el óxido nítrico (NO) a los que corresponden 2% y 1% del consumo de oxígeno, respectivamente. El radical superóxido deriva de la autooxidación no enzimática de biomoléculas y se produce a partir de oxígeno, y de algo que se oxida. El óxido nítrico proviene de la reducción enzimática del oxígeno realizada por la óxido nítricosintetasa (Figura 2).
 Tamaño completo
Tamaño completo Figura 2.
Estos dos radicales libres son similares; la única diferencia la da un orbital. Ambos tienen un electrón no apareado y son capaces de producir una serie de reacciones que llevan, en primera instancia, a la producción de radical hidroxilo y luego a la cadena de reacciones de radicales libres llamada lipoperoxidación, conocida desde 1950, causante de la lipoperoxidación de los alimentos. El hecho de que los alimentos se pongan rancios y produzcan lipoperóxido se conoce desde 1930.
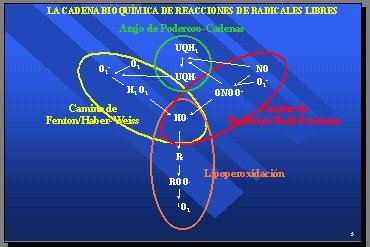
Dentro de la cadena bioquímica de reacciones de radicales libres, el camino que lleva de superóxido a hidroxilo se denomina camino de Fenton/Haber-Weiss y durante 15 años se consideró el camino rector de todas las reacciones de radicales libres. Sin embargo, en los cinco últimos años surgió la idea de que el óxido nítrico, al reaccionar con el superóxido, podía producir peroxinitrito y luego hidroxilo y constituir un segundo camino para llegar al hidroxilo, denominado camino de Beckman-Radi-Freeman. También hay un atajo que permite pasar de uno al otro. Por tanto, hay dos caminos: uno se inicia con superóxido y el otro con óxido nítrico, y ambos llevan a la producción del radical hidroxilo (Figura 3).
 Tamaño completo
Tamaño completo Figura 3.
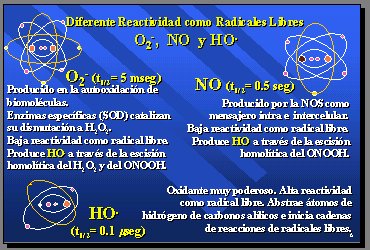
Estos radicales tienen diferente reactividad, como radicales libres, y eso se ve al comparar las vidas medias (t½):
- El superóxido dura 5 milisegundos.
- El óxido nítrico vive 0,5 seg.
- El hidroxilo vive 0,1 microsegundos. Este es el causante de la gran mayoría de las acciones o efectos biológicos y todo lo que se entiende como acciones tóxicas. El superóxido y el óxido nítrico son poco reactivos, y en realidad dan reacciones de radicales libres por medio de la generación del hidroxilo (Figura 4).
 Tamaño completo
Tamaño completo Figura 4.
Todas esas reacciones de radicales libres ocurren en el organismo humano, pero las investigaciones desarrolladas en los últimos años han permitido diferenciar la existencia de tres compartimientos separados, cada uno con sus reglas frente a estas reacciones generales, porque las concentraciones de los reactantes y del oxígeno son distintas. Ellos son: el espacio intracelular, en el que las reacciones son principalmente mitocondriales; el espacio vascular; y el lumen intestinal, que en la práctica puede considerarse como un medio externo virtual, según la concepción de los límites del cuerpo humano (Figura 5).
 Tamaño completo
Tamaño completo Figura 5.
Es importante conocer el efecto de los antioxidantes en los tres compartimientos, para comprender cómo los flavonoides y los antioxidantes de la dieta mediterránea influyen en la salud humana, mediante el mecanismo de la antioxidación, frenando las reacciones de radicales libres, que se sabe que son dañinas.
Compartimiento intracelular
La producción mitocondrial de anión superóxido ocurre en todas las células aeróbicas. A esta producción corresponde 2% del consumo de oxígeno, en el corazón e hígado de la rata, que es el mejor modelo (se perfunden corazones e hígados, se determina cuánto consumen y de ahí se aíslan las mitocondrias para así calcular este 2%). Esa producción mitocondrial de anión superóxido es alta, en los estados mitocondriales de reposo como el estado 4, y disminuye en el estado 3, que corresponde a actividad física, actividad muscular o frecuencia cardíaca aumentada.
Lo más espectacular es que hay una mangano superóxido dismutasa (Mn-SOD) específica en la matriz mitocondrial. Esto convence rápidamente a todas las personas que tienen formación biológica, de que hay formación de superóxido en la matriz mitocondrial, gracias a la presencia de esta dismutasa.
La producción mitocondrial de radicales superóxido se hace mediante dos reacciones fundamentales. Una de ellas es la oxidación del ubiquinol (UQ), que nosotros llamamos “reacción de Boveris-Cadenas” (aunque en general esto no se reconoce), la que se puede considerar como el marcapaso del envejecimiento, porque es la producción más alta del organismo según nuestras determinaciones (1). La otra es la autooxidación de la flavina por la FMNH deshidrogenasa, que puede ser relevante en la neurodegeneración, porque esa flavina es la misma que se destruye en la enfermedad de Parkinson, aunque esto aún es especulativo (2) (Figura 6).
 Tamaño completo
Tamaño completo Figura 6.
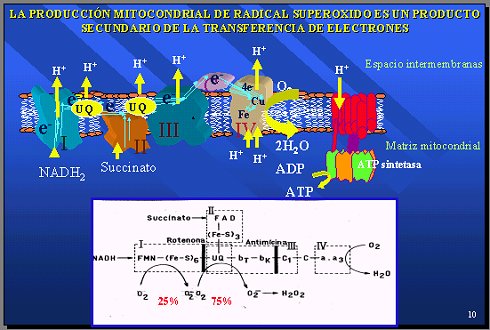
La producción mitocondrial de radical superóxido es un producto secundario de la transferencia de electrones. En la cadena respiratoria hay muchos movimientos y transferencias de electrones por todos lados, y hay algunos puntos donde el oxígeno puede reaccionar con UQ para producir superóxido. En medio de centenares de reacciones, hay algunas que producen significativamente superóxido, pero siempre es un producto secundario y la mayor parte de los electrones llegan al oxígeno para producir energía por medio del consumo de oxígeno por la citocromo oxidasa (Figura 7).
 Tamaño completo
Tamaño completo Figura 7.
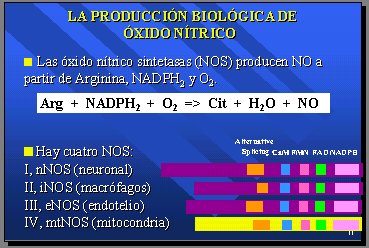
Esto era lo que se sabía acerca de la producción del superóxido, hasta que en 1990 se descubrió la producción biológica del óxido nítrico mediante las óxido nítrico sintetasas (NOS), que producen óxido nítrico a partir de arginina, NADPH2 y oxígeno molecular (O2), y que tiene tres formas clásicas, cada una con su propia enzima: la neuronal (nNOS), la de los macrófagos (iNOS) y la del endotelio (eNOS), que están totalmente secuenciadas. En 1998 apareció la cuarta vía, que muchos no creen que exista y piensan que realmente es contaminación, y que corresponde a la vía mitocondrial descrita por nuestro grupo de trabajo (con la mtNOS) (Figura 8).
 Tamaño completo
Tamaño completo Figura 8.
Producción mitocondrial de óxido nítrico
En las mitocondrias hay una oxido nítrico sintetasa mitocondrial (mtNOS) que está en el lado interno de la matriz mitocondrial. Su actividad fue reconocida originalmente en mitocondrias de hígado por un grupo en Suiza y luego en Los Angeles, y actualmente está determinada en cerebro, corazón, riñón y músculo.
A la producción de NO corresponde 0,5 % del consumo de oxígeno de los órganos. La mtNOS utiliza NADPH2, arginina y Ca2+ de la matriz mitocondrial, es decir, todos los cofactores que utilizan la otras NOS y sus Km para O2 están entre 18 y 80 micromolar, a diferencia de las otras, que están normalmente en el orden de 15 a 20 micromolar.
O2-, NO y ONOO- en la regulación, patología y envejecimiento mitocondrial
Se sabe que en las células hay dos fuentes de radicales libres en las mitocondrias, que por un lado producen anión superóxido (O2-) y por el otro, óxido nítrico (NO).
El O2- se produce en la autooxidación de componentes de la cadena respiratoria, en una reacción secundaria de ésta, y la mayor parte dismuta a peróxido de hidrógeno (H2O2) debido a la presencia de la Mn SOD.
Muy cerca de ahí, también en las mitocondrias, se produce el NO por acción de la mtNOS que actúa como regulador de la respiración. El NO se convierte mayormente en peroxinitrito (ONOO-).
El O2- y el NO reaccionan y producen, dentro de la matriz mitocondrial, ONOO-, un potente oxidante que normalmente se reduce por acción de los reductores mitocondriales como NADH2, ubiquinol (UQH2 ) y glutatión (GSH). Cuando se produce en exceso, porque se pierde su control (por ejemplo, en isquemia/reperfusión o inflamación), produce nitración de tirosinas y disfunción mitocondrial. Su efecto acumulativo contribuiría al envejecimiento tisular.
Antioxidantes del espacio intracelular
Los clásicos antioxidantes del espacio intracelular, que también lo son del espacio mitocondrial, se agrupan como sigue:
- Antioxidantes enzimáticos: la superoxido dismutasa, la catalasa y la glutatión peroxidasa. Son solamente de origen genético por el momento, hasta que se puedan manipular, cosa que ya es posible en las moscas, pero no en los seres humanos.
- Antioxidantes orgánicos, que son de origen alimentario, como las vitaminas E y C, y los carotenos. Los flavonoides están en duda, porque no se sabe si llegan al intracelular.
Las dudas con respecto a los flavonoides se deben a que la absorción desde el intestino al plasma es mala, por lo que se supone que el paso desde el plasma al espacio intracelular, a través de otra membrana, también es malo, de modo que si hay una reducción de 50 veces en el paso de intestino a plasma y otra reducción de 50 veces de plasma al espacio intracelular, prácticamente no llegará nada de flavonoides dentro de la célula. Hay mucha discusión con respecto a este punto y hay evidencia tanto a favor como en contra.
Mitocondrias disfuncionales: envejecimiento
Hay un modelo de mitocondrias disfuncionales, es decir, que no funcionan bien, que es el envejecimiento. Como estamos hablando de dieta mediterránea, longevidad y prevención de la neurodegeneración, parece ser un buen modelo, mucho mejor que una intoxicación con tetracloruro de carbono o algo similar.
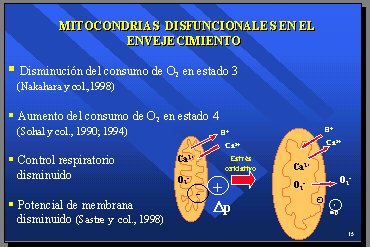
Al observar las mitocondrias en animales (casi siempre roedores, algunas veces monos) se ha encontrado una disminución en el consumo de oxígeno en el estado 3, que es el estado en el cual se produce ATP. Nakahara y colaboradores, en 1998, estudiaron esto en los ratones Sam, de senescencia acelerada (3). También hay un aumento del consumo de oxígeno en el estado 4 y, como el control respiratorio del estado 3 sobre el estado 4 se encuentra disminuido en el envejecimiento, el índice más sensible es la medición del control respiratorio en las mismas mitocondrias (4). Antes de producir el ATP se necesita la presencia de un potencial de membrana y hay una comunicación de Sastre y colaboradores que señala que dicho potencial está disminuido (5).
A partir de estos hechos, se ha postulado que, en el envejecimiento, el estrés oxidativo continuado transforma la mitocondria normal en una mitocondria más grande, que no maneja bien los iones y permite que le entre más agua de lo normal, y que, en lugar de tener salida de protones y entrada de calcio, tiene salida de calcio, salida de superóxido, que normalmente no sale, y disminución del potencial de membrana, con lo que se configura una mitocondria disfuncional (Figura 9).
 Tamaño completo
Tamaño completo Figura 9.
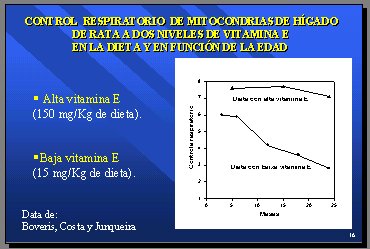
El manejo de antioxidantes en la dieta puede alterar el fenómeno de deterioro denominado “disfuncionalidad de las mitocondrias”. En un experimento, se administró a dos grupos de ratas una dieta con alta o baja cantidad de vitamina E (150 mg/kg versus 15 mg/kg) y se observó el efecto durante 25 meses, que en una rata equivale a unos 100 años en el ser humano (una semana corresponde a un año, aproximadamente). El grupo con dosis alta de vitamina E se mantuvo con muy elevados controles respiratorios y el grupo con dosis baja empezó a deteriorarse a partir de los 7 meses, equivalentes a los 28 años humanos (6) (Figura 10).
 Tamaño completo
Tamaño completo Figura 10.
Flavonoides
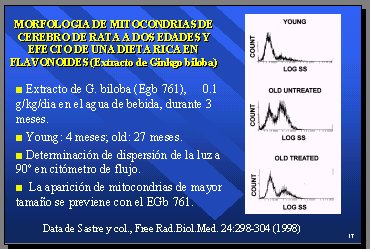
Ya no cabe duda de que la vitamina E puede ingresar a la célula. El grupo de Valencia, de Sastre, administró una dieta con extracto de Ginkgo biloba a ratas durante tres meses y se compararon individuos jóvenes de 4 meses con individuos viejos de 27 meses, que recibieron este tratamiento con respecto a la aparición de mitocondrias de mayor tamaño, determinada por la dispersión de la luz a 90°, en citómetro de flujo. En las ratas jóvenes se encontró una población de tamaño normal y en las viejas hubo una gran proporción de mitocondrias de tamaño grande; sin embargo, esto se previno con el Ginkgo biloba (7) (Figura 11).
 Tamaño completo
Tamaño completo Figura 11.
En esas mismas mitocondrias se determinaron algunos índices de estrés oxidativo, como el nivel de 8-hidroxideoxiguanosina (8-OH-dGuanosina), el nivel de peróxidos y el potencial de membranas. Todo eso estaba mal en las ratas a los 27 meses: los derivados de 8-OH-dGuanosina aumentados, los peróxidos aumentados y el potencial de membrana disminuido, y todos esos cambios se revirtieron, parcial o totalmente, con la dieta con extracto de Ginkgo biloba, volviendo casi a lo normal (Tabla I).
 Tamaño completo
Tamaño completo Tabla I.
Entonces, hay alguna evidencia, en ratas, de que la inclusión en la dieta de fenoles, flavonoides y polifenoles antioxidantes tiene un efecto beneficioso en las mitocondrias, adonde se consideraba muy difícil que pudieran llegar.
Compartimiento vascular
Está contenido en los árboles vasculares. Las reacciones de radicales libres en cadena del espacio vascular tienen dos vías principales de desarrollo.
La primera es la lipoperoxidación de las LDL, que se produce en tres etapas:
- Reacción de iniciación: corresponde a la producción de hidroxilo (HO) y alcoxilo (RO) provenientes de la homólisis de los hidroperóxidos (ROOH) plasmáticos y de hidroxilos provenientes de la homólisis del peroxinitrito (ONO2-) y del peróxido de hidrógeno (H2O2), que por lo tanto provienen de los polimorfonucleares y de las células endoteliales; en cambio, los primeros vienen de los alimentos.
- Reacción de propagación: intervienen los ácidos grasos insaturados de las LDL, observándose un efecto de la presión de oxígeno como delta arteriovenoso. Cuando se mide en el laboratorio el nivel de hidroperóxidos en la sangre arterial y venosa, por cateterismo cardíaco, se encuentran diferencias, ya que la sangre que sale del ventrículo derecho tiene menos hidroperóxidos que la sangre que sale del ventrículo izquierdo, o sea, el paso por el pulmón aumenta el nivel de éstos.
- Reacción de inhibición: por acción de los antioxidantes plasmáticos, que son el objetivo de esta exposición.
La segunda reacción de radicales libres en cadena del espacio vascular corresponde a la producción primaria de NO y O2- por los leucocitos y las células endoteliales, y secundaria de ONO2- y H2O2.
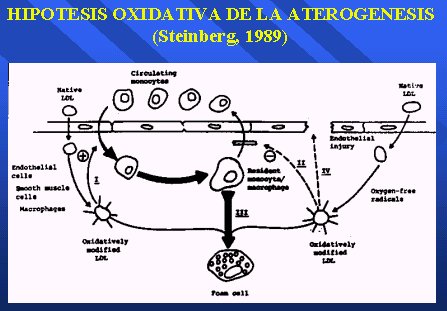
Acerca de la inhibición de la lipoperoxidación de las LDL por los antioxidantes plasmáticos, hay centenares de trabajos. Todo se basa en la hipótesis oxidativa de la aterogénesis de Steinberg, desarrollada en 1989, que plantea que en algún momento las LDL pasan al espacio subarterial, por acción de los radicales libres de oxígeno son modificadas oxidativamente, una vez que están modificadas son fagocitadas por macrófagos generándose las células espumosas. Todos los antioxidantes pueden interferir en esta modificación (Figura 12).
 Tamaño completo
Tamaño completo Figura 12.
Medwave, Año 2, No. 7, Edición Agosto 2002. Derechos Reservados.
- Boveris & Cadenas. Life 2000;50(4-5):245-50.
- Cadenas et al. Free Radic Res. 2000;33(6):747-56.
- Boveris & Turrens. Biochem J 1980;191(2):421-7.
- Nakahara et al. Free Radic Biol Med 1998;24(1):85-92.
- Sohal et al. Mech Ageing Dev 1994 ;74(1-2):121-33.
- Sastre et al. J Clin Invest 1998;102(1):4-9.
- Boveris, Costa y Junqueira (datos no publicados).
- Sastre et al. Free Rad Biol Med 1998;24:298-304.
- Lotito & Fraga, Free Rad Biol Med 1998;24:435-441.
Referencias
Figura 17.
 Tamaño completo
Tamaño completo Ursini y Sevanian observaron que una comida rica en grasas producía un aumento de los lipoperóxidos plasmáticos, lo que se puede prevenir con vino tinto. Esta es la prueba más importante que existe en este momento de la existencia de un compartimiento intestinal en el que se produce absorción de lipoperóxidos (9) (Figura 17).
Tabla IV.
 Tamaño completo
Tamaño completo Su estudio es reciente. Se sabe que los alimentos son normalmente portadores de hidroperóxidos (ROOH), derivados del proceso de enranciamiento de las grasas, y que mientras más ROOH almacenan es peor, pues se absorben y producen reacciones adaptativas, como aumento de la actividad de la glutatión peroxidasa en el hígado y el intestino.
Los alimentos fritos o provenientes de hornos de microondas muestran señales de radicales peroxilos libres (ROO); esto se ha demostrado poniendo pan en un horno de microondas y sacándole luego la corteza, que se pulveriza y se mete en los tubos para medir la señal de radicales libres que contiene; esta señal se ha encontrado aumentada alrededor de 10 veces. O sea, el horno de microondas es especialmente útil para calentar comida y generar radicales libres en los alimentos.
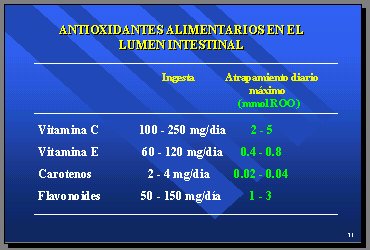
Lo que se sabe de los antioxidantes alimentarios del lumen intestinal es que tienen una capacidad de atrapamiento diario, medida en milimoles de radical peroxilo, de 2 a 5 en la vitamina C y de 0,4 a 0,8 en la vitamina E; los carotenos nuevamente está en niveles microscópicos y los flavonoides tienen una capacidad de atrapamiento en el intestino comparable a la vitamina C y la vitamina E (Tabla IV).
Compartimiento del lumen intestinal
Figura 16.
 Tamaño completo
Tamaño completo Con vino tinto hay una concentración inhibidora 50 de 3 microgramos/ml, concentraciones bajas, muy parecidas a las que usó Federico Leighton en los experimentos para prevenir la oxidación de las LDL, cuando vio que concentraciones altas, de 200 micromolar, pueden prevenir la nitración de la tirosina. El etanol no hace nada, y toda la nitración la previenen los flavonoides.
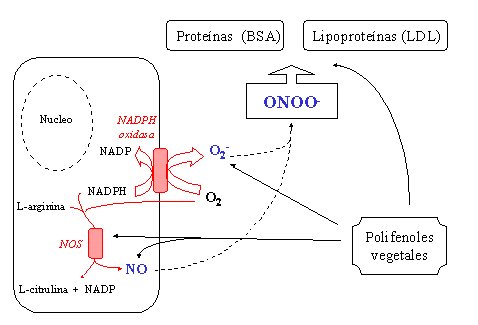
En resumen, en el espacio vascular, los polifenoles vegetales pueden frenar la NADPH oxidasa y la NO sintetasa, e interferir con la oxidación del peroxinitrito a las proteínas y a las lipoproteínas. Esto es lo que se mide y parece que hay concentraciones tres a cuatro veces mayores en el plasma de las mismas sustancias (Figura 16).
Tabla III.
 Tamaño completo
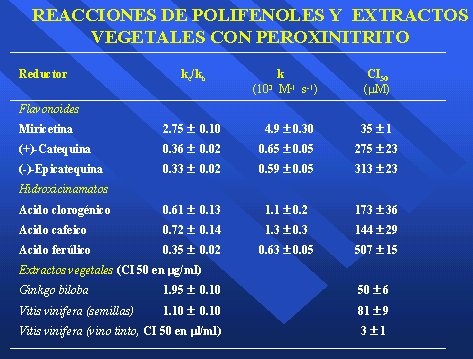
Tamaño completo En nuestros estudios de laboratorio se han usado 1, 2 ó 3 micromoles en plasma y se han probado miricetina, catequina, epicatequina y algunos compuestos más solubles para interceptar peroxinitrito. La mejor concentración inhibidora 50 la tiene la miricetina, con 35 micromolar, muy lejos del 2 y 3 micromolar del plasma. Puede ser que aumente pegándose en la interfase, pero se necesita una gran cantidad. Los hidroxicinamatos resultan peores aún, alrededor de 500, así que jamás van a tener algún efecto biológico.
Lo que llama la atención es que los extractos vegetales, cuya concentración inhibidora 50 está en microgramos/ml, resultaron muy activos. Entonces, quiere decir que la miricetina no es demasiado confiable, pero los extractos de Ginkgo biloba o de vitis vinífera de la semilla están con 50 y 80 microgramos/ml. O sea, es posible que en los extractos vegetales haya flavonoides muy específicos que aún no están identificados (Tabla III).
Tabla II.
 Tamaño completo
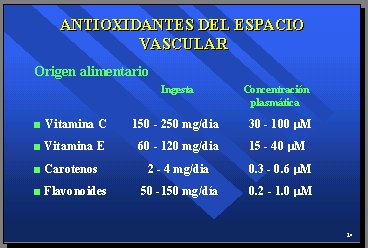
Tamaño completo Los clásicos antioxidantes del espacio vascular son la vitamina E, la vitamina C, los carotenos y los flavonoides. La ingesta aproximada, en Buenos Aires, es la mitad de la que entrega la dieta mediterránea, y se sabe qué concentraciones plasmáticas se pueden obtener razonablemente con estas ingestas. En cuanto a los flavonoides, está en discusión. Lo importante es que los antioxidantes se caracterizan por ser inespecíficos y porque todos pueden reaccionar con radicales libres, y el grueso de la actividad antioxidante y sus efectos biológicos están dados por la vitamina C (30 a 100mg/día) y la vitamina E (15 a 40). Por eso, no parece lógico hacer un estudio que cuesta millones de dólares, usando el betacaroteno con 0,3 a 0,6 micromolares en plasma, ya que habría que aumentarlos 100 veces para estar al nivel de la vitamina C, porque las reacciones no son específicas. También con los flavonoides, que es nuestro campo de acción, se producen concentraciones bajas (Tabla II).
Figura 14.
 Tamaño completo
Tamaño completo En la figura 14 se muestra el squema de un polimorfonuclear produciendo NO y O2- ante un bacillus anthracis con su espora en el centro; luego, el NO y el O2- forman peroxinitrito y H2O2. Hay una cobre-zinc superoxidodismutasa plasmática, lo que significa que hay superóxido que sale al espacio citosólico. El NO se produce con NO sintetasas adheridas a membranas y con sintetasas citosólicas, y el O2- se produce con una NADPH oxidasa, que lo libera hacia el espacio extracelular. Si se inyecta superóxidodismutasa se produce una disminución de la presión arterial, debido al aumento del nivel de NO.
Figura 13.
 Tamaño completo
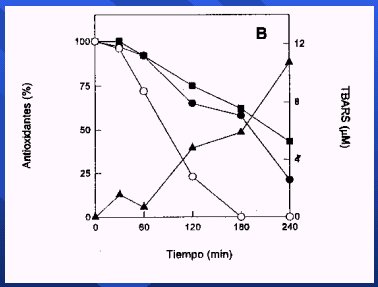
Tamaño completo Se puede hacer un experimento con plasma y LDL, oxidándola con luz ultravioleta o calentándola con un mechero Bunsen y agregándole antioxidantes, y en todos los casos se va a observar una mejoría, tal como observaron Lotitto y Fragga, en su trabajo publicado en 1998, en el que agregaron al plasma la catequina, el antioxidante presente en el vino. La catequina se oxida antes que la vitamina E (alfatocoferol) y el betacaroteno, y, cuando ya está algo oxidada, recién empiezan a producirse los compuestos tiobarbitúricos, que son una indicación de la oxidación de las LDL, por lo que se puede afirmar que en el espacio vascular los antioxidantes pueden prevenir la lipoperoxidación de las LDL (8) (Figura 13).