Cursos
← vista completaPublicado el 1 de agosto de 2007 | http://doi.org/10.5867/medwave.2007.07.3329
Asignación de órganos en Chile: ¿hay un sistema ideal?
Organ allocation in Chile: Is there an ideal system?
Resumen
Este texto completo es la transcripción editada y revisada de una conferencia dictada en el Curso Avances en Gastroenterología 2006, organizado por la Sociedad Chilena de Gastroenterología durante los días 8 al 11 de agosto de 2006.
Lista de espera y prioridades
La lista de espera para trasplante hepático incluye a pacientes con patologías hepáticas graves, que conllevan un alto riesgo de mortalidad; su objetivo es permitir una asignación adecuada de los órganos disponibles para trasplante, provenientes tanto de donante cadáver como de donante vivo. Dicha asignación se determina en una instancia central.
El tiempo de espera por un donante puede variar y algunos pacientes fallecen antes de conseguir uno, lo que se conoce como “mortalidad en la lista de espera”; otros pacientes se complican o sufren algún episodio que obliga a retirarlos de la lista de espera, por ejemplo, la aparición de un cáncer u otra complicación médica que lo inhabilite como receptor.
En los Estados Unidos, en la última década, la lista de espera para trasplante hepático aumentó en ocho a diez veces: en 1991 era de 1.800 a 2.000 personas y en la actualidad se compone de 17.000 pacientes; en contraste, el número total de trasplantes en el mismo país sólo se ha duplicado, subiendo de 3.000 trasplantes, en 1991, a 5000, en la actualidad, de modo que la brecha que existe entre la lista de espera de trasplante y la de pacientes trasplantados ha ido en aumento. A esto se agrega el hecho de que la mortalidad entre los pacientes que están en lista de espera y tienen indicación de trasplante, ha aumentado: en 1991 la cifra fue de 600 pacientes y en la actualidad alcanza a 1500 pacientes por año.
La escasez de órganos y de donantes y el aumento de la demanda por parte de pacientes cirróticos son problemas a escala mundial. La sociedad reconoce cada vez más que el trasplante hepático es la única posibilidad de sobrevida para un paciente con enfermedad hepática terminal, por tanto, un número cada vez mayor de enfermos se deriva a los centros de trasplante, lo que se traduce en tiempos de espera prolongados, enfermedad hepática más avanzada en el momento del procedimiento y, por ende, mayor mortalidad peri-trasplante. Es distinto trasplantar a un paciente en etapa Child B estable que a un paciente Child C, porque la mortalidad asciende en forma importante y muchas veces se rechaza a pacientes jóvenes que llegan en forma tardía a la unidad de trasplante, lo que aumenta aun más la mortalidad en la lista de espera.
En los últimos años, todos los centros del mundo se encuentran trabajando en la elaboración de un sistema que permita establecer la prioridad de los pacientes que están en la lista de espera, con el objetivo de asignar los órganos en forma justa y adecuada y así reducir la mortalidad en la lista de espera. Es frecuente que los distintos sistemas disponibles, Child-Pugh o MELD, asignen valores de sobrevida diferentes a un mismo paciente; por lo tanto, el sistema que se elija se debe ajustar lo más posible a la realidad, de modo que se logre distribuir los órganos en función de la gravedad de la enfermedad y así, reducir la mortalidad.
Es de conocimiento universal que la asignación de órganos se debe ajustar a los principios éticos de equidad, justicia y no discriminación; por lo tanto, cuando surge un donante hepático se debe identificar al paciente que tenga mayor necesidad de ese injerto en el corto plazo y la distribución debe ser eficaz, es decir, se debe seleccionar a los enfermos que tengan buen pronóstico post trasplante. Por este motivo, los equipos de trasplante han preparado documentos sobre indicaciones y contraindicaciones y evaluación de elementos como edad del paciente, gravedad y presencia de co-morbilidad, con la idea de seleccionar a los enfermos que tendrán mejor pronóstico. El objetivo es lograr un sistema de asignación de órganos justo y equitativo, especialmente en los países subdesarrollados, que suelen tener más problemas en la asignación de órganos, porque el período de espera es mayor.
En España se sigue utilizando el sistema de antigüedad en la lista de espera, porque en ese país no existe una alta tasa de donantes y se realizan 1.000 trasplantes al año, en una población de 41 millones de habitantes. En los Estados Unidos la tasa de donación de órganos es mayor, por lo que los pacientes más graves pueden recibir un trasplante hepático con rapidez y tienen bajas tasas de insuficiencia hepática fulminante y mejor evolución post trasplante. En Chile, la tasa de donación de órganos es tres a cuatro veces más baja, lo que determina que el tiempo de espera para trasplante sea mayor.
Evolución de los sistemas de trasplante en el mundo
El caso de Estados Unidos es paradigmático y ayuda a visualizar la evolución de los sistemas de trasplante en el mundo. En 1984 se dicta la Ley Nacional de Trasplante, que crea una red de procuración a cargo de la United Network for Organ Sharing (UNOS), institución central que vigila a todos los pacientes que se inscriben para trasplante hepático en los Estados Unidos, se encarga de la procuración y asignación de los órganos y verifica lo que ha ocurrido con los trasplantados hepáticos y de órganos sólidos en todo el país. UNOS publica la información disponible, periódicamente, en Internet. Cuando se deriva a un paciente a un centro de trasplante, se evalúa y, si se considera candidato a trasplante, se inscribe en la lista nacional de la UNOS.El centro se ubica en un área loco-regional, de modo que hay 62 Organ Procurement Organization (OPO), que son las instancias locales. Una vez que aparece un donante, por ejemplo, en el estado de California, se entrega el órgano a un receptor de la lista local que tenga el mismo grupo sanguíneo y a quien se haya asignado la mayor prioridad en ese territorio. En los diez a doce últimos años, en los Estados Unidos el sistema de asignación se ha ido modificando con miras a priorizar a los enfermos más graves, siguiendo el principio de otorgar al enfermo más grave el órgano que le permitirá seguir viviendo y mejorar su calidad de vida. Dada la gran cantidad de pacientes que integran las listas de espera en los Estados Unidos, que en la actualidad ascienden a 17.000 personas, es muy difícil asignar los órganos disponibles: cuesta decidir si el órgano irá a un niño o a un adulto, a un padre o a un hijo; la situación es compleja y genera dilemas éticos que comprometen a toda la sociedad.
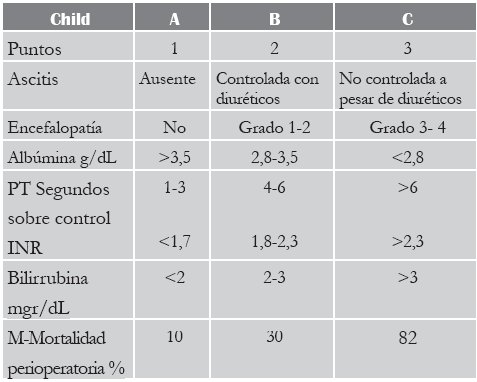
Hasta 1997, en los Estados Unidos se estratificaba según si el enfermo estaba hospitalizado y por su antigüedad en la lista de espera; así, un paciente cirrótico hospitalizado en la Unidad de Tratamiento Intensivo (UTI) y con gran antigüedad en la lista recibía el trasplante hepático primero. Era un método subjetivo que dependía del médico tratante, quien indicaba la hospitalización en UTI o intermedio, lo que originaba muchas injusticias. A partir de 1998 se establece un nuevo sistema de asignación de órganos, con base en la clasificación de gravedad de Child-Pugh (1, 2), conocida desde varios años antes, que evalúa variables clínicas y de laboratorio. En este nuevo sistema, el estado 1 corresponde a los pacientes con insuficiencia hepática fulminante y tiene prioridad sobre todas las demás situaciones hepáticas; los estados 2 A, 2 B y 3 corresponden a pacientes hospitalizados por distintas complicaciones de la cirrosis. Frente a pacientes en igual situación, por ejemplo, ambos en la UTI y complicados con una determinada patología, la prioridad se define por la antigüedad en la lista de espera (Tabla I).
 Tamaño completo
Tamaño completo Tabla I. Escala de Child-Pugh
Este nuevo método es más objetivo, pero no completamente, ya que, por ejemplo, la gravedad de la ascitis o de la encefalopatía se puede sobreestimar, con lo que aumenta el puntaje Child del paciente; y por el efecto del límite máximo, una bilirrubina de 3 mg/dl es lo mismo que una de 40 mg/dl.
En la búsqueda de un sistema más objetivo se desarrolló la escala de MELD (Model for End-stage Liver Disease), creado por la Clínica Mayo en un grupo de cirróticos. Esta escala sólo otorga puntaje a variables objetivas y comparables entre distintos centros y países (3), como los niveles de bilirrubina, creatinina e INR, variables de laboratorio que predicen con gran certeza el mal pronóstico del paciente cirrótico. La excepción a la regla es la insuficiencia hepática fulminante, que tiene prioridad sobre el resto de los pacientes crónicos, y condiciones especiales a las que el sistema estadounidense decidió otorgar puntos adicionales en el sistema MELD. El principio de asignación sigue siendo el otorgamiento de órganos en forma prioritaria al paciente más enfermo, según esta escala de gravedad, que ha asumido un papel importante en varios países del mundo.
El puntaje MELD tiene la ventaja de que se va actualizando cada semana o cada dos semanas, de modo que un paciente con MELD de 18 puede subir a 30 puntos y escalar dentro de la prioridad nacional. La escala se conoce en todos los países y hay calculadoras en Internet que permiten calcular el puntaje, que fluctúa entre 4 y 40 puntos. Los pacientes que tienen 40 puntos tienen una mortalidad a tres meses cercana a 90%; los que tienen menos de 15 puntos tienen una tasa de sobrevida de 80 a 85% a un año, de modo que no se justifica trasplantarlos, ya que la mortalidad perioperatoria del trasplante está entre 8% y 12% en el primer año. Los pacientes muy graves, con más de 29 puntos, tienen una mortalidad alta en los seis primeros meses y ellos son los que se benefician con el trasplante (Fig. 1).
 Tamaño completo
Tamaño completo Figura 1. Cálculo del puntaje MELD
Luego de la introducción del sistema MELD disminuyó el número de pacientes en lista de espera de trasplante y se estableció el propósito de no activar a los que no estuvieran tan enfermos. El puntaje MELD de los pacientes trasplantados subió de 18 a 24 puntos, lo que significa que se trasplantó a pacientes más graves y se redujo apreciablemente la mortalidad en la lista de espera. En resumen, el sistema MELD hizo que, por primera vez en la historia, se redujera la inscripción de pacientes y la mortalidad en la lista de espera, aunque se mantuvo la sobrevida post trasplante.
Realidad Nacional
En Chile se realizan 60 a 70 trasplantes hepáticos al año; la lista de espera supera los 200 pacientes anuales, lo que determina que los tiempos de espera sean de 5 a 24 meses.En un estudio multicéntrico efectuado en 221 pacientes inscritos en cinco centros de trasplante, 25% de ellos fallecieron durante el período de espera, drama que refleja la realidad mundial: todos los países que están utilizando sistemas de priorización por antigüedad en la lista de espera, entre ellos Chile, Brasil, India, Argentina, presentan tasas de mortalidad superiores a 25%. En contraste, los países que utilizan la priorización basada en la gravedad del paciente presentan cifras de mortalidad bajo 10%.
Conclusiones
- Se debe fomentar el trasplante hepático, optimizar la procuración de órganos, utilizar órganos marginales y derivar en forma oportuna a los pacientes, antes de que se encuentren en situación pre mortem.
- Con la implementación de criterios mínimos de trasplante se evitaría el trasplante innecesario de pacientes en etapa muy precoz.
- Es un criterio de justicia social privilegiar la asignación de órganos a los que más necesitan el recurso, identificados por un método como el sistema MELD, que reconoce en forma objetiva a los pacientes de mayor gravedad.
- En la actualidad se está trabajando para cambiar el sistema basado en la antigüedad en la lista de espera, por uno basado en la gravedad del paciente.
- La implementación en Chile de un sistema de prioridades adecuado es una medida razonable, ética y justa, que evitará que el tiempo de espera sea la variable más importante de la mortalidad.
Referencias
- Child, CG, Turcotte, JG. Surgery and portal hypertension. In: The Liver and Portal Hypertension, Child, CG (Ed), Saunders, Philadelphia 1964. p.50.
- Pugh RN, Murray-Lyon IM, Dawson JL, et al. Transection of the oesophagus for bleeding oesophageal varices. Br J Surg 1973; 60:646.
- Kamath et al. A model to predict survival in patients with end-stage liver disease.
- Hepatology. 2001 Feb; 33(2):464-70.

