Resúmenes Epistemonikos
← vista completaPublicado el 6 de mayo de 2019 | http://doi.org/10.5867/medwave.2019.04.7625
PET-CT para el manejo de pacientes con cáncer testicular tipo seminoma con masa residual post quimioterapia
PET-CT for the management of testicular seminoma patients with post-chemotherapy residual masses
Abstract
INTRODUCTION The use of PET-CT could select a subgroup of advanced testicular seminoma patients that display post-chemotherapy residual masses measuring >3 cm and could be managed with surveillance, avoiding unnecessary surgical resection of unviable tumor masses.
METHODS We searched in Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS We identified three systematic reviews that included eleven primary studies; none of these were randomized trials. We concluded the assessment of postchemotherapy residual masses by PET-CT in testicular seminoma patients may prevent unnecessary surgeries, but the certainty of the evidence is low. Furthermore, PET-CT could also offer a favorable risk/benefit and cost/benefit ratio for the management of testicular seminoma patients. However, systematic reviews and primary studies assessing the direct diagnostic impact of PET-CT are required.
Problema
El cáncer de testículo es la neoplasia más común en hombres entre 15 y 44 años. Se divide para su manejo en dos tipos: seminoma y no seminoma. Aproximadamente 30% de los casos debutan con enfermedad metastásica o bien evolucionan con recurrencia sistémica. En esos casos la intención de la terapia sigue siendo curativa; se indica quimioterapia basada en platino, y resección de masas residuales post tratamiento. Dado que los resultados en cuanto a sobrevida son muy buenos (hasta 90% de curación en pacientes de bajo riesgo), el foco actual está en minimizar toxicidades del tratamiento [1].
En el cáncer testicular tipo seminoma el tratamiento induce una reacción desmoplásica del tejido tumoral que hace técnicamente más compleja y de mayor morbilidad su resección; adicionalmente, muchas veces estas lesiones no tienen tumor viable, independiente de su tamaño. Considerando estos factores se acepta que, en esta histología, es seguro el seguimiento, sin cirugía, de lesiones residuales post quimioterapia de hasta 3 cm [2].
Durante los últimos años se ha popularizado el uso de la tomografía por emisión de positrones- tomografía computarizada (PET-CT) para seleccionar pacientes con seminoma que se podrían beneficiar de seguimiento de sus masas residuales post tratamiento, evitando su resección quirúrgica aunque midan más de 3 cm.
Métodos
Realizamos una búsqueda en Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y analizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
Acerca del conjunto de evidencia para esta pregunta
|
Cuál es la evidencia |
Encontramos tres revisiones sistemáticas [3], [4], [5] que incluyeron 11 estudios primarios en 13 referencias [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16], [17], [18] de los cuales ninguno corresponde a evaluación de impacto diagnóstico y todos corresponden a exactitud diagnóstica. Este resumen considera sólo a pacientes con cáncer testicular tipo seminoma. Por lo cual, al analizar las revisiones, se descartó la utilización de una de ellas por no entregar un análisis por separado de seminoma y no seminoma [4] y de otra por su baja cobertura y limitaciones metodológicas [5]. Además, fueron excluidos dos estudios en esta revisión [6], [7] por no presentar datos susceptibles de ser incorporados a un metaanálisis. Así, esta tabla y el resumen en general se basan en nueve estudios primarios [8], [9], [10], [11], [12], [13], [14], [15], [16], utilizando los resultados de exactitud diagnóstica entregados por una de las revisiones [3]. |
|
Qué tipo de pacientes incluyeron los estudios* |
La edad promedio reportada en cada estudio estuvo entre 29 a 42,5 años. Seis estudios incluyeron pacientes con seminoma puro [9], [10], [11], [12], [13], [15], mientras que tres estudios incluyeron pacientes con tumores tipo seminoma y no seminoma [8], [14], [16]. No se pudo obtener el perfil de marcadores tumorales desde la revisión sistemática incluida [3]. Un estudio incluyó pacientes post quimioterapia de primera línea [8], el resto incluyó pacientes post quimioterapia de primera línea y/o rescate [9], [10], [11], [12], [13], [14], [15], [16]. Un estudio también incluyó pacientes post radioterapia [13]. |
|
Qué tipo de intervenciones incluyeron los estudios* |
En todos los estudios se utilizó PET con 18F-fluorodesoxiglucosa (18F-FDG) [8], [9], [10], [11], [12], [13], [14], [15], [16]. En cuatro estudios se realizó FDG/PET-CT [6], [13], [14], [17]. El momento de realización varió entre las 4 y 12 semanas post quimioterapia. La dosis de 18F-FDG y el tiempo entre inyección y registro de imagen cumplió los protocolos locales de cada centro. Todos los estudios compararon contra tomografía computada [8], [9], [10], [11], [12], [13], [14], [15], [16]. Los gold standard utilizados fueron: solo seguimiento en un estudio [12], histología obtenida por cirugía en otro [10] y seguimiento o histología en los 7 estudios restantes [8], [9], [11], [13], [14], [15], [16]. |
|
Qué tipo de desenlaces midieron |
Debido a la ausencia de estudios de impacto diagnóstico, se reportaron las propiedades diagnósticas del test, es decir, sensibilidad, especificidad, valor predictivo positivo y negativo, y likelihood ratio positivo (LR+) y negativo (LR-) para identificar presencia de tumor viable en masas residuales post quimioterapia. El rango de seguimiento reportado por los estudios fluctúa entre 12 y 34 meses. |
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
Cuál es la evidencia
Resumen de los resultados
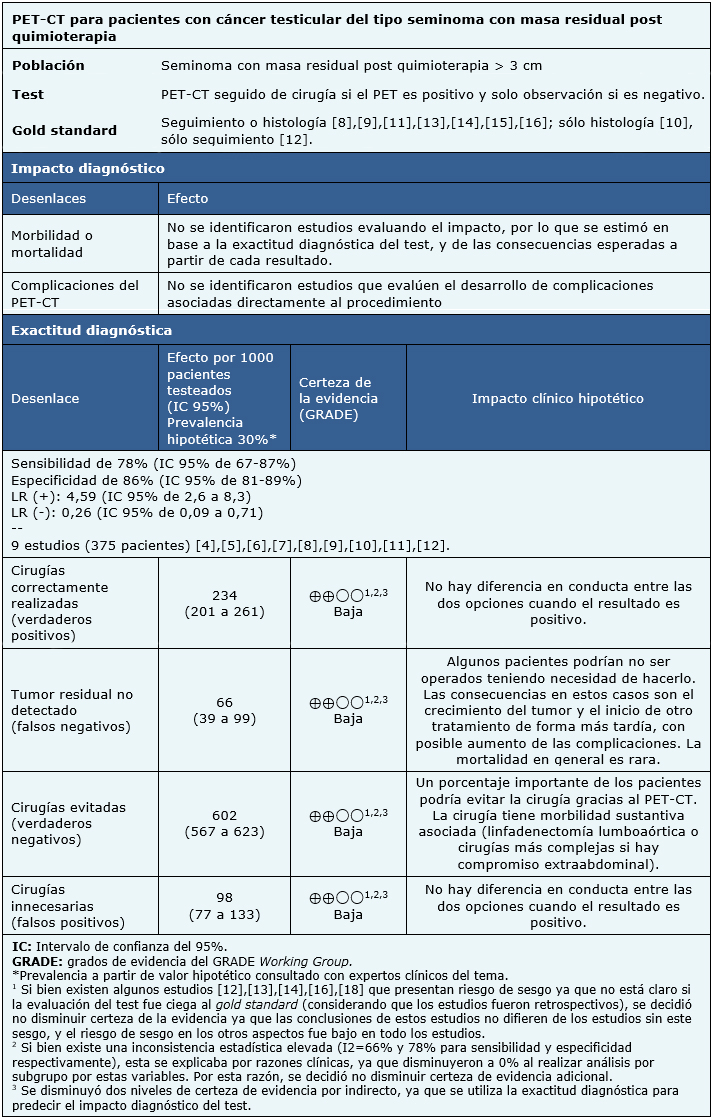
No se identificaron revisiones sistemáticas que evaluaran impacto diagnóstico, sólo resultados de exactitud diagnóstica. Se utilizaron los resultados entregados por una revisión sistemática [3], incluyendo 9 estudios primarios cuyos datos de exactitud diagnóstica se reutilizaron en el metanálisis [8], [9], [10], [11], [12], [13], [14], [15], [16].
El resumen de los resultados es el siguiente:
- El uso de PET-CT en la evaluación de masas residuales post quimioterapia en pacientes con cáncer testicular tipo seminoma podría evitar un porcentaje importante de cirugías innecesarias (certeza de la evidencia baja).
Otras consideraciones para la toma de decisión
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Cómo realizamos este resumen
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
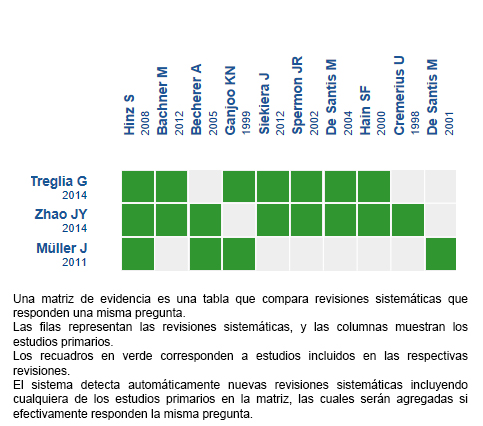
Siga el enlace para acceder a la versión interactiva: PET/CT para el manejo del cáncer testicular tipo seminoma con masa residual post quimioterapia.
Notas
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.

