Análisis
← vista completaPublicado el 30 de mayo de 2013 | http://doi.org/10.5867/medwave.2013.04.5671
Una historia de perjuicio, desperdicio y engaño: cómo la gran industria farmacéutica ha socavado la fe pública en los datos de sus ensayos clínicos y qué podemos hacer al respecto
A tale of harm, waste and deception: how big pharma has undermined public faith in trial data disclosure and what we can do about it
Resumen
El artículo aborda el tema de los datos relacionados con los estudios de intervención en seres humanos conducidos por la industria farmacéutica y cómo la falta de datos, o bien la distorsión de éstos, puede determinar un impacto sobre la toma de decisiones en clínica y en las revisiones sistemáticas. Se comentan los casos de rosiglitazona (Avandia™, GlaxoSmithKline), rofecoxib (Vioxx™, Merck) y de oseltamivir (Tamiflu™, Roche), como ejemplos de perjuicio (morbilidad y mortalidad mayor en quienes han usado los fármacos), de desperdicio (mayor gasto de los gobiernos en programas de control de problemas de salud pública que no tenían base en evidencia) y de engaño (no reporte de eventos adversos por parte de los encargados de los estudios). Las consecuencias de esta conducta sobre la producción científica son múltiples. Principalmente se produce una reducción y distorsión de la base de evidencia para fundamentar las decisiones clínicas, lo que también incluye el sesgo de publicación. Se recogen varias soluciones planteadas en la literatura internacional como el registro de los ensayos clínicos antes de su realización, el uso de directrices para mejorar la calidad de los reportes, fomentar la publicación de todos los resultados de investigación y la autonomía de la academia e investigadores. El registro de los ensayos clínicos no ha sido eficaz en prevenir la opacidad que rodea la experimentación fase III de los ensayos de intervención financiados por la industria. Deben hacerse cargo de este problema los editores de las revistas biomédicas, las autoridades sanitarias encargadas de dar la aprobación a los fármacos antes de su comercialización, los comités de ética que autorizan la ejecución de ensayos en sus establecimientos, los investigadores y académicos y las organizaciones de pacientes. La industria farmacéutica está llamada a responder a estas propuestas que fomentan la transparencia, con lo cual se podrá avanzar en la recuperación de la fe pública en la investigación realizada por ellos.
El contexto
En el siglo XX la salud de los pueblos ha mejorado sustancialmente con respecto de la historia de la humanidad. Arreglos poblacionales, como la introducción del agua potable, han contribuido de manera contundente al control de enfermedades y males que afectaban sobre todo a los más pobres. La introducción de medicamentos ha resultado fundamental en controlar flagelos que antes no tenían solución y su impacto no es menor. La industria farmacéutica ha jugado un papel crítico en producir estas mejoras de la salud humana. Es por esto que resulta tan preocupante lo que a continuación se relata y que tiene como protagonistas, precisamente, a grandes empresas farmacéuticas.
En 1999, la FDA (United States Food and Drug Administration) aprobó la rosiglitazona (Avandia™, GlaxoSmithKline) como hipoglicemiante oral para uso en diabéticos tipo 2. En 2010 el laboratorio retira el medicamento del mercado europeo, debido a las denuncias de mayor frecuencia de eventos adversos cardiovasculares en los pacientes tratados con esta droga.
Ese mismo año de 1999 la FDA aprueba la droga rofecoxib (Vioxx™, Merck) como antiinflamatorio no esteroidal para el tratamiento de la artritis reumatoide, en virtud de su mejor perfil gastrointestinal. En 2004, el laboratorio retira el medicamento del mercado mundial en medio de la extrema judicialización consecuencia de la mayor frecuencia de infartos de miocardio en los pacientes tratados con este fármaco.
En 2005 los gobiernos del mundo compran masivamente oseltamivir (Tamiflu™, Roche) como medida para reducir las complicaciones secundarias a la influenza H5N1, sobre la base de un solo estudio financiado por Roche1 que señalaba que la droga era efectiva en prevenir complicaciones. En 2009 se publica una revisión sistemática de la Colaboración Cochrane2 que indica que no existe evidencia para fundamentar tal aseveración, pero a esa fecha los gobiernos ya habían gastado más de US$7.6003 millones en una droga cuya efectividad no ha sido nunca demostrada.
¿Qué tienen en común estos tres casos y otros más como el de la paroxetina4 (Seroxat™, GlaxoSmithKline) o el de zanamivir5 (Relenza™, GlaxoSmithKline)?
Todos ellos están marcados por un tejido común cuyo hilo matriz es la opacidad de la industria farmacéutica acerca de los datos de los ensayos clínicos realizados en seres humanos durante la etapa de experimentación fase III, además de la solicitud de aprobación de las drogas ante las autoridades correspondientes para su comercialización.
Se trata de una política sistemática de ocultamiento de datos relacionados con los ensayos clínicos que han afectado a las autoridades sanitarias encargadas de dar la aprobación a los fármacos en cuestión; a los editores de prestigiosas revistas biomédicas y a los investigadores independientes que han buscado validar las afirmaciones de la industria sobre efectividad y seguridad. Las consecuencias de esta conducta son graves y profundas:
- Perjuicio porque se ha afectado la salud y la vida de miles y miles de personas en todo el mundo6,7;
- Desperdicio porque gobiernos, prestadores y pacientes han gastado miles de millones de dólares en compras y programas cuya efectividad no está corroborada por la evidencia2,7; y
- Engaño porque la industria farmacéutica persiste en resistirse a entregar la información completa de los ensayos clínicos que ha efectuado sobre las drogas que luego vende en los mercados internacionales8,9,10,11.
Los hechos
Repasemos la historia de cada uno de estos fármacos.
Rosiglitazona
En mayo de 1999 la FDA aprobó la droga rosiglitazona (Avandia™) para el tratamiento de diabetes tipo 2. En julio de ese mismo año un endocrinólogo expresó su aprehensión respecto de la existencia de riesgo cardiovascular asociado a la droga en congresos de la especialidad en Estados Unidos, lo que le valió ser objeto de fuertes amenazas por parte de altos ejecutivos de GlaxoSmithKline (entonces era SmithKline Beecham). El médico fue persuadido de firmar un acuerdo en que se comprometió a guardar silencio sobre el tema12.
En diciembre de 2002, la FDA advierte del posible mayor riesgo de insuficiencia cardíaca congestiva. En septiembre de 2005, GlaxoSmithKline revisa 37 ensayos clínicos aleatorizados conducidos por ellos en que se muestra un mayor riesgo de isquemia de miocardio. Los datos no fueron publicados en revistas revisadas por pares, sino que sólo en su sitio web, consecuencia de un acuerdo judicial con el estado de Nueva York. En septiembre de 2006 aparece el estudio DREAM13, que compara rosiglitazona con placebo, y en que figura un mayor riesgo de eventos cardiovasculares y riesgo estadísticamente significativo de insuficiencia cardíaca congestiva, lo que fue comentado en carta al editor por Nissen14. En diciembre de 2006 se publica el estudio ADOPT15 que también arroja un mayor número de infartos de miocardio. En ese mismo mes, GlaxoSmithKline comunica ventas récord por US$ 3.300 millones para el año. En 2006, estudios de la FDA y de la compañía corroboran el mayor riesgo cardiovascular, pero no son publicados ni divulgados.
En enero de 2007, la empresa deniega la entrega de datos de pacientes (los Clinical Study Reports, también conocidos como CSR) a un grupo de investigadores interesados en hacer un metaanálisis de los desenlaces cardiovasculares secundarios a rosiglitazona. Finalmente, en julio de 2007, la FDA emite su primera advertencia sobre el mayor riesgo de eventos isquémicos (40%), destacando que se habrían producido 83.000 infartos de miocardio, causados por el uso de la droga y evitables16. En enero de 2009, la ADA (American Diabetes Association) y la EASD (European Associationa for the Study of Diabetes) emiten una recomendación de no indicar rosiglitazona. En junio de 2009 se publica el estudio RECORD17 pero cuya potencia estadística es insuficiente para evaluar desenlaces cardiovasculares. En julio de 2009, la FDA instruye a la compañía a realizar un estudio sobre desenlaces cardiovasculares asociados a uso de rosiglitazona, cuyos resultados se deberían conocer recién en 2015.
En 2010 GlaxoSmithKline retira la droga del mercado europeo, pero sigue comercializándola en Estados Unidos. En Chile, la rosiglitazona ha sido objeto de dos tibias alertas de seguridad de parte del Instituto de Salud Pública, la última con fecha abril de 201118, pero su comercialización está vigente. GlaxoSmithKline se encuentra actualmente enfrentando numerosas demandas judiciales en el Reino Unido19.
Rofecoxib
En 1999 la FDA aprueba Vioxx™ para el tratamiento de la artritis reumatoide sobre la base del estudio VIGOR20 que compara rofecoxib con naproxeno. En él la droga en estudio se asoció con significativamente menos eventos gastrointestinales altos que el control. El estudio se publicó en 2000 en el NEJM (New England Journal of Medicine), pero sin que se incluyeran datos sobre mayor riesgo de infarto de miocardio en el grupo tratado con rofecoxib. En 2005 el NEJM publica una nota de reserva sobre el estudio21, la que dice:
“Tres infartos de miocardio, todos en el grupo tratado con rofecoxib, no fueron incluidos en los datos que se enviaron a la Revista. Los editores tuvieron conocimiento de estos casos en 2001 cuando la FDA publicó datos actualizados del estudio…
A fines de noviembre de 2005, seguíamos pensando que estos eventos eran alejados y que no estaban en conocimiento de los autores a tiempo como para haber sido incluidos en el artículo publicado en la Revista el 23 de noviembre de 2000. Sin embargo, ahora se conoce un memorándum interno de la farmacéutica con fecha 5 de julio de 2000, que se obtuvo mediante exhorto en el juicio por Vioxx y que fue puesto a disposición de la Revista, que revela que al menos dos de los autores supieron de los tres infartos de miocardio adicionales, al menos dos semanas antes del envío de la primera de dos revisiones del manuscrito, y cuatro meses y medio antes de la publicación del artículo. En virtud de este memo, parece que hubo tiempo suficiente como para haber incluido estos datos en el artículo.
El hecho que tres infartos de miocardio no hubiesen sido incluidos, conlleva certeza de que los cálculos y las conclusiones del artículo son incorrectos”*.
Pero también Circulation, Annals of Internal Medicine y otras revistas publicaron artículos escritos por funcionarios de Merck. La filiación a la farmacéutica de los autores fue conocida con posterioridad gracias a la divulgación de documentación judicial. En los artículos publicados, no todos los autores dieron a conocer sus relaciones financieras con Merck.
En 2005, el NEJM publica el estudio APPROVe sobre uso de rofecoxib en adenomatosis colorrectal22 y en 2006 la misma revista publica una corrección del artículo, mostrando graves errores en la sección resultados23. Merck retiró voluntariamente el medicamento en 2004 en medio de extrema judicialización.
Oseltamivir
En 1999, la Organización Mundial de la Salud publica su primer plan para pandemia de influenza, en que recomienda utilizar antivirales como profilaxis. Luego, en 2002 hace un llamado a incluirlos en los programas nacionales24. En 2005 los gobiernos del mundo comienzan a comprar grandes cantidades de Tamiflu™ para contrarrestar las complicaciones de la pandemia por gripe aviar (H5N1) –aún cuando el proveedor era monopólico-, basados fundamentalmente en las directrices entregadas por la Organización Mundial de la Salud en 200425. En ese mismo año, el Plan Pandemia de Estados Unidos recomienda el uso de Tamiflu sustentado en el estudio Kaiser1.
En 2006, una revisión sistemática de la Cochrane indica que Tamiflu es efectiva en prevenir complicaciones asociadas a influenza26, y la CDC (Centers for Disease Control and Prevention) también afirma en sus guías que Tamiflu reduce el riesgo de neumonía e ingresos hospitalarios, siempre basado en el estudio Kaiser. En abril de 2009 aparece la gripe porcina (H1N1) y en julio del mismo año un médico japonés señala a los revisores de la Cochrane que las conclusiones de su revisión sistemática sobre los inhibidores de la neuroaminidasa se fundaban sobre un solo estudio que, por lo demás, había sido financiado por Roche y que era un análisis agrupado de 10 ensayos clínicos aleatorizados. Todos ellos conducidos y financiados por Roche, de los cuales dos habían sido publicados, y otros ocho no. Hasta la fecha, estos ocho ensayos aún no han sido publicados27.
En agosto de 2009, los autores de la revisión Cochrane, Tom Jefferson y Peter Doshi, contactan a los autores del estudio Kaiser para obtener los datos completos de los pacientes incluidos (los CSR), pero todos los autores, tanto Kaiser, como los autores Treanor (primer estudio publicado en JAMA, Journal of the American Medical Association) y Nicholson (el segundo estudio publicado en Lancet) dijeron no tener datos de pacientes, no necesitarlos y que las consultas se deben remitir únicamente a Roche, que es donde se hicieron todos los análisis estadísticos3.
En diciembre de 2009, Jefferson y col publican una revisión sistemática con metaanálisis en el BMJ (ex British Medical Journal) refutando la efectividad de Tamiflu y concluyen que no hay evidencia que corrobore que Tamiflu es efectivo en reducir complicaciones por influenza2. A la luz de la publicación del BMJ (Figura 1), en el mismo mes, Roche anuncia que entregará los informes completos de los estudios para revisión independiente. Sin embargo, hasta la fecha no los ha entregado28.
 Tamaño completo
Tamaño completo Pero la EMA (European Medicines Agency) sí entregó todo lo que Roche le había incluido en su solicitud de autorización para oseltamivir, y sin censura. Basados en las miles de páginas de datos de pacientes que la EMA facilitó al grupo de Jefferson, estos pudieron actualizar la revisión sistemática de 2009, la que fue publicada en 2012 y en que se concluye que Tamiflu, a lo más, podría reducir en un día la duración del cuadro de influenza29. Según Doshi, entre 2005 y 2009 los gobiernos habrían gastado US$7.600 millones en Tamiflu para prevenir complicaciones por influenza. Uno puede sospechar que esa cifra está fuertemente subestimando el gasto total en un medicamente producido por un laboratorio farmacéutico, ya que no sólo los gobiernos compraron, sino que también las personas de su bolsillo.
Los aprendizajes
“Intimidación corporativa, el silenciamiento de la disidencia científica y la supresión de los puntos de vista científicos, amenazan tanto el bienestar público como la salud financiera del gobierno federal, que paga por el cuidado de la salud”12.*
“Se han aprobado drogas contra la diabetes solamente basados en sus efectos hipoglicemiantes, lo que se ha comprobado que es miope y sin fundamento científico. Las drogas que reducen la glicemia pueden potencialmente tener otros efectos adversos que podrían anular el beneficio buscado”30.*
“La historia de rosiglitazona dice mucho acerca de lo que está pasando con la atención sanitaria, que no se ve centrada en los intereses de los pacientes, en aliviar la enfermedad, en promover función y autovalencia, en curar patologías, si no que más bien en promover otro tipo de intereses, puntualmente los de la industria farmacéutica. ¿Acaso la corrupción en salud ha llegado tan lejos, que se corre el riesgo de parecer ingenuo o irracional si se pretende que las compañías farmacéuticas sea responsables, que las autoridades sean proactivas e ilustradas, y que los prescriptores sean ponderados y razonables?”31.*
Las citas anteriores son reveladoras del lado más oscuro de la conducta de la gran industria farmacéutica que, como se ha demostrado en el transcurso de este artículo, no escatima esfuerzos para lograr sus objetivos comerciales. El problema es que estos objetivos están crecientemente menos alineados con los intereses de los pacientes o con las preocupaciones de salud pública de los gobiernos.
El interés de la industria es mantener una producción constante de nuevos medicamentos que, aún siendo muy similares a otros ya existentes en el mercado, puedan tener alguna característica nueva, distinta o novedosa que permita levantar una campaña de marketing. Estas drogas son conocidas en la jerga inglesa como “me-too drugs”; pertenecen a una clase existente; tienen una leve diferenciación de lo que ya hay y su perfil de seguridad es menos conocido. Por otra parte, tienen una gran ventaja sobre la oferta disponible en el mercado: mantienen su patente vigente, lo que permite precios elevados en la comercialización.
Sumando y restando, para la industria es siempre rentable introducir un medicamento nuevo al mercado, crear la necesidad en los prescriptores sustentados en millonarias campañas de posicionamiento y prebendas, y asegurar recaudación máxima hasta que expire la patente. En su libro Mala Ciencia, Ben Goldacre sostiene que de los US$200 mil millones que las grandes farmacéuticas estadounidenses facturan al año, sólo 14% es gasto relacionado con investigación y desarrollo, mientras que el doble (31%) se gasta en marketing y administración32.
Existe amplia evidencia en la literatura de que los estudios publicados ocultan sistemáticamente el riesgo. En el caso de Vioxx, por ejemplo, Merck financió y condujo todos los aspectos relacionados con los ensayos, incluyendo análisis de datos, monitoreo de seguridad y preparación de manuscritos33. De la documentación judicial divulgada en Estados Unidos, se supo que no todos los autores admitían relación financiera y remunerativa con Merck, por lo que la opacidad se incrementa aún más: no sólo datos sobre seguridad, sino que también las relaciones de los autores con el financiador del estudio, se mantienen bajo secreto.
La paciencia de los editores se ha visto puesta a prueba, como lo demuestra un editorial del NEJM34 que se expresa en duros términos contra algunas farmacéuticas por haber abierto el ciego de varios estudios, haber tomado decisiones que fueron impuestas unilateralmente a los investigadores y haber interactuado indebidamente con los Data and Safety Monitoring Board, todo lo cual socava la fe pública en la conducta de los ensayos y el grado de independencia que tienen los investigadores con respecto del financiador. La autonomía de los comités de monitoreo de datos de los estudios multicéntricos internacionales está siendo fuertemente cuestionada ya que muchas universidades del primer mundo, que se hacen cargo de esta tarea para la industria, permiten convenios de confidencialidad (los llamados gagging clauses) que son impuestos por la industria y permiten que los investigadores no tengan acceso a los datos del estudio para hacer sus análisis propios.
Otra revista que ha sido implacable en su lucha por abrir esta caja de Pandora que son los ensayos clínicos financiados por la industria es el BMJ. Si en 2009 ya se plantean serias interrogantes sobre la probidad de la investigación sobre Tamiflu, en 2012 esta revista dedica un número entero a la cuestión de los datos ocultos y comienza la campaña de transparencia respecto de todos los datos inherentes a los estudios de intervención35,36.
Cuando no toda la información científica está disponible para ser independientemente analizada y los reportes publicados no son fiel reflejo de lo que en realidad ocurrió durante el proceso de conducción y desarrollo de los ensayos, las consecuencias son gigantescas. En el menor de los casos se reduce y se distorsiona la base de evidencia sobre la cual clínicos y salubristas actúan. Por otra parte, pacientes y voluntarios que han participado de los ensayos también ven contrariado su interés de aportar al bien común, pues el supuesto de que todo lo investigado será compartido con la comunidad científica mayor queda vulnerado irremediablemente y sujeto al interés secundario de lo que es o no rentable para la compañía.
Aterrizando en Chile, en 2010 Salas y Russo se preguntan por las consecuencias locales de los problemas relacionados con Avandia y ponen correctamente el foco sobre el actuar de los comités de ética de la investigación. Estos son las entidades encargadas de autorizar la investigación clínica en los establecimientos sanitarios del país, incluyendo el reclutamiento de pacientes37. ¿Hasta qué punto estos comités tienen las competencias necesarias para regular de buena manera el acceso a nuestros pacientes, a preservar la integridad de la investigación y a cumplir con las exigencias legales en materia de protección de la dignidad de los sujetos? Ello es un tema abierto y que necesariamente debería ser materia de investigación, tanto en Chile como en los demás países de la región.
Las soluciones
Estamos en una época en que se está investigando siempre con mayor interés el tema del sesgo de publicación40,41,42,43,44,45. Al encontrarse con un número siempre mayor de sesgos, que son los sesgos no por error de azar que podríamos controlar y mitigar con buenos diseños metodológicos, la comunidad de investigadores con correcta percepción se pregunta hasta qué punto aquello que publicamos es el fiel reflejo de lo que se investigó y si los datos entregados a la luz pública son verdaderos y replicables. Ioannidis, en el artículo más citado de la historia, sostiene de entrada que la mayor parte de los resultados de las investigaciones científicas, son falsos46.
Entonces ¿qué hacemos?
Publicar todo
No debe quedar al arbitrio de una compañía farmacéutica o de un investigador si se publican o no los resultados de la investigación científica47. Sir Iain Chalmers ha sido uno de los voceros más insistentes sobre este tema, llegando incluso a sostener en el Symposio Equator-Network de 2012 (Freiburg, Alemania) que se debería establecer que la no publicación de cualquier tipo de resultados de investigación, sean estos positivos o negativos, debería ser criminalmente perseguido48. No es posible insistir suficientemente acerca de la enorme importancia que tiene esta sola medida, que no sólo se debe aplicar a la industria farmacéutica, sino que a todos quienes conducen investigación, independientemente del origen de su financiamiento.
Registrar los ensayos y publicar los protocolos
Estas dos medidas son fundamentales para asegurar la transparencia de lo que posteriormente se va a publicar como artículo final. Sin embargo, varios estudios han puesto en evidencia que no siempre se cumple la palabra empeñada. Gracias a la sagacidad de algunos, se han podido descubrir distorsiones posteriores en la ejecución del ensayo con respecto de los registrados, incluyendo cambios en los desenlaces, cambios post-hoc en la pregunta del estudio, etc.49.
Modificar la metodología de los metaanálisis
La Colaboración Cochrane está cambiando paulatinamente su unidad de análisis: si antes eran los estudios publicados, ahora deben ser los Clinical Study Reports, que en otras palabras son los datos individuales de los pacientes. El caso de Tamiflu puso en evidencia que no todo lo que brilla es oro. La necesidad de tener acceso a los datos duros de los ensayos es clave a la hora de determinar la efectividad de una intervención. En consecuencia, las publicaciones ya no son confiables por las razones ya mencionadas. Sin embargo, no es posible, para quien quiere ejercer una práctica clínica basada en la evidencia, emprender este tipo de revisiones sistemáticas, las que requieren de gran cantidad de tiempo y esfuerzo.
Directrices para mejorar la calidad de los reportes
Y para aquello que sí se publica, y pensando en que en el futuro se debería publicar todo, es fundamental que los artículos sean completos, precisos y replicables. La autocorrección es un principio fundacional de las ciencias, por lo que es necesario difundir y aplicar las directrices que van en el sentido de mejorar la transparencia, precisión y exactitud de la comunicación biomédica con el fin último de corroborar o refutar, aquello que otros hacen.
Políticas editoriales firmes
Nada sacamos con tener registros de los ensayos y publicación de protocolos si las revistas biomédicas –y principalmente las de alto impacto de los países desarrollados– no aplican con mano dura las exigencias señaladas. Hay estudios que muestran que las revistas que recomiendan el uso de directrices, luego no aplican medidas para asegurar que estas se respetan. O que aún cuando digan que es obligatorio haber registrado el ensayo, lo publicado finalmente no estaba registrado50,51.
Autonomía de la academia
Estando conscientes de que “quien pone el dinero, pone la música”, que la academia resguarde y proteja su autonomía cobra fundamental importancia. Si se hace una búsqueda en clinicaltrials.gov de los ensayos realizados o en vías de realización en Chile, aparecen 889; 41 estudios de estos 889 indican que su estatus se desconoce. Ello quiere decir que han pasado más de dos años desde que se introdujo información al registro. De los 848 restantes, 450 informan que están completados y de estos sólo 120 informan resultados. Otros 330 están completados y sin resultados. De ellos, 267 son financiados por la industria, de los cuales los que están siendo conducidos en Chile, y que han sido completados excluyendo los estudios cuyo estatus se desconoce y que no informan resultados, sólo 53 han ingresado alguna actualización al sistema en 2013 (clinicaltrials.gov). En otras palabras, hay 214 estudios de los que no tenemos información actual y no reportan resultados en este registro (Figura 2).
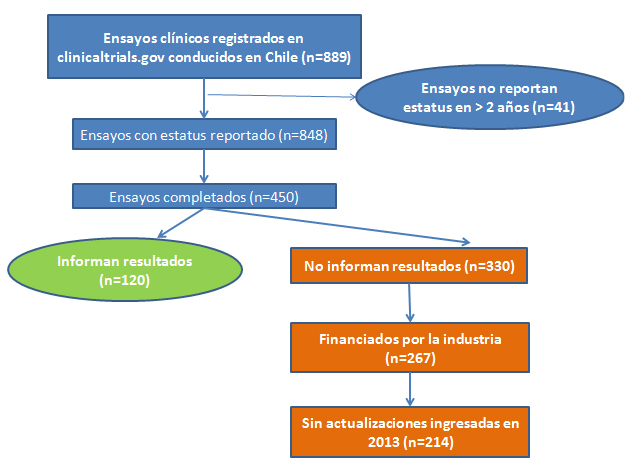 Tamaño completo
Tamaño completo Aquí se ve claramente la responsabilidad que le cabe a la academia y a los comités de monitoreo de datos de los estudios, para ser proactivos en impedir la no divulgación de los resultados de los estudios en los que están participando.
Conclusión
De esta problemática se deben hacer cargo muchas partes: autores, pares revisores, editores, entidades financiadoras de investigación, educadores médicos, comités de ética, agencias de certificación de fármacos y organizaciones de pacientes. Solamente cuando se arroje luz sobre el perjuicio al que se ha expuesto a pacientes y voluntarios, sobre el desperdicio de gastar en soluciones sanitarias que no tienen evidencia de respaldo, y sobre el engaño al que hemos sido sometidos quienes leemos la literatura científica, es que podremos avanzar en incrementar la transparencia e integridad de la investigación científica que, en último análisis, la hacemos para beneficiar nuestros pacientes y pueblos. La responsabilidad es de todos.
La reposición de la fe pública en la investigación científica conducida por la industria farmacéutica, es clave para poder recobrar la confianza en aquello que la industria nos ofrece como tratamientos de enfermedades que a todos nos pueden afectar. Seguir las medidas propuestas significará que tendremos un mayor grado de certeza respecto del perfil de seguridad de los fármacos introducidos a mercado. Primando la necesaria transparencia se podrá generar un control social en que la industria, como es de esperar, ponga al centro del interés a los pacientes con sus necesidades de salud.
Notas
*La traducción es de la autora.
Declaración de conflictos de intereses
La autora ha completado el formulario de declaración de conflictos de intereses del ICMJE traducido al castellano por Medwave, y declara no haber recibido financiamiento para la realización del artículo/investigación; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado, en los últimos tres años; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. El formulario puede ser solicitado contactando a la autora responsable.

