Consenso
← vista completaPublicado el 1 de enero de 2010 | http://doi.org/10.5867/medwave.2010.01.4357
Revisión de la literatura para la actualización en las normas de seguimiento de pacientes tratadas por un cáncer de mama (etapas 0-III)
Literature review for the update on the guidelines for follow-up of patients treated for breast cancer (stages 0-III)
Contenidos
Introducción
Objetivos Específicos
Síntesis de la Evidencia y Recomendaciones
1. ¿Cuáles son las Recomendaciones Básicas para el Seguimiento?
2. ¿Cuál es el Rol de la Mamografía?
3. ¿Cuánto Tiempo se Debe Extender el Seguimiento?
4. ¿Quién Puede Realizar el Seguimiento?
5. ¿Cómo Influyen las Mutaciones BRCA en el Seguimiento?
6. ¿Cuáles son las Complicaciones Alejadas del Tratamiento?
7. ¿Cuál es el Seguimiento Ginecológico Adecuado?
8. ¿Se Puede Usar Terapia de Reemplazo Hormonal (TRH)?
9. ¿En qué Consiste el Seguimiento luego de una Mastectomía Total?
10. ¿Se Puede Recomendar el Uso de Mastectomía Contralateral Profiláctica (MCP), en Ausencia de Mutaciones de BRCA?
11. ¿Qué Impacto Tienen las Guías para el Seguimiento de Pacientes Tratadas por Cáncer de Mama?
12. ¿Qué Estudios No se Deben Hacer en Pacientes Asintomáticos?
Referencias
Introducción
El tiempo total de sobrevida luego del tratamiento de un cáncer de mama se divide en el lapso sin enfermedad detectable y el período complementario con enfermedad detectable hasta la muerte. El uso de exámenes de seguimiento en pacientes asintomáticos, salvo para la detección de una recurrencia local potencialmente curable (mamografía y examen físico), no produce aumento de sobrevida global ni mejor calidad de vida, sino tan sólo la migración de una categoría a otra.
Estando la paciente en el grupo de recurrencia sistémica, la curación prácticamente no existe y la sobrevida global no ha sido impactada con los tratamientos disponibles en las últimas 2 décadas: mediana de SV global de 2,5 años; Figura N°1 (Dawood, 2008: Journal of Clinical Oncology, Vol 26, No 30 -October 20-, 2008: pp. 4891-4898). De este modo, el uso indiscriminado de exámenes de rutina en pacientes asintomáticas sólo produce ansiedad, deterioro de la calidad de vida y aumento en los costos del sistema de salud. En este capítulo se revisan las recomendaciones actuales para el seguimiento de pacientes tratadas por un cáncer de mama.
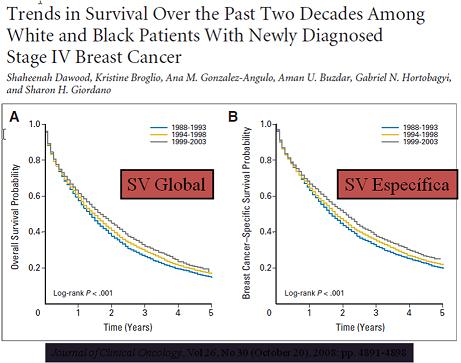 Tamaño completo
Tamaño completo Objetivos Específicos
El objetivo de esta revisión es identificar, sintetizar y evaluar la mejor evidencia disponible para la actualización de las Normas de Seguimiento de Pacientes Tratadas por Cáncer de Mama (etapas 0-III) a partir de lo señalado en el Consenso de Cáncer de Mama del año 2003.
Para esto se revisaron las siguientes preguntas:
- ¿Cuáles son los objetivos del seguimiento?
- ¿Cuál es el rol de la mamografía?
- ¿Cuánto tiempo se debe extender el seguimiento?
- ¿Quién puede realizar el seguimiento?
- ¿Cómo influyen las mutaciones de BRCA en el seguimiento?
- ¿Cuáles son las complicaciones alejadas del tratamiento?
- ¿Cuál es el seguimiento ginecológico adecuado?
- ¿Se puede usa terapia de reemplazo hormonal?
- ¿En qué consiste el seguimiento luego de una mastectomía total?
- ¿Se puede recomendar el uso de mastectomía contralateral profiláctica, en ausencia de mutaciones de BRCA?
- ¿Qué impacto tienen las guías para el seguimiento de pacientes tratadas por cáncer de mama?
- ¿Qué estudios No se deben hacer en pacientes asintomáticas?
Síntesis de la Evidencia y Recomendaciones
1. ¿Cuáles son las recomendaciones básicas para el seguimiento?
Síntesis de la evidencia:
El principal objetivo del seguimiento es reconocer las recurrencias locales potencialmente curables en pacientes tratadas por cáncer de mama, y la detección de enfermedad metastásica, que por lo general es incurable. En este esfuerzo en pacientes asintomáticas, el 60% de recurrencias son detectadas por las mismas pacientes entre controles y un 40% por examen físico médico y exámenes de rutina (Bock, 2004; Pandya, 1985). Ensayos aleatorizados no han demostrado diferencia en sobrevida entre las pacientes seguidas con examen físico y mamografía comparadas con aquéllas incluidas en sistemas de seguimientos más intensivos que asocian test de laboratorio y estudios de imágenes (GIVIO, 1994; Rojas, 2005; Rosselli Del Turco, 1994; Joseph, 1998).
Nivel de evidencia I.
La tasa esperada de recurrencia oscila entre 1% y 1,5% por año, siendo el segundo año del seguimiento el de mayor diagnóstico de recurrencias sistémicas. Las pacientes con recurrencia mamaria clínica tienen peor pronóstico que las pacientes con recurrencias detectadas por mamografía (Montgomery, 2007).
Nivel de evidencia II.
Recomendación:
- Educación para autoexamen mamario mensual.
- Examen físico cada 3-6 meses por los primeros 3 años postratamiento, cada 6-12 meses en los años 4 y 5, y luego anualmente.
- Primera mamografía un año después de la mamografía que condujo al diagnóstico, pero no antes de 6 meses de terminada la radioterapia local. Luego, una mamografía anual.
- Educación a las pacientes respecto de los síntomas más frecuentemente relacionados a eventuales recurrencias: nódulos mamarios nuevos, dolor óseo, dolor torácico, dolor abdominal, disnea y/o cefalea persistente.
- Sitios web para autoeducación de pacientes: www.plwc.org y www.cancer.org.
2. ¿Cuál es el Rol de la Mamografía?
Síntesis de la evidencia:
La mamografía muy probablemente ayuda al diagnóstico de lesiones más tempranas (< de 1 cm o DCIS) de cáncer metacrónico (Mellink, 1991). Sin embargo, el método de detección de recurrencia ipsilateral no afecta la sobrevida global. El diagnóstico de cáncer contralateral ocurre en etapas más tempranas que el primario original en las pacientes seguidas con mamografía (Grunfeld, 2002). Cada mamografía adicional durante el seguimiento se asocia con una disminución de 0,69 veces en la probabilidad de morir por cáncer. La protección es más fuerte en pacientes inicialmente tratadas en etapa I, sometidas a mastectomía y las de mayor edad (Lash, 2007). Las recurrencias sólo mamográficas son de menor tamaño (Orel, 1993). El uso de mamografía de seguimiento decae con el tiempo, especialmente en pacientes con comorbilidades o tratadas con mastectomía (Doubeni, 2006). El riesgo contralateral es bajo y cuando ocurre no se afecta la sobrevida global (Fisher, 1984).
Nivel de evidencia II.
Recomendación:
- Primera mamografía un año después de la mamografía que condujo al diagnóstico, pero no antes de 6 meses de terminada la radioterapia local. Luego, una mamografía anual.
3. ¿Cuánto tiempo se debe extender el seguimiento?
Síntesis de la evidencia:
El seguimiento se debería extender por largo tiempo, probablemente de por vida (EBCTCG, 2005; Hayes, 2007).
Nivel de evidencia I.
Adquiere especial relevancia en la detección de recurrencias locales o primarios contralaterales luego de pasados los 5 primeros años después del tratamiento sin la aparición de enfermedad metastásica (Schootman, 2008; Burstein, 2000; Stierer, 1989). El riesgo de recurrencia local o un primario contralateral es estable en el tiempo (Jatoi, 2005). El 50% de las pacientes que desarrollarán metástasis ocurren en los primeros 5 años cuando RE- y en los primeros 10 años cuando RE+ (Kattlove, 2003).
Nivel de evidencia II.
Recomendación:
- Seguimiento anual con mamografía en pacientes asintomáticas sin límite de edad, salvo decisión basada en criterio clínico.
4. ¿Quién puede realizar el seguimiento?
Síntesis de la evidencia:
La mayoría de las pacientes tratadas por un cáncer de mama sobreviven largo tiempo o se curan de su enfermedad (Hayes, 2007). Eso produce un gran número de pacientes que deben ser seguidas por mucho tiempo. En los sistemas en que se produce una sobrecarga de los recursos especializados se podría entrenar a médicos generales para realizar el seguimiento específico y esto tendría buenos resultados; ensayos aleatorios no han encontrado diferencias en pronóstico con seguimiento por especialista o médico de familia especialmente entrenados para este propósito (Grunfeld, 1999; Grunfeld 2006).
Nivel de evidencia I.
Recomendación:
- Seguimiento por equipo médico multidisciplinario especializado o por personal médico general especialmente entrenado para este propósito.
5. ¿Cómo influyen las mutaciones BRCA en el seguimiento?
Síntesis de la evidencia:
La presencia de mutaciones de BRCA aumenta el riesgo de recurrencia local y de cáncer contralateral. Además, están asociadas a mayor riesgo de desarrollar cáncer de ovario y próstata (Struewing, 1997; Modan, 2001).
Nivel de evidencia II.
Recomendaciones:
- Ooforectomía luego de completar la paridad en pacientes portadoras de mutaciones de BRCA disminuye la ocurrencia de cáncer de mama y cáncer de ovario.
- Considerar mastectomía profiláctica en pacientes portadoras de mutaciones de BRCA.
- Resonancia magnética de seguimiento en pacientes asintomáticas portadoras de mutaciones de BRCA.
- Estudio de familiares relacionados a pacientes portadoras de mutaciones de BRCA. Inicio de screening mamográfico a los 25 años o 10 años antes de la edad del caso índice.
6. ¿Cuáles son las complicaciones alejadas del tratamiento?
Síntesis de la evidencia:
El seguimiento debe considerar la detección de complicaciones alejadas del tratamiento como: bochornos y síntomas relacionados a la deprivación de estrógenos (Grunfeld, 2005); osteoporosis y su asociación con inhibidores de aromatasa (Brown, 2002; Perez, 2006; Hillner, 2003; Bundred, 2008); linfedema de brazo en pacientes sometidas a una disección axilar, especialmente si se ha asociado radioterapia a la axila y a la fosa supraclavicular (prevalencia entre 10% y 40%); alza de peso en relación a la quimioterapia y el tratamiento adyuvante que induce menopausia; alteraciones cognitivas y neoplasias hematológicas secundarias a quimioterapia (Ahles, 2002).
Nivel de evidencia I-II.
Recomendaciones:
- Evaluación de osteoporosis con densitometría ósea. Ingesta de 1,5 gr de calcio al día y ejercicio físico rutinario. Eventual tratamiento farmacológico de osteoporosis progresiva con bifosfonatos, especialmente cuando se usan inhibidores de aromatasa.
- Para las pacientes que recibieron quimioterapia con antraciclinas, especialmente las sometidas a esquemas dosis-densas, existe mayor riesgo de desarrollar leucemias agudas o mielodisplasias. Sólo se recomienda seguimiento con hemogramas cuando existen síntomas de anemia, trombocitopenia o infecciones frecuentes.
7. ¿Cuál es el seguimiento ginecológico adecuado?
Síntesis de la evidencia:
En pacientes asintomáticas que se encuentran tomando tamoxifeno, el uso de ecografía transvaginal de rutina se asocia a un alto índice de falsos positivos, produce procedimientos innecesarios y no se recomienda su uso en ausencia de metrorragia (Geber, 2000). En ausencia de síntomas específicos basta el examen ginecológico anual (Khatcheressian, 2006).
Nivel de evidencia II.
Recomendaciones:
- Un examen ginecológico anual en pacientes asintomáticas que toman tamoxifeno, y uso de ecografía transvaginal para evaluación del endometrio cuando exista metrorragia en pacientes postmenopáusicas. Educación acerca de los síntomas de trombosis venosa profunda y embolia pulmonar.
8. ¿Se puede usar terapia de reemplazo hormonal (TRH)?
Síntesis de la evidencia:
En una revisión sistemática de estudios observacionales para cuantificar el riesgo de recurrencia de cáncer de mama relacionado con TRH, se estimó que el uso de TRH no parece aumentar el riesgo de recurrencia de un cáncer de mama tratado (Col, 2001). En un estudio de casos y controles, se observó una menor recurrencia y mortalidad por cáncer de mama en las pacientes USUARIAS de TRH (O´Meara, 2001).
Nivel de evidencia II.
Por otro lado, el estudio WHI confirmó el aumento de riesgo de desarrollar cáncer de mama en TRH con asociación de estrógenos + progestinas (Rossouw, 2002; WHI Group). En estudios aleatorios que evalúan el riesgo de recurrencia de cáncer en pacientes postmenopáusicas al momento del tratamiento de su cáncer mamario, tratadas con tamoxifeno o inhibidores de aromatasa, tanto el uso de estrógenos + progestinas se asoció a mayor riesgo de recurrencia (Holmberg, 2008; HABBITS Study Group), como también el uso de tibolona se asoció a mayor riesgo de recurrencia de cáncer mamario (Kenemans, 2009; LIBERATE Study Group).
Nivel de evidencia I.
Recomendación:
- El uso de terapias de reemplazo hormonal o tibolona NO está recomendado y se debe evitar luego del tratamiento de pacientes con cáncer de mama. Su uso debe considerar la total participación de la paciente adecuadamente informada.
9. ¿En qué consiste el seguimiento luego de una mastectomía total?
Síntesis de la evidencia:
Cuando se ha realizado una mastectomía total con o sin reconstrucción, la probabilidad de una recurrencia local está asociada al uso de radioterapia postoperatoria. La ausencia de este tratamiento se relaciona con una mayor probabilidad de recurrencia local en las pacientes con tumores de mayor tamaño, un recuento mayor de linfonodos con metástasis, los tumores con RE- y un recuento bajo de linfonodos en la pieza de disección axilar (Recht, 1999).
Nivel de evidencia I.
Recomendación:
- Seguimiento clínico con examen físico cuidadoso, sin uso de imágenes.
10. ¿Se puede recomendar el uso de mastectomía contralateral profiláctica (MCP), en ausencia de mutaciones de BRCA?
Síntesis de la evidencia:
Estudios descriptivos han mostrado que el uso de MCP se casi triplicó en Estados Unidos en un período de 6 años, especialmente para las pacientes cuyo primario requirió una mastectomía, para las pacientes más jóvenes, para las tratadas por un cáncer lobulillar invasor, y para las pacientes con diagnóstico anterior de cáncer mamario (Tuttle, 2007). El grado de satisfacción de las pacientes que optan por esta decisión es, en general, adecuado. La insatisfacción se asocia a las complicaciones derivadas de los procedimientos reconstructivos (Frost, 2005).
Nivel de evidencia III.
Recomendación:
- El uso de MCP en ausencia de mutaciones de BRCA debe ser balanceado contra el riesgo futuro de desarrollar un nuevo cáncer contralateral.
- La disponibilidad de alternativas de reconstrucción mamaria facilita la decisión de MCP.
- Se debe educar a las pacientes respecto de los beneficios y contratiempos asociados a esta decisión.
11. ¿Qué impacto tienen las guías para el seguimiento de pacientes tratadas por cáncer de mama?
Síntesis de la evidencia:
Existe una gran dispersión en los criterios para el seguimiento de las pacientes tratadas por un cáncer de mama con intención curativa. El uso rutinario de múltiples exámenes de laboratorio e imágenes como práctica habitual en los estudios clínicos controlados hizo extender esa costumbre hacia la práctica médica habitual. Luego de la comprobación de la inutilidad de estos procedimientos fuera de estudios clínicos controlados, ha sido difícil la erradicación de esta costumbre que aumenta enormemente los gastos en salud sin beneficio clínico alguno demostrado. La incorporación de guías clínicas de seguimiento producen una homogenización de la conducta médica y una disminución importante de los costos de salud relacionados (Mille, 2002).
Nivel de evidencia III.
Recomendación:
- Desarrollo, difusión e implementación de guías clínicas para el seguimiento de pacientes tratadas con intención curativa por un cáncer de mama, fuera de estudios clínicos.
12. ¿Qué estudios no se deben hacer en pacientes asintomáticos?
Síntesis de la evidencia:
Las pacientes con cáncer de mama que participan de protocolos de investigación son sometidas a numerosas evaluaciones periódicamente. Estas evaluaciones son parte del sistema de registro de eventos adversos y del registro de eventos de enfermedad y son parte integral inevitable en los estudios actuales. La extensión de esta práctica dentro de los protocolos de investigación a la práctica clínica habitual no debería ocurrir, debido a que esta última no requiere de la pesquisa de eventos adversos en paciente asintomáticos. En ellos basta con un examen físico adecuado, la educación respecto de síntomas relevantes y una mamografía de buena calidad (Hayes, 2007; Khatcheressian, 2006).
Nivel de evidencia II.
Recomendación:
Exámenes NO recomendados en pacientes asintomáticos:
- Hemograma
- Pruebas hepáticas
- Radiografía de tórax
- Cintigrama óseo
- Ecografía abdominal
- Tomografía computada
- PET-CT
- Resonancia magnética de mamas (en ausencia de mutación de BRCA)
- Marcadores tumorales (CA 15-3, CA 27,29, CEA, etc.)
- Ecografía transvaginal en ausencia de metrorragia
- Biopsia endometrial en ausencia de metrorragia
Notas y agradecimientos
Este artículo fue redactado en su versión final después de haber recibido las contribuciones y comentarios de los delegados que asistieron a la III Jornada Nacional de Diagnóstico y Tratamiento de Cáncer de Mama, realizada en Coquimbo, Chile, en agosto de 2009. A su vez, las ponencias que se presentaron en esa jornada fueron la síntesis del artículo completo de revisión de la literatura y trabajo previo de la comisión correspondiente. Este trabajo de formulación duró un año, comenzó en junio de 2008 y se llevó a cabo bajo la asesoría de Medwave Estudios Ltda., en el marco del proyecto denominado “Asesoría en la Formulación de Consenso y Recomendaciones en Cáncer de Mama Basados en la Evidencia”. El financiamiento para la ejecución de la asesoría provino de la Sociedad Chilena de Mastología.
La coordinación de la asesoría fue realizada por Vivienne Bachelet; el metodólogo jefe fue Miguel Araujo; y la metodóloga adjunta fue Gabriela Moreno. Colaboró en la sistematización bibliográfica y en el formato final de los documentos, Matías Goyenechea. El artículo definitivo es el resultado del trabajo final presentado a las jornadas de consenso, donde fue conocido, revisado y discutido por los concurrentes, y luego fue revisado por un comité editorial de pares constituido por la misma Sociedad Chilena de Mastología, tras lo cual fue enviado a Medwave para su publicación.

