Consenso
← vista completaPublicado el 7 de septiembre de 2020 | http://doi.org/10.5867/medwave.2020.08.8012
Reduciendo el impacto de COVID-19 sobre la radioterapia oncológica en países en desarrollo: revisión rápida y consenso de expertos
Reducing the impact of COVID-19 on radiation oncology units of developing countries: A rapid review and expert consensus
Resumen
Objetivo Establecer recomendaciones para la toma de decisiones de manejo en radioterapia durante la pandemia de COVID-19, adaptadas a un país con recursos de salud limitados.
Métodos A través de una revisión rápida de la literatura se buscaron publicaciones que describieran medidas para reducir el riesgo de infección por COVID-19, así como también pautas de manejo para reducir la carga de trabajo en las unidades de radioterapia. Se incluyeron en el alcance de esta revisión las siguientes patologías: tumores ginecológicos, cáncer de mama, tumores gastrointestinales, tumores genitourinarios, tumores de cabeza y cuello, cáncer de piel, tumores del sistema nervioso central y linfomas. Un grupo de expertos discutió en línea los datos extraídos y redactó las recomendaciones. Mediante un método Delphi modificado, se evaluó el consenso entre 14 radio-oncólogos certificados. Se evaluó la calidad de la evidencia que sustentó las recomendaciones sobre esquemas de tratamiento.
Resultados Se incluyeron un total de 57 documentos. De 25 trabajos se extrajeron las estrategias para reducir el riesgo de infección. De los restantes, se obtuvieron las recomendaciones para cada patología. Las recomendaciones están orientadas a establecer escenarios específicos donde se pueden omitir, diferir, priorizar y acortar los tratamientos. En el ítem de acortar se recomiendan esquemas de tratamiento para cada patología, priorizando los esquemas hipofraccionados cuando fue posible.
Conclusión Se plantean estrategias para la gestión de los servicios de radioterapia con el objetivo de garantizar que los tratamientos de alta calidad para pacientes oncológicos sigan entregándose, pese a la crisis sanitaria ocasionada por COVID-19.
Ideas clave
- Asegurar la entrega de tratamientos de radioterapia en las circunstancias adversas en las que la pandemia por COVID-19 ha colocado a los sistemas sanitarios, es un reto en el manejo del paciente con cáncer.
- Debido a la característica emergente de la pandemia, no están disponibles estudios que permitan sustentar las recomendaciones con el nivel de evidencia más deseable para la toma de decisiones.
- Este trabajo cuenta con las limitantes vinculadas a datos clínicos restringidos; inclusión de documentos publicados a través de procesos editoriales abreviados, sin el rigor metodológico deseable para la toma de decisiones; evaluación formal de la calidad de la evidencia de las recomendaciones de esquemas de tratamiento, y evaluación global de la calidad para el resto de las recomendaciones, entre otras.
- Todas estas limitaciones deben considerarse a la hora de implementar las recomendaciones.
Introducción
Desde que la Organización Mundial de la Salud, OMS, declaró la enfermedad por coronavirus 2019 (COVID-19) como una pandemia global, en marzo de 2020, esta se ha extendido rápidamente por el mundo[1]. Según la OMS actualmente en América Latina y El Caribe, la epidemia está más activa con respecto a otras regiones con 2,7 millones de contagios y más de 121 900 muertes, siendo la segunda zona del mundo con más casos detectados de la enfermedad. Ecuador es uno de los países más afectados de la región, con más de 61 000 casos confirmados y 4770 fallecidos distribuidos en todas las provincias[1]. Se ha calculado que en Ecuador la tasa de mortalidad por COVID-19 es de 19,5 por 100 000 habitantes, una de las más altas de la región[2].
La pandemia ha afectado severamente a los sistemas de salud a nivel mundial y esto inevitablemente tendrá consecuencias en la atención de pacientes oncológicos. No se sabe qué efecto tendrán las demoras en el inicio de los tratamientos sobre la supervivencia a largo plazo de esta cohorte, así como tampoco se sabe por cuánto tiempo se mantendrán estos retrasos[3]. Además, la propia malignidad y las terapias anticancerígenas convierten a estos pacientes en un grupo vulnerable frente a la infección. Cohortes retrospectivas han reportado que los pacientes oncológicos tienen tasas de mortalidad por COVID-19 tres veces más altas que los pacientes sin cáncer, así como también mayor probabilidad de requerir cuidados intensivos, mayor riesgo de eventos severos y mayor posibilidad de necesitar ventilación mecánica invasiva[4],[5].
La radioterapia tiene un papel crucial en el tratamiento de la mayor parte de pacientes con cáncer[6]. Asegurar la atención durante la pandemia sin interrupciones prolongadas, reduciendo el riesgo de infección en pacientes y personal, en medio de una restricción de recursos; es un problema al que se enfrentan muchos departamentos de radio-oncología.
Este trabajo tiene como objetivo realizar una revisión rápida de la evidencia disponible sobre medidas para reducir el riesgo de infección por COVID-19 en las unidades de radioterapia, y estrategias para priorizar la atención de los pacientes oncológicos. Su finalidad es establecer recomendaciones sobre la entrega del tratamiento de radioterapia durante la pandemia, adaptadas a un país con recursos limitados.
Métodos
Definición del alcance y búsqueda de la literatura
En un protocolo escrito a priori se definió el alcance de la revisión, enfocada en pacientes que reciben tratamiento de radioterapia durante la pandemia de COVID-19, buscando:
1) Estrategias para reducir el riesgo de infección de los pacientes y del personal.
1) Sistemas de categorización para priorización del tratamiento de radioterapia.
2) Esquemas de tratamiento para omitir, diferir y acortar el tratamiento en las patologías más frecuentes en el país: tumores ginecológicos, cáncer de mama, tumores gastrointestinales, tumores genitourinarios, tumores de cabeza y cuello, cáncer de piel, tumores del sistema nervioso central, linfomas y manejo paliativo.
Estas patologías fueron establecidas como prioritarias por el grupo de expertos en función de la frecuencia de su presentación y perfil epidemiológico de las distintas unidades de radioterapia del país.
Se realizó una búsqueda mediante la combinación de términos en vocabulario controlado y no controlado en MEDLINE a través de PubMed, actualizada al 6 de abril de 2020. Los términos usados fueron: "COVID-19", "COVID", "coronavirus", "radiotherapy", "radiation". Se buscaron artículos adicionales en los repositorios de la American Society of Radiation Oncology/European Society for Radiotherapy and Oncology, ASTRO/ESTRO y la Royal College of Radiologist, donde dichas instituciones compilaron documentos relacionados con COVID-19 y radioterapia.
También se revisaron las referencias de los manuscritos incluidos y se solicitó al grupo de expertos que recomendaran documentos relevantes.
Selección de los estudios
Un revisor determinó la elegibilidad de los documentos por título y resumen. Un segundo revisor verificó el 20% de los documentos tamizados, para comprobar la elegibilidad. Finalmente, otro revisor evaluó la elegibilidad de los artículos en texto completo.
Se incluyeron documentos que emitan estrategias y recomendaciones para el manejo de pacientes que reciben tratamiento en las unidades de radioterapia durante la pandemia por COVID-19. Debido a la característica emergente de este escenario, se previó la falta de guías de práctica clínica con recomendaciones con los mejores niveles de evidencia, y la falta de revisiones sistemáticas. Por estas razones se incluyeron opiniones de expertos, experiencias, comunicaciones cortas, guías clínicas y protocolos institucionales. Se incorporaron también declaraciones de posición de instituciones académicas y gubernamentales publicadas en sus respectivas páginas web. Se incluyeron sólo aquellos documentos publicados en inglés y español. Se excluyeron los documentos con recomendaciones específicas sobre patologías fuera del alcance de esta revisión.
Extracción de datos
Un revisor extrajo el tipo de estudio, país de procedencia, tópico y ámbito de las recomendaciones. Los categorizó según si daban solución a algunos de los aspectos señalados previamente. Posteriormente, dos revisores extrajeron individualmente las estrategias o intervenciones propuestas en cada documento en una hoja de extracción de datos preestablecida. Cuando el grado de discrepancias en la extracción de los datos fue mayor al 60%, un tercer revisor resolvió tales discrepancias.
A un grupo se les pidió que extrajeran las medidas propuestas para reducir la transmisión del virus en las unidades de radioterapia. Una vez discutidas en el grupo, estas fueron evaluadas por dos expertas en microbiología, quienes individualmente determinaron si técnicamente eran adecuadas.
Para las recomendaciones por grupo de patología se utilizó el enfoque RADS (por sus siglas en inglés, Remote Visits, Avoid Radiation, Defer Radiation, Shorten Radiation)[7]. Para cada patología se les pidió extraer recomendaciones que respondan a las siguientes preguntas:
1) ¿En qué pacientes se puede omitir el tratamiento de manera segura?
2) ¿En qué pacientes se puede diferir el tratamiento y por cuánto tiempo?
3) ¿Qué pacientes deben recibir tratamiento prioritario?
4) ¿Cuál sería la técnica de tratamiento preferida y en qué fraccionamiento?
5) ¿Se justifica el uso de compensación de dosis en caso de suspensiones prolongadas de tratamiento?
Las recomendaciones se compilaron en una sola hoja y fueron entregadas a los grupos de expertos para su discusión. Se les solicitó que consideraran un escenario en el que la pandemia duraría varios meses, con una proporción significativa no disponible de personal y en un sistema sanitario colapsado, lo que limitaría los recursos.
Evaluación de la calidad de la evidencia
Se evaluó la calidad de la evidencia de las recomendaciones sobre esquemas de tratamiento utilizando el método descrito por Varker y colaboradores[8]. Este considera los niveles de evidencia según el Centro de Medicina Basada en Evidencia (Center for Evidence-Based Medicine, CEBM, por sus siglas en inglés), el riesgo de sesgo de los estudios y la consistencia de los hallazgos. Se calificó como alta calidad de la evidencia si uno o más estudios de nivel I con bajo riesgo de sesgo o tres o más estudios de nivel II con bajo riesgo de sesgo, sustentan la recomendación. Se señaló como moderada calidad, cuando uno o dos estudios de nivel II con bajo riesgo de sesgo o dos o más estudios de nivel III con bajo riesgo de sesgo y hallazgos consistentes, fundamentan la recomendación. Se consideró de baja calidad cuando uno o más estudios de nivel I al IV con un alto riesgo de sesgo, sustentan la recomendación.
Un revisor evaluó la calidad de la evidencia de cada recomendación sobre esquemas de tratamiento.
Desarrollo del consenso
El grupo de consenso estuvo conformado por 14 radio-oncólogos certificados pertenecientes a siete unidades de radioterapia del país. Se emitieron invitaciones dirigidas para lograr la inclusión de una muestra representativa que permitiera contar con médicos especialistas en radioterapia de las distintas ciudades del país, con diferentes grados de experticia, especializados en varios campos de la especialidad y con equidad de género.
Para la elaboración del consenso se siguió el enfoque de Delphi modificado por la American Society of Clinical Oncology, ASCO[9]. En la primera ronda se solicitó a los miembros del grupo que calificaran el acuerdo con cada recomendación en una escala Likert de cinco puntos, que va desde muy de acuerdo a muy en desacuerdo, mediante encuesta en línea. El formulario de calificación incluyó un espacio para comentarios. Para cada pregunta se calculó el porcentaje de acuerdo y el puntaje promedio. El porcentaje de acuerdo se refiere al número de evaluadores que indicaron estar de acuerdo o totalmente de acuerdo, dividido por el número total de evaluadores. No se incluyeron los no respondedores en el denominador. Se definió consenso con un acuerdo del 80% y un puntaje promedio de 1 o 2[9]. Para todas las recomendaciones, los resultados detallados de las rondas de consenso se proporcionarán bajo requerimiento, junto con las opiniones discrepantes.
Al completar la primera ronda de calificaciones, cinco miembros del grupo de expertos discutieron los resultados, abordaron los comentarios y revisaron las recomendaciones que no alcanzaron el umbral de consenso. Posteriormente se solicitó a todo el grupo de consenso calificar su acuerdo con la recomendación revisada. Los miembros del grupo recibieron la iteración previa de las recomendaciones, la distribución de calificaciones y las recomendaciones revisadas. No se revaloraron las recomendaciones que alcanzaron el acuerdo en la primera ronda. Los resultados se reportan de manera narrativa, describiendo la recomendación, la fuente y el grado de consenso.
Resultados
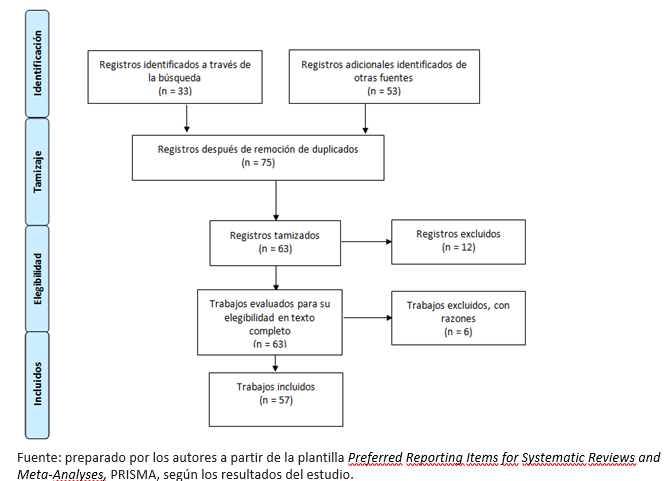
Se incluyeron un total de 57 documentos. Las características de los documentos incluidos se pueden observar en la Tabla 1 del material suplementario. El diagrama de flujo del proceso de inclusión se puede observar en la Figura 1.
 Tamaño completo
Tamaño completo De los 57 documentos, 25 aportaron estrategias para reducir la transmisión del virus[10],[11],[12],[13],[14],[15],[16],[17],[18],[19],[20],[21],[22],[23],[24],[25],[26],[27],[28],[29],[30],[31],[32],[33],[34]; nueve incluyeron recomendaciones para cáncer de cabeza y cuello[22],[23],[26],[27],[35],[36],[37],[38],[39]; 13 para tumores gastroinestinales[22],[26],[27],[38],[40],[41],[42],[43],[44],[45],[46],[47],[48]; nueve para tumores genitourinarios[7],[22],[23],[26],[27],[36],[38],[49],[50]; diez para tumores ginecológicos[22],[23],[26],[27],[36],[38],[51],[52],[53],[54]; tres para linfomas[22],[26],[27]; 13 para cáncer de mama[22],[23],[26],[27],[36],[38],[55],[56],[57],[58],[59],[60],[61]; cinco para tumores del sistema nervioso central [22],[26],[27],[38],[62]; tres para cáncer de piel[22],[26],[27] y seis para paliativos[22],[26],[27],[38],[59],[63]. Catorce radio-oncólogos certificados, pertenecientes a siete unidades de radioterapia del país, contribuyeron en las discusiones en línea y votaron a través de encuestas electrónicas.
Estrategias para reducir la transmisión del virus
Las estrategias están orientadas a reducir la probabilidad de infección en pacientes y personal, cubriendo los problemas que pueden presentarse en un departamento de radioterapia. Para su implementación se debe hacer un análisis en cada centro basado en las circunstancias y recursos disponibles, los protocolos establecidos en cada hospital, así como la normativa vigente establecida por el Ministerio de Salud Pública.
Estas medias se han clasificado en las siguientes categorías:
1. Sistemas de triaje
- Establecer un punto de triaje en el ingreso al hospital que indague sobre sintomatología respiratoria alta, control de temperatura, historial de viaje y contacto con casos confirmados[10],[13],[14],[15],[16],[17],[18],[19],[20],[23].
- Se recomienda un triaje clínico adicional en el ingreso al servicio, en las unidades donde existan los recursos para hacerlo[14],[15],[18],[19],[24].
- Telefonear a los pacientes antes de la simulación y del primer día de tratamiento para averiguar sobre síntomas respiratorios, si ha sido diagnosticado o ha tenido contacto cercano con caso positivo de COVID-19[10],[15],[22],[23].
- Enviar a los pacientes con sospecha de COVID-19 para valoración en emergencia o unidad especializada y toma de muestra, registro y notificación del caso. Diferir su cita o inicio de tratamiento. Para definir responsables de este proceso, se deberán seguir los protocolos de manejo de casos sospechosos de cada hospital[10],[14],[15],[17],[18],[23].
- Diferir por al menos 14 días la simulación o inicio de tratamiento en pacientes que hayan estado en contacto cercano con un caso de COVID-19 confirmado o probable en los últimos 14 días. El Ministerio de Salud Pública establece como contacto cercano: exposición por más de 15 minutos de contacto cara a cara o más de dos horas en un espacio cerrado, incluye el domicilio[14],[19],[23].
- Tomar la temperatura del personal a la llegada a la unidad y luego del almuerzo, manteniendo un umbral de 37,5 grados Celsius[10],[13],[14],[16],[17],[19].
- Indagar por síntomas respiratorios altos entre el personal[14],[15],[16],[17],[22].
- No deberá asistir el personal con síntomas respiratorios altos o temperatura mayor a 37,5 grados Celsius[10],[17],[22].
- Cumplir con las reglas nacionales de retorno de viaje y auto-aislamiento[10],[22].
2. Medidas generales de higiene
- Lavarse las manos 20 segundos como mínimo antes y después de posicionar a los pacientes, después de manipular implementos, cuando las manos estén visiblemente sucias y regularmente durante el día. Si no tienen cerca un lavabo, se podría usar alcohol gel[10],[13],[14],[15],[16],[17],[18],[19].
- Limpiar regularmente todas las superficies de contacto de alto volumen, incluidos mostradores, teléfonos celulares, interruptores de luz, grifos e inodoros, perillas de puertas y los teclados, de acuerdo con las instrucciones del fabricante y las políticas de cada institución[10],[17],[22].
- Reducir el uso de teléfonos móviles cuando se está en contacto con pacientes y superficies. Desinfectarlo frecuentemente con alcohol al 70%[10].
- Proveer de dispensadores de alcohol gel, pañuelos antisépticos y medidas informativas en las salas de espera de pacientes[15],[18],[22],[23].
3. Uso de equipos de protección personal
- Los técnicos de radioterapia que interactúan con un gran volumen de pacientes, deben usar rutinariamente mascarillas quirúrgicas[13],[24],[25],[26],[27],[28],[29],[30],[31],[33],[34].
- Cuando la examinación de faringe y cavidad oral sean estrictamente necesarias, deberán realizarse con mascarilla N95 o equivalentes, gafas y guantes[10].
- El personal en contacto con pacientes sospechosos o confirmados deben usar mascarilla N95, o FFP2 o FFP3 estándar o equivalentes[19],[28],[32].
- Pacientes y acompañantes deberán usar obligatoriamente mascarilla quirúrgica[14],[16],[17],[18],[21].
- Paciente con sintomatología respiratoria, pero con condición clínica respiratoria preexistente recogida en el historial clínico, debe acudir con mascarilla quirúrgica y continuar tratamiento[16].
- Hacer uso racional del equipo de protección, en concordancia con los protocolos de cada institución[14],[15],[16],[18],[19].
4. Medidas de distanciamiento social
- Evitar cualquier reunión presencial, preferir herramientas electrónicas[10],[13],[14],[16],[21],[22].
- Cuando las reuniones sean inevitables, permitir máximo cinco personas con 1,5 metros de separación entre ellas[15],[17].
- Evitar al máximo los acompañantes de los pacientes, excepto cuando estos requieran asistencia[10],[13],[17],[22].
- El paciente debe permanecer en la sala de espera el menor tiempo posible, cumpliendo estrictamente los horarios de los aceleradores[20],[25],[26].
- Diferenciar tres zonas en el servicio: contaminada, semicontaminada y limpia[13],[19],[21].
- En áreas comunes, el personal deberá conservar una distancia de al menos 1,5 metros entre sí[13],[17],[22].
- En la sala de espera los pacientes deben sentarse a una distancia de al menos 2 metros (o por lo menos una silla entre pacientes)[32].
- Dar prioridad al tratamiento de niños, para disminuir el tiempo de estancia en las salas de espera[25],[27],[29],[31],[32],[34].
- Restringir la movilización del personal en el hospital y entre hospitales[10],[19].
5. Limpieza y desinfección de dispositivos de inmovilización y aceleradores
- Desinfectar los inmovilizadores de uso compartido con alcohol al 70% después de cada tratamiento de radioterapia[14],[18],[25],[27],[29],[32],[34].
- Evitar el uso de cualquier dispositivo que no pueda ser desinfectado adecuadamente[15].
- Desinfectar dispositivos como máscaras termoplásticas con alcohol al 70%, luego de cada tratamiento y almacenar por separado las de pacientes con sintomatología respiratoria[18],[22],[23],[25],[27],[28],[32],[34].
- Desinfectar los dispositivos de inmovilización personalizados tales como bolsas al vacío o cunas α después de cada tratamiento con un desinfectante de base alcohólica, aplicado con un paño suave (consulte las instrucciones del fabricante). Evite aerosoles, blanqueadores, solventes o detergentes abrasivos[15],[16].
- Guardar las máscaras termoplásticas y bolsas al vacío en fundas plásticas individuales, luego de cada uso[15],[16],[28].
- Desinfectar luego de cada tratamiento las superficies del acelerador que entren en contacto con el paciente, con sustancias de base alcohólica y según las especificaciones técnicas del fabricante[14],[24],[26],[29],[31].
- Se recomienda aseo del piso al menos tres veces al día y cuando esté visiblemente sucio[24],[25].
- Limpiar áreas comunes como sala de espera o vestidores al menos dos veces al día[27].
- Aplicar desinfección terminal a todas las áreas después de finalizar los tratamientos programados[32].
6. Reorganización del trabajo
- Para reducir el riesgo de exposición, hay que considerar la división del personal en dos grupos de trabajo rotativo que no tengan contacto entre sí, para preservar una reserva de proveedores de atención[10],[13],[14],[15],[19],[21],[22],[23].
- Organizar el trabajo, para que un grupo acuda al servicio y el otro pueda trabajar en la planificación remota de los tratamientos[13],[14],[15],[16],[18],[19],[32].
- Mantener el mínimo número de personal necesario trabajando en la unidad[15],[18],[21],[22],[23].
- Si una persona del grupo se confirma como caso positivo, considerar que todo el grupo pudiese ir a cuarentena de 14 días[14],[19].
- Identificar al personal que podría realizar trabajo remoto, garantizando la calidad de la atención[10],[18],[22],[23].
- Gestionar actividades para hacer posible la planificación remota de tratamientos[26],[32],[34].
- Realizar reuniones clínicas o de trabajo vía video conferencia[10],[13],[15],[16],[17],[20],[23].
- Mantener el servicio de consulta externa al mínimo, solo para pacientes en tratamiento activo o nuevos[10],[14],[15],[16],[17],[22].
- Diferir controles de pacientes subsecuentes o en seguimiento[20],[21],[23],[30],[34].
- Adaptar los esquemas para tener el mínimo de consultas posibles durante el tratamiento[10],[16],[21],[22].
- Realizar seguimiento vía telefónica y/o por telemedicina de pacientes que culminaron tratamiento sin toxicidad y con dificultad en la movilidad para acudir a control[24],[25],[26],[28],[29],[30],[31].
- Cancelar los controles semanales a pacientes sin toxicidad radioinducida[31].
- Llamar por teléfono a pacientes de seguimiento, para solicitar resultados de exámenes y modificar fecha de cita hasta después de la emergencia[17],[22],[23].
7. Medidas para personal de física médica
- Priorizar tareas esenciales y urgentes, posponiendo aquellas tareas que pueden tolerar demoras[32].
- Los controles de calidad anuales podrían ser pospuestos por tres o cuatro meses[31],[32],[33],[34].
- Asegurar la disponibilidad de un grupo de físicos para los controles de calidad de aceleradores y dosimetrías urgentes[17],[22],[23].
- El personal de física médica amerita de una segregación estricta para garantizar que no haya contaminación cruzada. Para esto se debe dedicar diferentes salas a los médicos para contornear y a los físicos para la planificación del tratamiento, en donde haya disponibilidad de espacio físico[17],[31],[32],[33],[34].
- El personal se debería organizar en turnos de trabajo separados, para minimizar la exposición en un espacio cerrado como las sala de planificación, en donde haya disponibilidad de espacio físico[31],[32],[33],[34].
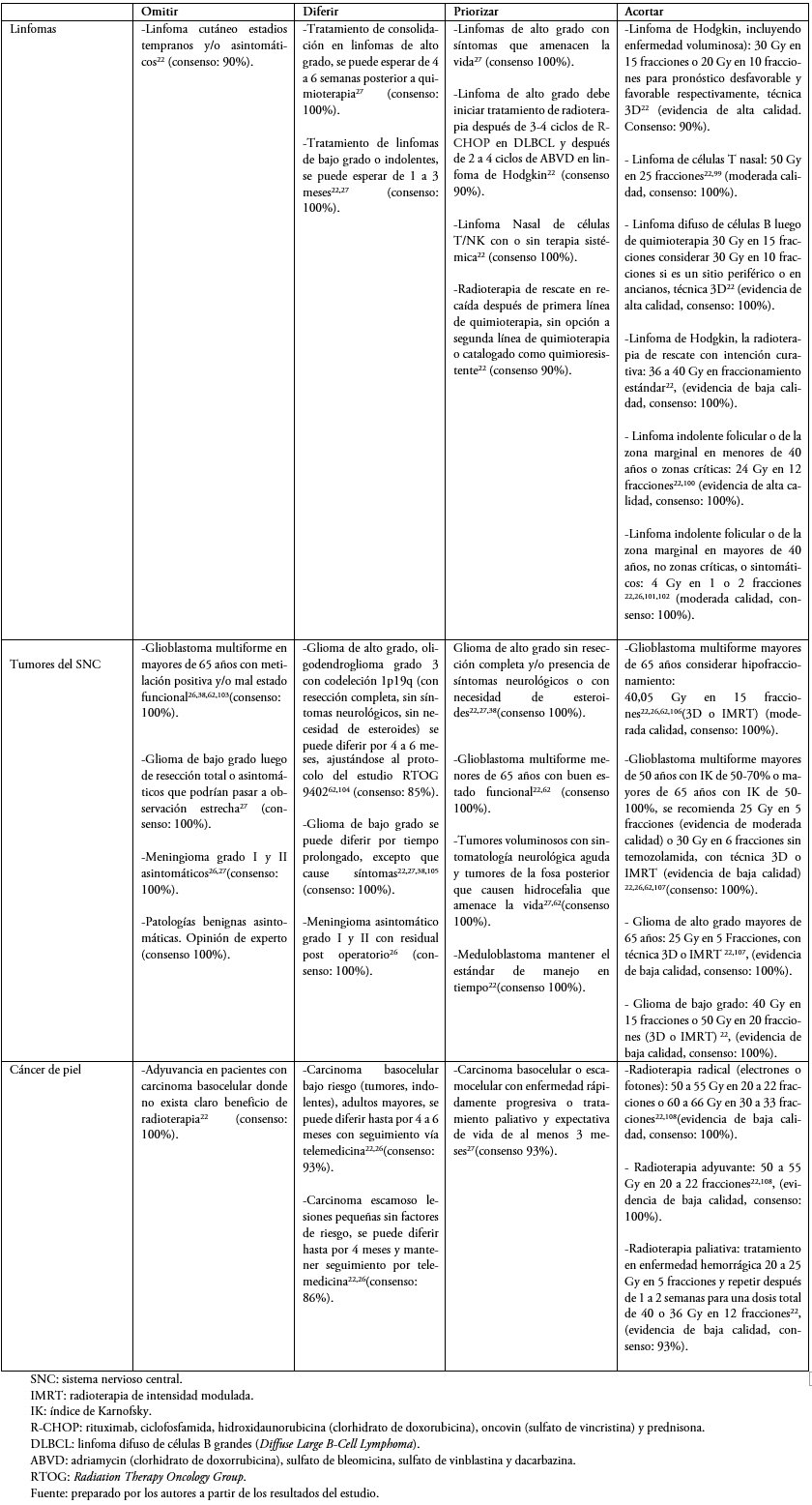
Recomendaciones por patología
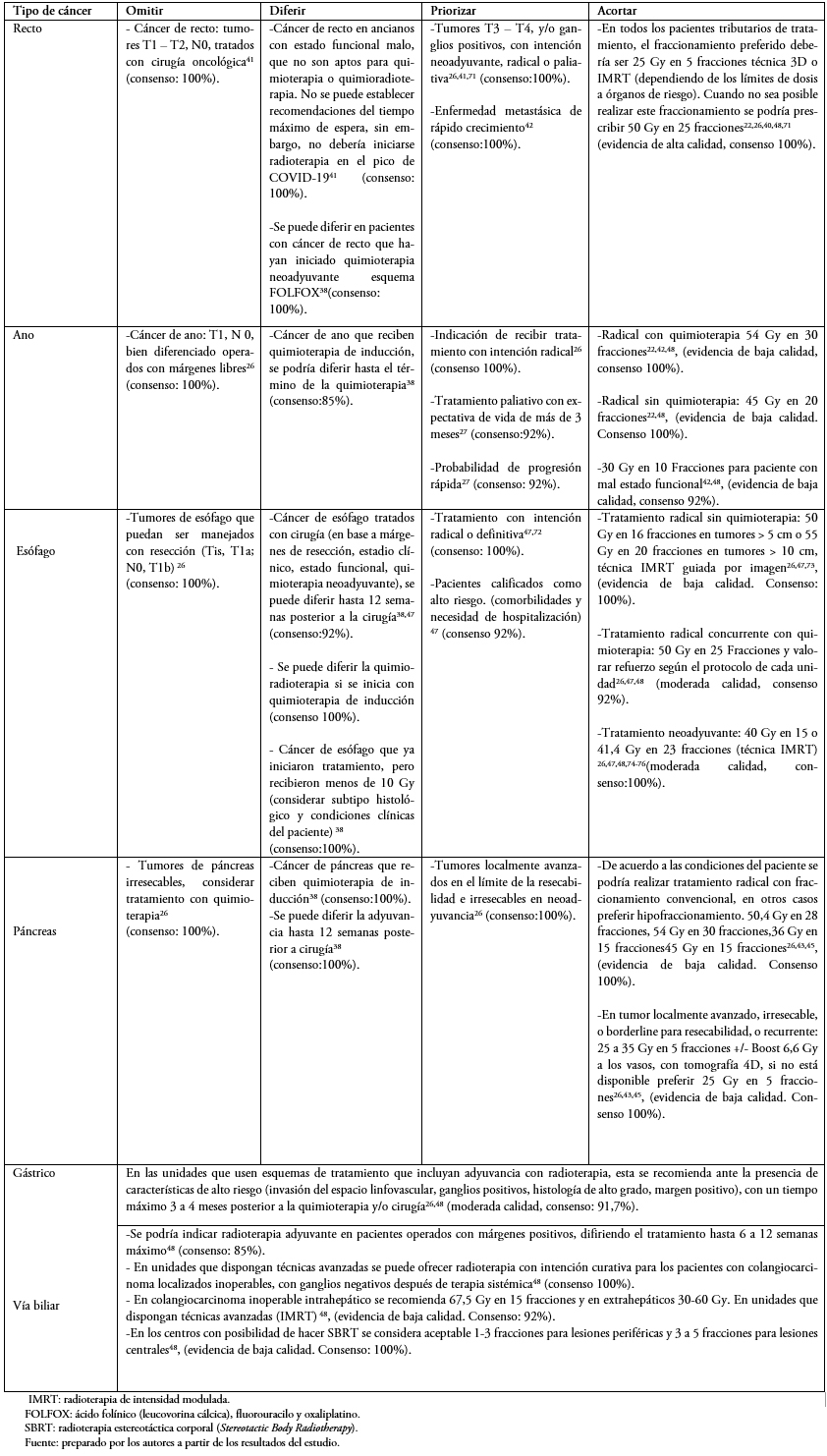
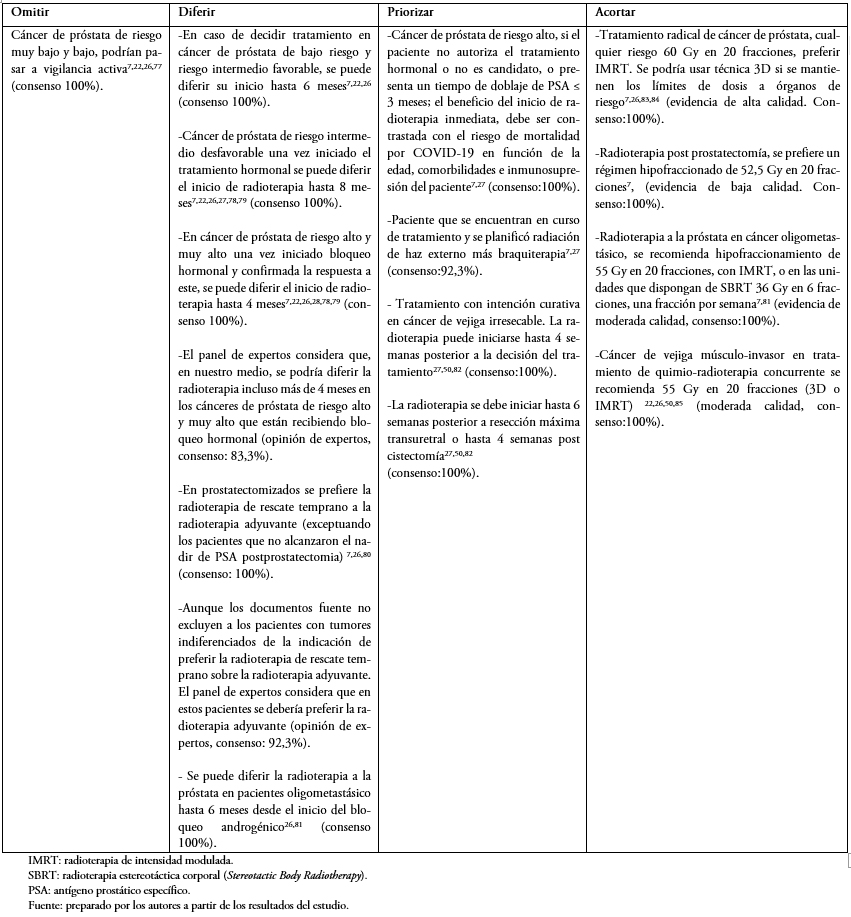
En las Tablas 1 a 6 se presentan las recomendaciones por patología, orientadas a establecer escenarios donde se pueden omitir, diferir, priorizar y acortar los tratamientos. Se recomiendan esquemas de tratamiento para cada patología priorizando el hipofraccionamiento cuando sea posible. En la Tabla 2 del material suplementario se describen estrategias en el caso de que existan suspensiones de tratamiento. [7]
 Tamaño completo
Tamaño completo 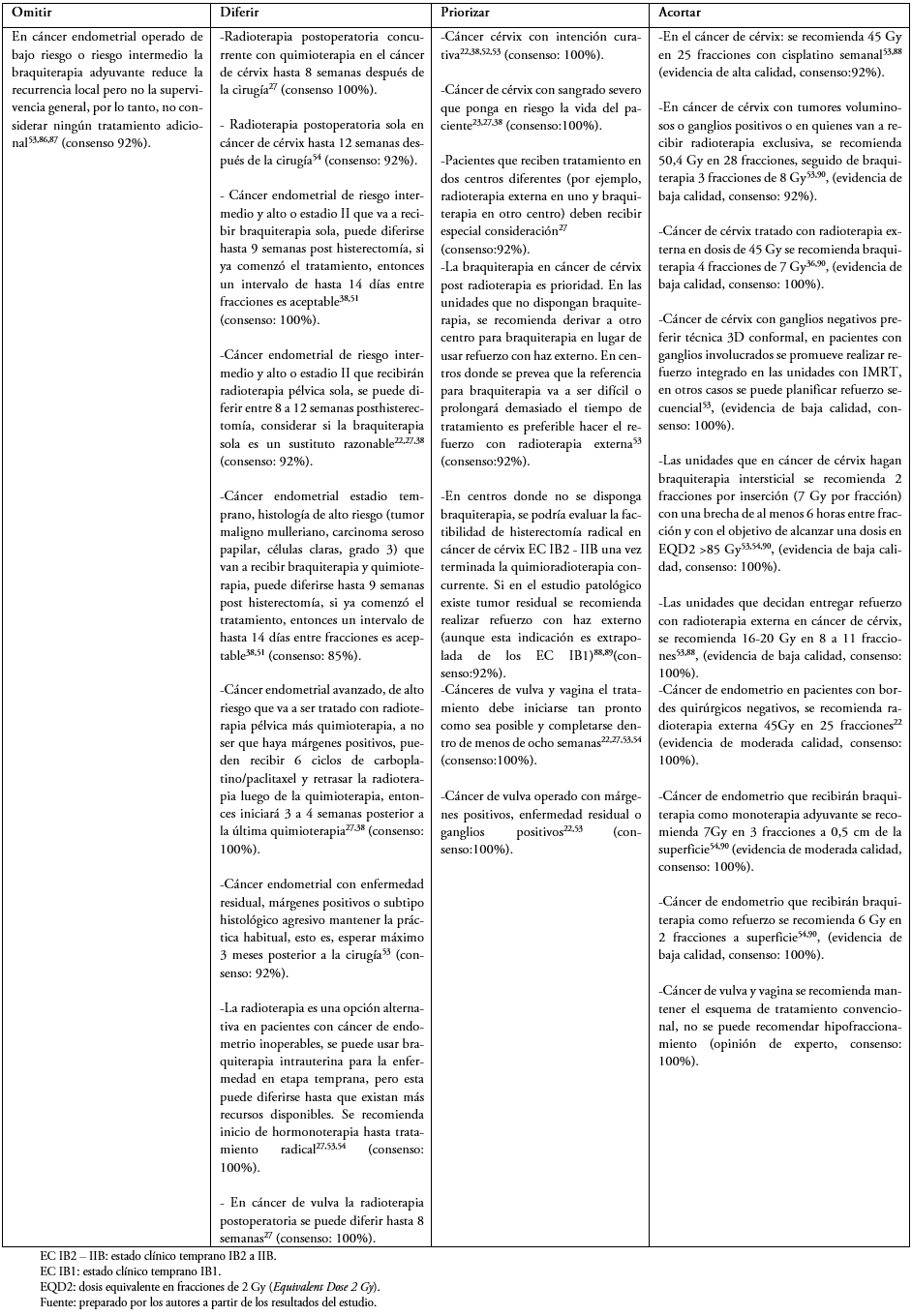 Tamaño completo
Tamaño completo 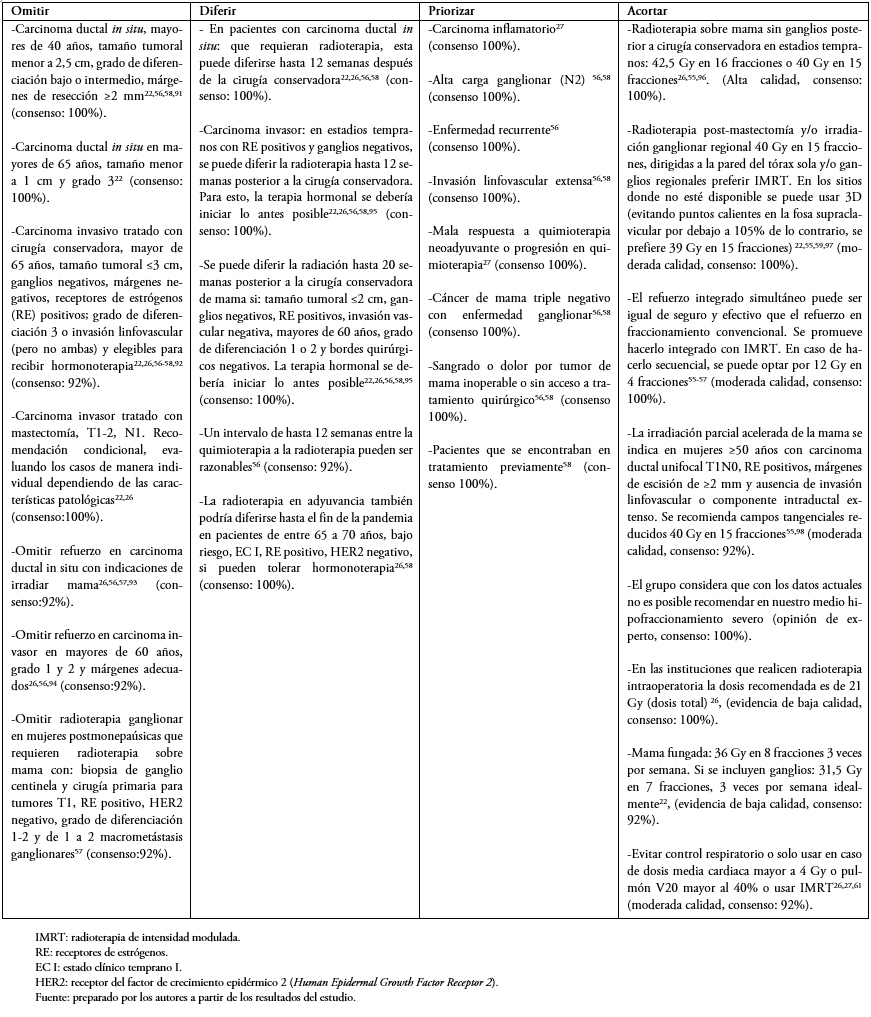 Tamaño completo
Tamaño completo
 Tamaño completo
Tamaño completo Radioterapia con intención paliativa
En el caso de la radioterapia entregada con intención paliativa se recomienda omitir el tratamiento de radioterapia en los siguientes casos:
- Pacientes metastásicos con expectativa de vida menor a tres meses[38] (consenso: 82%).
- Metástasis óseas asintomáticas o controladas con analgésicos[26] (consenso: 100%).
- Cáncer de próstata oligometastásico, radioterapia pre-operatoria en fracturas patológicas[26] (consenso: 100%).
Se podría diferir en:
- Pacientes estables sin síntomas emergentes, se puede esperar hasta progresión de los síntomas[63] (consenso: 100%).
- Metástasis cerebrales estables con manejo sintomático[26] (consenso: 91%).
- Metástasis en columna sin invasión del canal medular[27] (consenso 91%).
Los siguientes casos deberían recibir tratamiento prioritario:
- Síndrome de vena cava superior con categorización de severidad 3 a 5 según la escala de Yu y colaboradores[38],[109] (consenso 100%).
- Compresión medular y metástasis cerebrales sintomáticas no candidatos a cirugía[22],[26],[27] (consenso 100%).
- Metástasis óseas con o sin fractura, sin respuestas a opiáceos[22],[26] (consenso 100%).
- Obstrucción de vía aérea[27] (consenso 100%).
- Hemorragia aguda sin posibilidad de otros tratamientos[26],[27],[63] (consenso 100%).
- Dolor severo que no responde a manejo conservador[27] (consenso 100%).
Algunos esquemas recomendados:
- Metástasis cerebrales 20 Gy en 5 fracciones (3D o radioterapia de intensidad modulada). Radioterapia estereotáctica corporal una fracción, si son de 1 a 3 lesiones en casos seleccionados[22],[63],[110](moderada calidad, consenso: 100%).
- Metástasis cerebrales, con mal pronóstico dos fracciones de 6 Gy, técnica 3D[26], (evidencia de baja calidad,consenso: 100%).
- En metástasis óseas que ocasionen síndrome de compresión medular se recomienda una sola sesión de 8Gy, o 16 Gy en 2, o 15 Gy en 3 o 20 Gy en 5 fracciones, esta última se prefiere en pacientes con mejor pronóstico[22],[58],[111],[112](evidencia de alta calidad, consenso: 100%).
- Sangrado tumoral gastrointestinal o ginecológico, 20 Gy en 5 fracciones [26],[63], (evidencia de baja calidad, consenso: 100%).
- Síndrome de vena cava superior 20 Gy en 5 fracciones (técnica 3D) o 17 Gy en 2 fracciones una cada semana (con técnica avanzada donde esté disponible)[63],[113] (evidencia de moderada calidad, consenso: 100%).
- Obstrucción de vía aérea 20 Gy en 5 fracciones[63] (moderada calidad, consenso: 91%).
Discusión
El objetivo del presente documento fue proporcionar un apoyo urgente a los profesionales de las unidades de radioterapia de países con sistemas sanitarios limitados, donde la pandemia ha golpeado fuertemente. Hay una serie de recomendaciones sustanciales, estructuradas en torno a distintos escenarios, pero las decisiones de tratamiento en la práctica deberán tener en cuenta todos los factores clínicos relevantes.
Al considerar la implementación de estas recomendaciones, deben abordarse varios problemas que pueden afectar su uso clínico. Si bien se han analizado las realidades de la mayoría de las unidades de Ecuador, cada pauta podría o no ser implementada en función de los recursos humanos y técnicos disponibles. Según el Directorio de Centros de Radioterapia del Organismo Internacional de Energía Atómica, con datos actualizados a 2018, en Ecuador existen 11 centros de radioterapia concentrados en las ciudades de Quito, Guayaquil y Cuenca. En estos centros hay un total de 21 aceleradores lineales, seis unidades de braquiterapia y sólo en ocho centros se entregan tratamientos con radioterapia de intensidad modulada (IMRT, del inglés Intensity Modulated Radiotherapy).
Incluso dentro de una misma unidad de radioterapia, la capacidad o necesidad de implementar las recomendaciones podrían variar según qué fase de la pandemia estén atravesando. Por otra parte, es importante recalcar que las unidades de radioterapia deben regirse según las normativas emitidas por el Ministerio de Salud Pública. Es por ello, que de ningún modo estas recomendaciones pretenden suplantar a las emitidas por la autoridad competente.
Un efecto importante de COVID-19 es un cambio en la forma como se evalúa la relación riesgo-beneficio para la toma de decisiones. Ante la reducción de recursos, pueden ser necesarias decisiones de manejo fuera de los protocolos establecidos, con la consecuencia de verse obligados a adoptar tratamientos con mayor riesgo de efectos adversos o que podrían considerarse sub-óptimos, con el objetivo de garantizar seguridad y beneficio terapéutico para un mayor número de personas[39].
Varios trabajos han sido publicados desde el inicio de la pandemia haciendo un llamado a las unidades de radioterapia para que se priorice la entrega de tratamientos en función del tipo de tumor, de la intencionalidad del tratamiento y de los recursos disponibles[11],[20],[59]. Así, las guías disponibles insisten en la priorización del tratamiento de tumores considerados rápidamente proliferativos como cáncer de cabeza y cuello o cáncer de cérvix, especialmente cuando la intención es radical, ya que el diferir o suprimir la radioterapia en estos tumores afectaría significativamente el control de la enfermedad[26],[31],[35],,[39],[54].
Por otra parte, otros trabajos también han sugerido el uso de medidas prácticas para mitigar el impacto de las interrupciones del tratamiento[23],[38], así como también una implementación más amplia de programas hipofraccionados en la práctica clínica[7],[11],[12],[26],[38],[41],[47],[56],,[63]. Dichos documentos concuerdan en señalar que aunque la evidencia actual sobre esquemas hipofraccionados no ha logrado estandarizarse para todas las patologías, se debería considerar implementarlos, cuando sea factible, como el paradigma esencial para disminuir el acceso de los pacientes a los hospitales[7],[41],[56],[63].
Las presentes recomendaciones intentan recoger de manera sistemática estos trabajos publicados. La idea es proponer un sistema de priorización de la entrega de tratamiento por patología, esquemas hipofraccionados donde la evidencia lo permite, y sistemas para compensación de las dosis, según han sido propuestos por varios autores e instituciones.
Estas recomendaciones han sido desarrolladas bajo consenso y sustentándose en una metodología sujeta a las limitaciones que suponen datos clínicos acotados. A esto se suma la necesidad de desarrollarlas en el menor tiempo posible para dar una respuesta rápida a esta grave situación impuesta por la pandemia de CIVID-19. Es por ello que, por una parte, se incluyeron como artículos fuente documentos publicados a través de procesos editoriales acortados y sin el rigor metodológico deseable para la toma de decisiones. Por otra parte, sólo se realizó una evaluación formal de la calidad de la evidencia de las recomendaciones de esquemas de tratamiento. Para el resto de recomendaciones, la calidad de la evidencia se evaluó de forma global durante las discusiones entre expertos. Estas limitaciones deben considerarse a la hora de implementar las recomendaciones.
Finalmente, un grupo de patologías estuvieron fuera del alcance de esta revisión por considerarse de baja prevalencia y bajo impacto en las unidades de radioterapia. Estas patologías fueron cáncer de pulmón o tumores del tejido conectivo. En estos casos consideramos que se debe mantener la práctica habitual antes de la pandemia por COVID-19.
Conclusiones
Se plantean estrategias orientadas a la gestión de los servicios de radioterapia para reducir el riesgo de infección de pacientes y personal.
También se hacen recomendaciones por patología, con el objetivo de garantizar que los tratamientos de radioterapia de alta calidad continúen en beneficio de todos los pacientes oncológicos que requieren este tratamiento.
Finalmente, dada la urgente necesidad de procesar dichas recomendaciones, y ante el carácter emergente de esta pandemia, se trabajó con diversas limitaciones como el análisis de datos clínicos acotados, inclusión de documentos con procesos editoriales de rigor insuficiente y falencias en la evaluación de la calidad de evidencia, entre otros. Por estos motivos, es importante considerar las limitaciones al momento de implementar estas recomendaciones.