Revisión clínica
← vista completaPublicado el 29 de abril de 2022 | http://doi.org/10.5867/medwave.2022.03.002550
Impulso, esfuerzo y trabajo respiratorio: revisión de definiciones y herramientas no invasivas de ventiladores de cuidados intensivos durante tiempos de pandemia
Respiratory drive, inspiratory effort, and work of breathing: review of definitions and non-invasive monitoring tools for intensive care ventilators during pandemic times
Resumen
Los avances tecnológicos de la ventilación mecánica han sido parte esencial del aumento de la sobrevida en las unidades de cuidados intensivos. Desde la conexión a la ventilación mecánica, comúnmente se utiliza ventilación controlada sin la consecuente participación de los músculos respiratorios del paciente, con el fin de favorecer la protección pulmonar. El retiro de la ventilación mecánica implica un periodo de transición hacia la respiración espontánea, utilizando principalmente ventilación mecánica asistida. En esta transición, el desafío de los clínicos es evitar la sub y sobre asistencia ventilatoria, minimizando el esfuerzo respiratorio excesivo, daño diafragmático y pulmonar inducidos por la ventilación mecánica. La monitorización con balón esofágico permite mediciones objetivas de la actividad muscular respiratoria en tiempo real, pero aún hay limitaciones para su aplicación rutinaria en pacientes ventilados mecánicamente en la unidad de cuidados intensivos. Al igual que el balón esofágico, la electromiografía de los músculos respiratorios y la ecografía diafragmática son herramientas que permiten monitorizar la actividad muscular de la respiración, siendo mínimamente invasivas y con requerimiento de entrenamiento específico. Particularmente, durante la actual pandemia de enfermedad por coronavirus se ha extendido el uso de herramientas no invasivas disponibles en los ventiladores mecánicos para monitorizar el impulso (drive), esfuerzo y trabajo respiratorio, para promover una ventilación mecánica ajustada a las necesidades del paciente. Consecuentemente, el objetivo de esta revisión es identificar las definiciones conceptuales de impulso, esfuerzo y trabajo respiratorio utilizadas en el contexto de la unidad de cuidados intensivos, e identificar las maniobras de medición no invasivas disponibles en los ventiladores de cuidados intensivos para monitorizar impulso, esfuerzo y trabajo respiratorio. La literatura destaca que, aunque los conceptos de impulso, esfuerzo y trabajo respiratorio se perciben intuitivos, no existe una definición clara. Asimismo, destacados autores los definen como conceptos diferentes.
|
Ideas clave
|
Introducción
El número de pacientes que se hospitalizan en las unidades de cuidados intensivos requiriendo ventilación mecánica está aumentando en todo el mundo, y en mayor volumen durante la actual pandemia por la enfermedad de coronavirus (COVID 19) [1],[2]. Históricamente, los avances tecnológicos y procedimentales de la ventilación mecánica han sido parte esencial del aumento de la sobrevida en la unidad de cuidados intensivos, sobre todo los relacionados con la monitorización y sincronía entre la asistencia del ventilador y la acción de los músculos respiratorios [3]. Desde la conexión a la ventilación mecánica, comúnmente se utiliza ventilación controlada, atenuando o anulando temporalmente la participación de los músculos respiratorios y favoreciendo la protección pulmonar [4].
El retiro de la ventilación mecánica implica un periodo de transición hacia la respiración espontánea [5], el cual desafía a los clínicos a evitar la sub y sobre asistencia de la musculatura respiratoria, minimizando el esfuerzo respiratorio excesivo, diafragmático y pulmonar inducidos por ventilación mecánica [6]. Estas amenazas refuerzan la necesidad de personalizar la ventilación mecánica, identificando ajustes precisos de los parámetros ventilatorios en función de seguimiento de variables fisiológicas específicas y objetivos individualizados [7]. La personalización de los ajustes ventilatorios se torna aún más desafiante durante la ventilación asistida [8], en la que se debe mantener un delicado equilibrio entre la carga de los músculos respiratorios y el soporte del ventilador. Siguiendo el conocimiento de los clínicos, el ajuste de la ventilación asistida se limita mayoritariamente al volumen corriente como indicador de sobre asistencia [9], en vez de considerar parámetros específicos de esfuerzo inspiratorio [8],[10].
La medición de la presión esofágica (Peso), mediante balón esofágico, está bien descrita para:
- Caracterizar las propiedades mecánicas del sistema respiratorio (fundamentalmente durante la ventilación mecánica controlada).
- Entender la interacción paciente–ventilador.
- Monitorizar continuamente y en tiempo real la actividad de los músculos respiratorios durante la ventilación mecánica asistida [11],[12].
Particularmente, el balón esofágico permite monitorizar respiración a respiración el trabajo respiratorio del paciente (WOBp) a través de la construcción del diagrama de Campbell [13]. Adicionalmente, permite medir componentes aún más específicos del esfuerzo inspiratorio a través del cálculo del producto presión-tiempo (PTP) y de la presión muscular respiratoria (Pmus) [11],[12]. Un esfuerzo respiratorio normal se puede identificar con un producto presión tiempo entre 50 y 150 centímetros de agua por segundo al minuto o con una presión muscular entre cinco y 10 centímetros de agua. Por lo tanto, con el balón esofágico es posible ajustar el soporte respiratorio basado en el desempeño de cada paciente, personalizando así la programación de la ventilación mecánica asistida.
Si bien la monitorización con balón esofágico entrega mediciones objetivas del esfuerzo y trabajo respiratorio, aún hay limitaciones para su aplicación rutinaria en pacientes ventilados. Esto, porque requiere tiempo, equipamiento específico y correcta interpretación fisiológica de señales [11],[12]. Alternativamente, la medición de la actividad eléctrica diafragmática permite un buen acercamiento al concepto de esfuerzo respiratorio, ya sea utilizando electromiografía de superficie diafragmática [14] o ventilación asistida ajustada neuronalmente [15]. Sin embargo, estas opciones requieren electrodos o una sonda nasogástrica para funcionar. Por otro lado, la medición de la fracción de acortamiento por medio de la ecografía diafragmática permite una buena aproximación al esfuerzo inspiratorio que se correlaciona bien con variables provenientes del balón esofágico. No obstante ello, sus limitaciones incluyen la necesidad de equipamiento, capacitación y no es continuo ni sincronizado con las formas de onda del ventilador [16]. Es por todo esto que los clínicos requieren técnicas simples, factibles y no invasivas para evaluar la interacción pacientev entilador y el esfuerzo respiratorio.
Durante los últimos años, y particularmente durante la actual pandemia, se ha puesto énfasis en el estudio del impulso (drive) respiratorio y esfuerzo inspiratorio. Esto, por sus particulares interacciones con la hipoxemia y disnea de los pacientes con síndrome de dificultad respiratoria aguda debido a COVID- 19 [17]. Más aún, se ha popularizado el uso de maniobras no invasivas disponibles en los ventiladores de cuidados intensivos para monitorizar impulso, esfuerzo y trabajo respiratorio, espe-cialmente durante la ventilación con presión de soporte [17],[18],[19],[20], con el fin de promover una ventilación mecánica ajustada a las necesidades del paciente. Consecuentemente, el objetivo de esta revisión es primero identificar las definiciones conceptua-les de impulso, esfuerzo y trabajo respiratorio disponibles en la literatura para los cuidados intensivos. Secundariamente, también se busca identificar las maniobras no invasivas disponibles en los ventiladores de cuidados intensivos para medir o estimar parámetros de impulso, esfuerzo y trabajo respiratorio.
Métodos
Para la selección de documentos de esta revisión se utilizaron referencias de la búsqueda de un scoping review previamente publicado, relacionado con este tópico [21]. Primero, se realizó una actualización de la búsqueda simple en PubMed/MEDLINE combinando palabras clave como: “respiratory drive”, “respiratory effort”, “work of breathing”, “assisted ventilation”, “intensive care unit” y “mechanical ventilation”. Se seleccionaron todos los documentos que respondieran al objetivo, de manera no sistemática y, sin límite de tiempo ni tipo de estudio. Se incluyeron también artículos relacionados a COVID- 19. Segundo, se revisaron los manuales de funcionamiento de los ventiladores de cuidados intensivos utilizados en Chile, disponibles en la web. Finalmente, se realizó una revisión en terreno de los ventiladores más utilizados en hospitales y clínicas del país (de forma presencial o remota por video llamada), en busca de maniobras no invasivas para medir o estimar impulso, esfuerzo o trabajo respiratorio. Se visitaron hospitales y empresas hasta lograr incluir las marcas y modelos de los ventiladores mecánicos más utilizados en Chile durante la pandemia. Se incluyeron todos los ventiladores diseñados para ventilación invasiva con funcionamiento de válvulas, excepto los ventilado-res para el transporte biomédico.
Los contenidos de esta revisión se exponen a continuación desde lo más general (abarcando los conceptos fisiológicos y definiciones de impulso, esfuerzo y trabajo respiratorio), hasta la descripción y recolección de las maniobras disponibles en los ventiladores de cuidados intensivos. Para ello, nos basamos en la literatura seleccionada y en la revisión in situ de los ventilado-res, en especial en las maniobras no invasivas.
Resultados y discusión
Definiciones
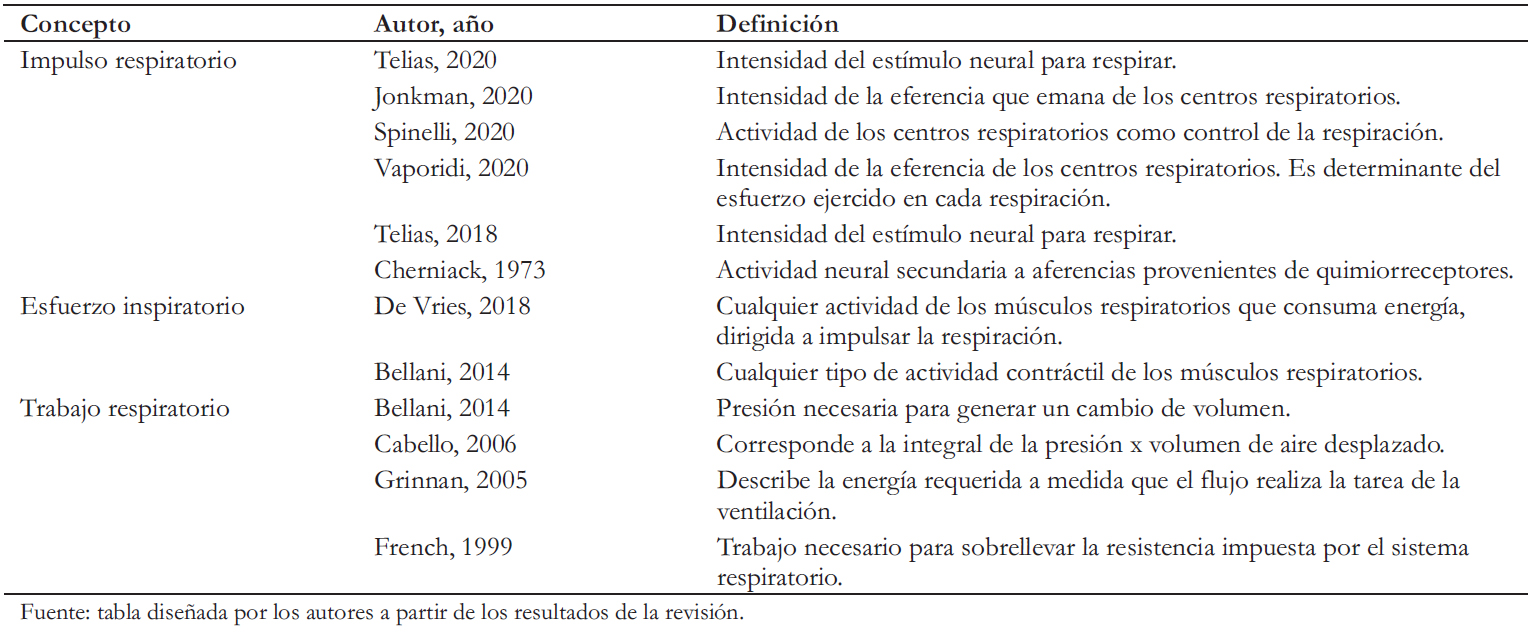
La literatura destaca que, aunque los conceptos de impulso, esfuerzo y trabajo respiratorio se perciben intuitivos, no existe una definición clara. Además, destacados autores los definen como conceptos diferentes [22] (Tabla 1). Si bien bajo condi-ciones de indemnidad del sistema respiratorio, el impulso respi-ratorio, esfuerzo inspiratorio y trabajo respiratorio tienen una estrecha relación, en condiciones de enfermedad esto puede no siempre cumplirse [23]. Este antecedente justifica distinguir las definiciones de los conceptos abordados en esta revisión (Figura 1).
 Tamaño completo
Tamaño completo 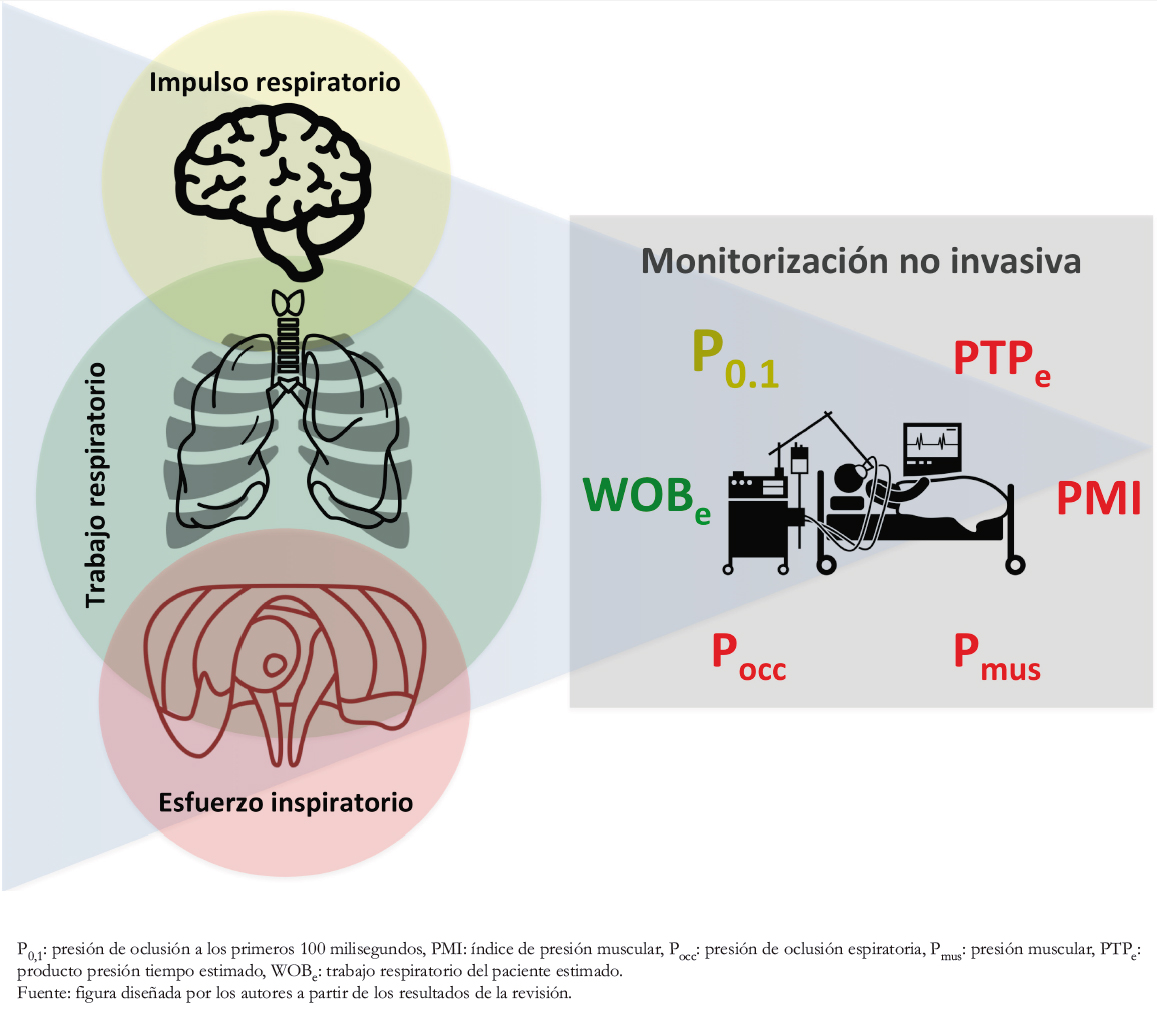 Tamaño completo
Tamaño completo Definición de impulso respiratorio (drive respiratorio)
El objetivo primario de la respiración es mantener un intercambio gaseoso equilibrado. En otras palabras, un balance entre la captura de oxígeno y la eliminación de dióxido de carbono (CO2). Este objetivo se logra mediante un control estricto de la respiración gracias a la regulación del centro respiratorio. La intensidad y velocidad de la respuesta depende de la retroalimentación de cuatro principales fuentes aferentes: bioquímica, mecánica, emocional e inflamatoria [23].
La primera y principal aferencia es la bioquímica proveniente de los quimiorreceptores [24], la cual corresponde a una retroali-mentación refleja que se encuentra mediada por aferencia originada en quimiorreceptores centrales y periféricos. El objetivo de este mecanismo de control es minimizar las fluctuaciones de los niveles de dióxido de carbono arterial, pH y evitar la hipoxemia [25]. Los quimiorreceptores periféricos, localizados en los cuerpos carotídeos, regulan el impulso respiratorio modificando la sensibilidad y umbral excitatorio de los quimiorreceptores centrales [26].
La segunda, corresponde a las aferencias provenientes de los mecanorreceptores a nivel pulmonar, parrilla costal, vía aérea y músculos respiratorios. El huso muscular y los receptores de estiramiento de adaptación lenta son un ejemplo de esto, ya que proveen información sobre estiramiento y volumen pulmonar a través de sus fibras vagales. Estos receptores son los responsables del reflejo Hering-Breuer, el cual da término a la inspira-ción y facilita la espiración frente a altos volúmenes corrientes [27].
La tercera aferencia corresponde a la retroalimentación suprapontina. El miedo, ansiedad, dolor o delirium, también son responsables de transmitir una retroalimentación sensorial a los centros respiratorios. La corteza cerebral y el hipotálamo tienen la capacidad de modular el impulso respiratorio.
La cuarta aferencia está mediada por la respuesta inflamatoria [23], por ejemplo, en pacientes que cursan con sepsis o falla respiratoria aguda. Los mediadores inflamatorios (histamina, bradiquininas y prostaglandinas) provocan un estímulo vagal que aumenta la frecuencia respiratoria y disminuye el volumen corriente [25], generando un patrón respiratorio rápido y superficial.
Una vez integrada la información de las cuatro aferencias, se elabora una respuesta en el centro respiratorio. Esto es conocido como impulso respiratorio. Así, se define impulso respiratorio como la intensidad de la eferencia respiratoria que se genera a nivel del sistema nervioso central [18],[23],[28]. Varios autores coinciden con que el impulso no necesariamente refleja modificaciones en el esfuerzo inspiratorio, ya que se refiere a señal eléctrica y no directamente a señal mecánica. El impulso se origina desde un grupo de interneuronas (centro respiratorio) localizado a nivel del tronco encefálico [27]. La amplitud de la señal que emerge desde este grupo neuronal, determina la respuesta mecánica de los músculos respiratorios.
En pacientes conectados a ventilación mecánica, un impulso respiratorio disminuido, ya sea por sobre asistencia o por efecto de la sedación, contribuirá a generar debilidad diafragmática [29]. Un impulso débil también será responsable de la pérdida de sincronía entre el paciente y el ventilador. Al igual que en el caso anterior, un impulso elevado puede resultar en daño de las fibras del diafragma por sobrecarga [30]. Asimismo, un impulso aumentado conduce a un patrón respiratorio rápido y superficial, con reclutamiento de musculatura accesoria e incremento de la disnea y como consecuencia, a un fracaso en las pruebas de ventilación espontánea [31]. Otro efecto de un impulso respiratorio desmedido es la asincronía entre paciente y ventilador. Durante la ventilación asistida, una programación que no está acorde a las demandas ventilatorias del paciente, puede provocar fenómenos tales como hambre de flujo (flow starvation), ciclado prematuro o gatillaje inefectivo [32],[33]. Por lo tanto, el impulso (y sus aferencias) ocurren como antecesor del esfuerzo y trabajo respiratorio. Su intensidad y magnitud son causa de lo que ocurre con la actividad y ritmo muscular.
Definición de esfuerzo inspiratorio
La definición de esfuerzo inspiratorio pareciera ser bastante intuitiva, sin embargo ha sido poco explorada en la literatura y podría confundirse con las definiciones de trabajo respiratorio [22],[34]. Es más, frente a ciertas situaciones como el atrapamiento aéreo (PEEPi) o debilidad muscular respiratoria, su conceptualización puede resultar confundente cada vez que esfuerzo y trabajo se asumen como un mismo concepto. Es importante señalar que el esfuerzo inspiratorio se encuentra controlado por el impulso respiratorio, para así mantener un balance con las demandas ventilatorias. De esta forma, el esfuerzo inspiratorio es dependiente de la intensidad de la eferencia emanada desde los centros superiores, y también de los propiedades visco elásticas del sistema respiratorio [19],[34].
La responsable de mantener el equilibrio de la demanda ventilatoria es la bomba respiratoria, la que está conformada por diferentes músculos esqueléticos, que actúan de manera coordinada para sostener una ventilación alveolar acorde a las demandas metabólicas [22]. La función de la bomba muscular inspiratoria es llevada a cabo principalmente por el diafragma [35]. Cuando aumenta la carga respiratoria, y el diafragma no es capaz por sí solo de llevar a cabo la ventilación, se reclutan músculos acce-sorios que contribuyen a la inspiración. Los principales músculos que colaboran son esternocleidomastoideo, para esternal e intercostales externos [36]. Por lo tanto durante la respiración espontánea, la caída del valor de la presión pleural va a depender de la contracción de los músculos inspiratorios (presión muscular) y del diferencial de presión que se genera sobre la pared del tórax [22],[37].
Según la literatura, esfuerzo inspiratorio se define como cualquier consumo de energía por parte de los músculos respira-torios con el propósito de conducir la respiración [22]. Este concepto tiene la capacidad de englobar al tiempo y tipo de contracción muscular. Las contracciones isométricas generan un consumo de energía que no se traduce en un cambio de volumen, pero que sin embargo constituyen un esfuerzo. Esta definición resulta de gran importancia ya que marca una distancia con el concepto de trabajo. No toda contracción de la musculatura respiratoria resulta en un cambio de volumen, aunque sí significa un consumo de energía. En sujetos sanos, la inspiración comienza en el punto de equilibrio del sistema respiratorio. Esto es, donde la tendencia del colapso de los pulmones es igual a la tendencia hacia la expansión de la parrilla costal [38]. En este punto, la acción de los músculos inspiratorios (presión muscular) provoca una caída en el valor de la presión pleural y, consecuentemente, un cambio de volumen.
Definición de trabajo respiratorio
En física, el término trabajo hace referencia a la fuerza aplicada sobre un objeto y el desplazamiento que ocurre a consecuencia de esto [34]. En otras palabras, corresponde a fuerza por desplazamiento (W= F × d). En el sistema respiratorio, trabajo respiratorio (WOB) se calcula como el producto entre la integral de la presión y el volumen:
WOB = ∫ presión × volumen
Es decir, el área en un diagrama de presión-volumen [13]. Conceptualmente se define como el trabajo necesario para sobrellevar la carga impuesta por el sistema respiratorio. Este trabajo, entonces, puede ser llevado a cabo por los músculos respiratorios cuando la respiración es espontánea, exclusivamente por el ventilador mecánico si la respiración es controlada, o por ambos en el caso de que la ventilación sea asistida [39]. Para entender los componentes del trabajo respiratorio es preciso mencionar la ecuación de movimiento del gas alveolar. Esta ecuación pone en evidencia que a cada momento, la presión de vía aérea tiene un componente elástico (necesario para vencer la elastancia del parénquima), un componente resistivo (la circulación de un flujo siempre se le opone una carga resistiva) y un componente inercial que para frecuencias respiratorias menores a un hercio se considera despreciable [40]:
Paw = Ers × V + Raw × Q + PEEPtot
Paw: presión de vía aérea, Ers: elastancia del sistema respiratorio, V: volumen, Raw: resistencia de la vía aérea, Q: flujo del gas y PEEPtot: presión positiva al final de la espiración.
Por lo tanto, de esta ecuación se puede desprender que el tra-bajo respiratorio debe vencer un componente resistivo, elástico y el aire que queda atrapado al final de la espiración (presión positiva al final de la espiración) [13].
El concepto trabajo respiratorio puede resultar confuso. Esto es debido a la definición clásica de trabajo en la que siempre debe haber un cambio de volumen frente a la administración de una presión determinada. En fisiología respiratoria, tanto de individuos sanos como enfermos, existe un componente isométrico que la conceptualización de trabajo no puede considerar, pero que sin embargo, genera consumo de energía (esfuerzo) por parte de los músculos respiratorios [34].
Maniobras no invasivas de impulso, esfuerzo y trabajo respiratorio disponibles en los ventiladores de cuidados intensivos
Dentro de las maniobras disponibles en los ventiladores identi-ficamos la presión de oclusión de vía aérea de los primeros 100
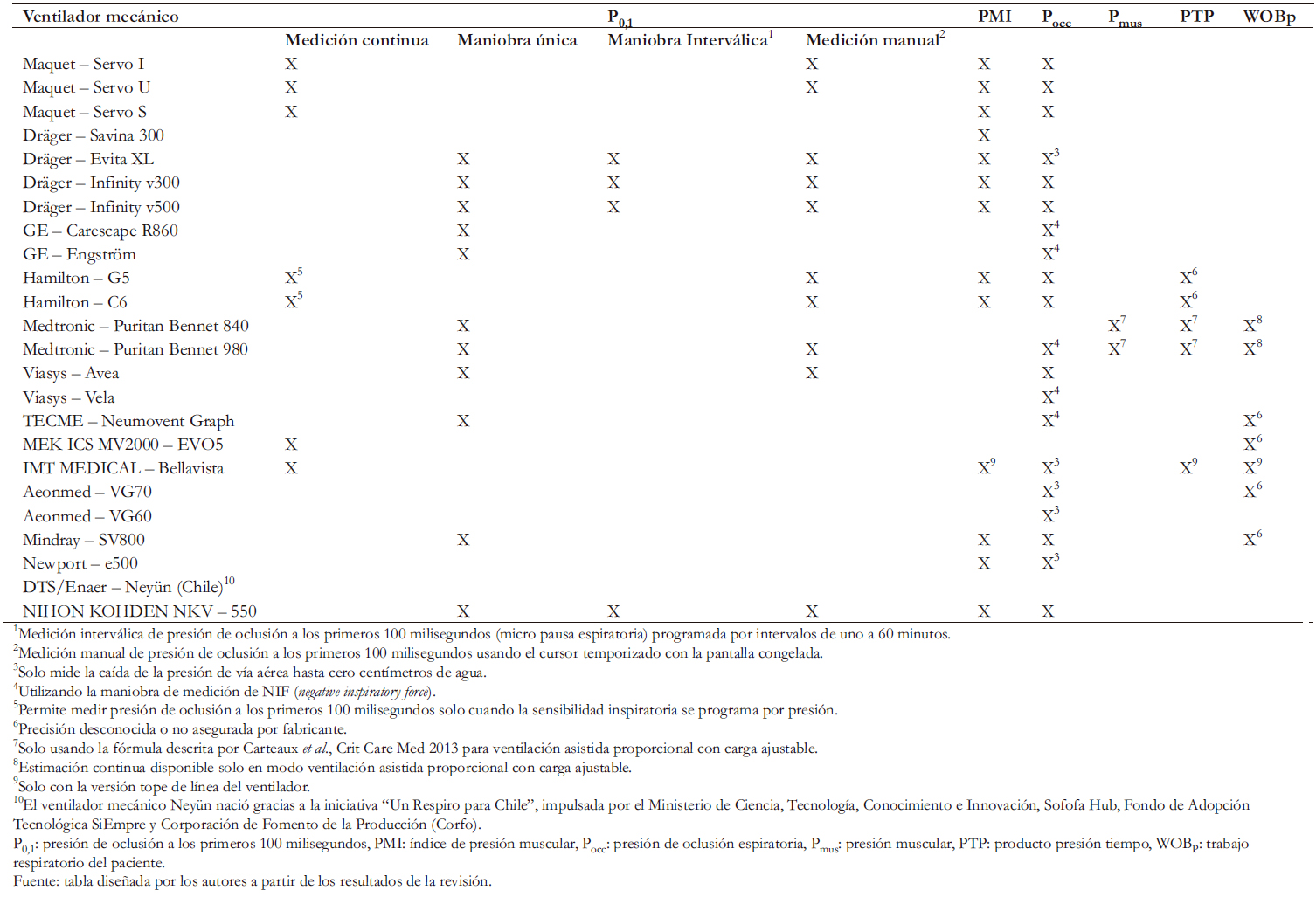
milisegundos (P0,1), la diferencia de la presión de oclusión espi-ratoria (ΔPocc) y el índice de presión muscular (PMI). Además, se consideran variables calculables con la información de los ventiladores como la presión muscular, producto presión- tiempo y trabajo respiratorio del paciente (Tabla 2).
 Tamaño completo
Tamaño completo Presión de oclusión de vía aérea
La presión de oclusión a los primeros 100 milisegundos es una medición no invasiva para monitorizar el impulso, definida tal como lo indica su nombre por la caída de la presión de la vía aérea durante los primeros 100 milisegundos (0,1 segundos) frente a una oclusión al final de la espiración. Fue inicialmente descrita por Whitelaw et al. en 1975 en personas sanas [41] y luego comenzó a utilizarse en pacientes críticos [42],[43]. Actualmente sigue siendo foco de estudio [44],[45],[46]. Además es una herramienta que se utiliza para predecir el destete de la ventilación mecánica y para ajustar el soporte respiratorio, incluso en pacientes con soporte vital extracorpóreo [47]. Los valores de la presión de oclusión a los primeros 100 milisegundos oscilan entre 0,5 y 1,5 centímetros de agua en personas sanas, y entre 1,3 y 3,5 centímetros de agua en pacientes críticos [18]. Una presión de oclusión a los primeros 100 milisegundos mayor a 3,5 centímetros de agua tiene una sensibilidad del 92% y una especificidad del 89% para detectar un esfuerzo inspiratorio excesivo [48]. Los ventiladores modernos muestran la presión de oclusión a los primeros 100 milisegundos de forma continua, ya sea estimándola según la caída de la presión de la vía aérea durante la fase de activación, o realizando una maniobra de oclusión breve al final de la espiración [49]. La presión de oclu-sión a los primeros 100 milisegundos aumenta proporcionalmente a la presión arterial de dióxido de carbono durante la ventilación asistida y no se ve afectada por la debilidad de los músculos respiratorios [47],[50]. Como la variabilidad respiración a respiración de la presión de oclusión a los primeros 100 mili-segundos es significativa, se recomienda considerar un prome-dio de tres a cuatro mediciones [18].
Maniobra de oclusión espiratoria
Con una maniobra de oclusión espiratoria en ventilación asistida, se puede obtener la diferencia de la presión de oclusión espiratoria, siendo la diferencia entre la presión base (comúnmente la presión positiva al final de la espiración total) del trazado presión-tiempo y el valor más negativo durante la caída de la presión luego de una oclusión mecánica al final de la espiración (habitualmente con una pausa espiratoria de cinco segundos) [51]. En términos simples, es la continuación de la maniobra de la presión de oclusión a los primeros 100 milisegundos considerando el valor más negativo.
La maniobra de diferencia de la presión de oclusión espiratoria fue descrita inicialmente por Bertoni et al. en 2019 [51] como un método no invasivo para estimar el esfuerzo inspiratorio durante la ventilación asistida. Si bien la oclusión espiratoria se utiliza habitualmente para medir la presión positiva al final de la espiración intrínseca en ventilación controlada o para medir la presión inspiratoria máxima (PIM) durante esfuerzos inspiratorios voluntarios máximos, la oscilación de la presión de las vías respiratorias durante una maniobra breve de oclusión al final de la espiración aplicada al azar, sin un esfuerzo voluntario máximo, puede usarse para evaluar el esfuerzo inspiratorio. De hecho, durante la oclusión, la oscilación de la presión de las vías respiratorias se correlaciona exactamente con la oscilación de la presión pleural [37], siempre y cuando esta oclusión única, breve e inesperada no modifique mayormente el impulso respiratorio [52].
Teniendo en cuenta las diferencias en la oscilación de la presión esofágica entre las condiciones ocluidas y dinámicas, se ha pro-puesto multiplicar el resultado de la diferencia de la presión de oclusión espiratoria por 0,75 para obtener un valor estimado de presión muscular [20]. Esto es:
Pmus = −0,75 × ΔPocc
Ello corresponde a la fuerza global generada por los músculos inspiratorios (https://rtmaven.com). Los valores esperados de presión muscular para un paciente con adecuado nivel de esfuerzo inspiratorio son entre 5 y 10 centímetros de agua [53] y para diferencia de la presión de oclusión espiratoria son entre 7 y 15 centímetros de agua [20]. Alternativamente, usando la maniobra de oclusión espiratoria se puede estimar la presión de distención transpulmonar dinámica (ΔPL), la cual se calcula como:
ΔPL = (peak Paw − PEEP) −0,66 × ΔPocc
Esto indica sobredistención con valores sobre 16 a 17 centímetros de agua. Con la maniobra de oclusión espiratoria no solo se puede detectar el potencial daño pulmonar y el esfuerzo respiratorio excesivo o ausente, sino también se puede utilizar para diferenciar varias formas de asincronías paciente-ventilador. Esta maniobra puede desenmascarar esfuerzos inefectivos, identificar autogatillajes y diferenciar los dobles gatillajes de gatillajes reversos (en cuyo caso habrá apnea durante la pausa espiratoria) [54]. Además, si el ventilador tiene disponible la función de medir con cursor el inicio y fin del esfuerzo inspiratorio durante la pausa espiratoria, se podría estimar el tiempo inspiratorio neural del paciente y observar la morfología de la caída de la presión dada por la inclinación o pendiente entre la presión de oclusión a los primeros 100 milisegundos y la diferencia de la presión de oclusión espiratoria. Una limitación destacable de la maniobra de oclusión espiratoria es que la hiperinsuflación dinámica y la presión positiva al final de la espiración intrínseca pueden llevar a una subestimación del esfuerzo, sobre todo si la presión positiva al final de la espiración intrínseca no se ha equilibrado con la vía aérea ocluida [54].
Maniobra de oclusión inspiratoria
Una maniobra breve de oclusión al final de la inspiración se utiliza ampliamente para medir la presión meseta (Pplat) y la pre-sión de distención (ΔP) en ventilación mecánica controlada. Bellani et al. sugirieron que una breve maniobra de oclusión inspiratoria permite mediciones confiables de presión meseta incluso en ventilación mecánica asistida [55]. Durante una oclusión inspiratoria en ventilación mecánica asistida, los pacientes relajan los músculos inspiratorios, dando como resultado un aumento de la presión de distención de vía aérea, lo cual es detectable en la forma de onda del ventilador.
La maniobra de oclusión inspiratoria en ventilación asistida no es nueva, ya que fue descrita inicialmente por Foti et al. en 1997 como un método para evaluar la presión desarrollada por los músculos inspiratorios en pacientes con lesión pulmonar aguda, durante la ventilación con presión de soporte [56]. Cuando el paciente está sobre asistido y el esfuerzo respiratorio es bajo, la presión de vía aérea cae por debajo de la presión meseta durante la oclusión inspiratoria en ventilación asistida. Por el contrario, cuando la presión de vía aérea se eleva por sobre el valor de la presión meseta, podría indicar un esfuerzo respiratorio alto o bien, sub- asistencia, indicado por la magnitud de la relajación de la musculatura inspiratoria. En este último caso, la diferencia entre la presión de vía aérea y la presión meseta durante una oclusión inspiratoria es lo que se conoce como PMI, Pmusc,index o índice de presión muscular [56]. Durante la ventilación con presión de soporte, el índice de presión muscular se calcula como:
PMI = Pplat − (PEEP + PS)
En donde la presión meseta es la presión alcanzada durante la oclusión inspiratoria. Valores del índice de presión muscular mayores a tres centímetros de agua indican un esfuerzo inspiratorio elevado [56]. Parte del razonamiento del índice de presión muscular, fue descrito por Prinianakis et al. en 2008, quienes examinaron la causa del aumento de la presión del ventilador por encima del nivel preestablecido de presión de soporte al final de la inspiración durante la ventilación con presión de soporte [57]. Dado que la relajación de los músculos inspiratorios precede a la contracción de los músculos espiratorios, el aumento de la presión del ventilador usando la ventilación con presión de soporte puede significar el final de la inspiración neural. La técnica de medición del índice de presión muscular no está libre de limitaciones. Debido a que la presión se obtiene en condiciones cuasi estáticas, esta medición puede afectarse por los mecanismos de Pendelluft, especialmente en pacientes con síndrome de dificultad respiratoria aguda [58]. Por otro lado, puede haber inestabilidad del trazado de la presión de vía aérea durante la oclusión, lo cual podría confundir la relajación de los músculos inspiratorios con la acción de los músculos abdominales que pueden aumentar rápidamente la presión de vía aérea como el inicio de la espiración neural durante la oclusión inspiratoria [59].
Cálculos derivados de la información de los ventiladores
Los ventiladores actuales entregan valores estimados de varia-bles de esfuerzo inspiratorio y trabajo respiratorio sin la necesitad de una sonda o equipamiento adicional, como el producto presión-tiempo y el trabajo respiratorio del paciente. Los métodos disponibles en los ventiladores para acercarse a estos parámetros provenientes originalmente del uso de balón esofágico [60], no son del todo precisos. Por este motivo deben interpretarse con cautela, ya que incluso cada ventilador tiene características de presurización diferentes [61]. Algunos ventiladores entregan valores de producto presión-tiempo o trabajo respiratorio del paciente basados en estimaciones del área de la gráfica presión-tiempo.
Particularmente, la ventilación asistida proporcional con carga ajustable tiene fundamentos descritos inicialmente por Magdy Jones en 1991 como un modo ventilatorio que entregaba soporte según la demanda del paciente considerando las pro-piedades mecánicas del sistema respiratorio [62]. Desde 2007, la ventilación asistida proporcional con carga ajustable (PAV+) entrega valores de trabajo respiratorio elástico y resistivo del ventilador y del paciente a partir de una breve oclusión inspiratoria de 300 milisegundos, obteniendo una presión meseta y, consecuentemente, los principales componentes de la ecuación de movimiento distensibilidad y resistencia [63],[64]. Los valores esperados para un trabajo respiratorio aceptable en ventilación asistida proporcional con carga ajustable oscilan entre los 0,3 y 0,7 Joules por litro. Desde 2013, la ventilación asistida proporcional con carga ajustable permite calcular la presión muscular y el producto presión-tiempo utilizando las fórmulas desarrolladas por Carteaux et al. [53], sin la necesidad de un balón esofágico. Usando la ventilación asistida proporcional con carga ajustable, la presión muscular puede ser calculada como:
Pmus = (Ppeak – PEEP) × (% soporte ÷ % paciente)
En donde % soporte es el porcentaje de asistencia programado en el ventilador y % paciente es el porcentaje de trabajo que realiza el paciente (https://bit.ly/3kj6oTz). Consecuentemente, al obtener la presión muscular es posible calcular:
PTP = [(Pmus x tiempo inspiratorio) × frecuencia respiratoria] ÷ 2.
La estimación del producto presión-tiempo solo era posible en la ventilación asistida proporcional con carga ajustable hasta antes de la descripción de la diferencia de la presión de oclusión espiratoria usando la maniobra de oclusión espiratoria, con la cual se obtiene presión muscular. Sin embargo, aunque aún no ha sido estudiado, actualmente se podría estimar el producto presión- tiempo durante la ventilación con presión de soporte utilizando el cálculo de presión muscular con la maniobra de oclusión espiratoria.
Formas de curvas y asincronías
La aparición de asincronías en las curvas de presión-tiempo y flujo-tiempo pueden alertar sobre la presencia de impulso y esfuerzo respiratorio elevado, particularmente ante la presencia de hambre de flujo (flow starvation), ciclados prematuros y doble gatillaje [18]. En general, la interpretación de la gráfica ventilatoria puede facilitar la identificación de desfase o discordancia entre el tiempo inspiratorio neural y el mecánico, lo cual es frecuente usando la ventilación con presión de soporte [65]. Así como las pendientes de los trazados de presión y flujo en relación con el tiempo pueden ayudar a medir el Stress Index y esfuerzos inefectivos, también pueden ser útiles para estimar el nivel de esfuerzo inspiratorio. Recientemente, se describió una nuevo método basado en la pendiente del flujo inspiratorio llamado Flow Index [66]. Aunque aún este método requiere estudios sobre la aplicabilidad clínica sin la necesidad de equipamiento adicional, permite un acercamiento al concepto de esfuerzo inspirato-rio utilizando el análisis e interpretación de la gráfica ventilatoria para ajustar la ventilación con presión de soporte según el nivel de esfuerzo del paciente y al volumen corriente [63].
Futuras direcciones
Frecuentemente se asume que la sedación profunda induce a minimizar o anular el esfuerzo inspiratorio espontáneo (en inglés denominado “respirolysis”) [67]. El futuro manejo de la ventilación mecánica apunta a minimizar el uso de sedación profunda como práctica clínica rutinaria, incluyendo otras alternativas para el control del esfuerzo inspiratorio [68]. Primero, el desarrollo de características innovadoras del ventilador que mejoran la sincronía entre el paciente y el ventilador, como lo es la asistencia ventilatoria ajustada neuralmente. En segundo lugar, se está introduciendo el concepto de usar dispositivos extracorpóreos, en pacientes con síndrome de dificultad respiratoria aguda severa, con el fin de eliminar el dióxido de carbono excesivo como estímulo indeseable en el centro respiratorio [67],[68]. Por último, el enfoque actual en los ajustes de la ventilación mecánica basado en la demanda muscular respiratoria está permitiendo mitigar la presencia de asincronías sin la necesidad de sedación excesiva.
Conclusiones
Las diferencias entre los conceptos de impulso, esfuerzo y trabajo respiratorio son clave para entender la interacción entre la bomba muscular respiratoria del paciente y el soporte que entrega el ventilador.
Estos tres conceptos, que interactúan entre sí, pueden monitorizarse de manera no invasiva utilizando maniobras o herramientas disponibles en ventiladores mecánicos de cuidados intensivos.
Sin embargo, no todos los ventiladores tienen la posibilidad de medir variables de impulso, esfuerzo o trabajo respiratorio utilizando ventilación con presión de soporte. De las maniobras identificadas, las más disponibles fueron presión de oclusión a los primeros 100 milisegundos y presión de oclusión espiratoria, las cuales tienen creciente evidencia científica y podrían utilizarse para monitorizar impulso y esfuerzo respiratorio en más del 60% de los ventiladores utilizados en Chile. Esto cobra mayor relevancia en tiempos pandémicos, por el gran volumen de pacientes críticos.
Futuros estudios debiesen explorar la precisión y pertinencia de las maniobras no invasivas identificadas en esta revisión.
Notas
Autoría
FR- C: conceptualización, metodología, investigación, curación de datos, preparación del manuscrito original, revisión y edición del artículo, visualización y administración de proyecto. FG- S: conceptualización, metodología, investigación, curación de datos, preparación del manuscrito original, revisión y edición del manuscrito, visualización, y administración de proyecto. JM: conceptualización, revisión y edición del manuscrito y supervisión.
Agradecimientos
Agradecemos a las siguientes instituciones y colaboradores durante la revisión en terreno de los ventiladores de cuidados intensivos en esta revisión: Hospital Metropolitano, Santiago (Nicolás Aguirre y Javier Leiva), Clínica INDISA, Santiago (Felipe Castillo Merino y Juan Enrique Lee Goic), Hospital del Salvador, Santiago (Antonieta Rosales y Andrea Fuentes), Hospital Eduardo Pereira, Valparaíso (Sebastián Castro), Clínica Bicentenario, Santiago (Nicolás Piñeiro), Hospital San Pablo, Coquimbo (Eduardo González), Departamento de Paciente Crítico, Clínica Alemana, Santiago (Agustín Camus- Molina) y DTS – Neyün, Santiago (Roger Burgos, Patricia Espinosa, Michael Espinoza).
Conflictos de intereses
Los autores no tienen conflictos de intereses con la materia de este trabajo.
Financiamiento
Los autores declaran que este trabajo no tuvo financiamiento.
Aspectos éticos
El presente artículo estaría exento de la aprobación de un comité de ética acreditado, debido a que es un artículo de revisión de tipo narrativo.
Origen y arbitraje
No solicitado. Con revisión por pares externa, por tres árbitros a doble ciego.
Idioma del envío
Español.

