Estudios originales
← vista completaPublicado el 24 de septiembre de 2024 | http://doi.org/10.5867/medwave.2024.08.2923
Fulvestrant en la práctica clínica: análisis de efectividad en pacientes uruguayas con cáncer de mama HR+/HER2-
Fulvestrant in clinical practice: Effectiveness analysis in Uruguayan patients with HR+/HER2- breast cancer
Resumen
Introducción Fulvestrant demostró beneficio en sobrevida global y sobrevida libre de progresión en pacientes con cáncer de mama avanzado, con receptores hormonales positivos y receptor de factor de crecimiento epidérmico humano 2 negativo. Se evaluaron las características, la evolución y la sobrevida de pacientes con cáncer de mama receptor hormonal positivo, HER2 negativo, tratadas con fulvestrant, de acuerdo con los protocolos nacionales de cobertura de tratamiento del Fondo Nacional de Recursos. Su objetivo fue conocer la eficacia de fulvestrant en pacientes tratados en la práctica clínica habitual. Se compararon los resultados obtenidos en el presente trabajo con los resultados de los estudios pivotales.
Métodos Se utilizó la base de datos del Fondo Nacional de Recursos, que abarca el período de 2009 a 2022. La evaluación de las curvas de sobrevida se realizó mediante el método Kaplan-Meier y las diferencias se analizaron utilizando el test de Log-Rank.
Resultados Se incluyeron 1085 pacientes con una edad media de 63,66 años. Tras un seguimiento de 14 meses, la mediana de la sobrevida global fue de 16 meses y la de la sobrevida libre de progresión de 6 meses. La presencia de metástasis hepáticas y óseas se asoció con una menor sobrevida global. Los pacientes del sector público y aquellos con una mejor escala de estado funcional experimentaron una mayor sobrevida global.
Conclusiones Los resultados obtenidos ofrecen una perspectiva valiosa para la gestión de tratamientos en un contexto de recursos limitados. La sobrevida global y la sobrevida libre de progresión fueron algo inferiores a los reportados en los ensayos clínicos pivotales. La presencia de metástasis hepáticas y óseas se asoció a un peor pronóstico y una peor sobrevida. Además, los pacientes con peor escala de estado funcional tuvieron una menor sobrevida global. Estos hallazgos subrayan la necesidad de terapias personalizadas, abriendo nuevas líneas de investigación futura.
Ideas clave
- El cáncer de mama tiene la incidencia más alta que cualquier otro tipo de cáncer a nivel mundial, y en Uruguay es la principal causa de muerte por cáncer en mujeres.
- El fulvestrant ha demostrado ser eficaz en el manejo de cáncer de mama avanzado en pacientes posmenopáusicas que previamente no respondieron a tratamientos con antiestrogénicos. Datos disponibles de su uso en la práctica clínica habitual en diversos países reportan resultados similares, aunque con variaciones significativas.
- El estudio resalta la importancia de adaptar la investigación y el tratamiento del cáncer de mama a las realidades de países con recursos limitados. Los resultados subrayan la necesidad de estrategias de manejo personalizado, dada la variabilidad en la respuesta al tratamiento observada.
- Dado que el estudio se realizó bajo condiciones específicas del sistema de salud uruguayo y no incluyó un grupo control, las conclusiones deben interpretarse con precaución. La relevancia de los hallazgos podría estar limitada por estos factores contextuales y metodológicos.
Introducción
El cáncer de mama tiene la incidencia más alta que cualquier otro tipo de cáncer a nivel mundial, con 2,2 millones de casos nuevos en 2020, siendo el tipo de cáncer con mayor prevalencia [1]. En Uruguay, el cáncer es una de las principales causas de muerte de la población; siendo el cáncer de mama la principal causa de muerte por cáncer en mujeres [2].
El fulvestrant es un antagonista puro de los receptores de estrógeno, administrado por vía intramuscular. Tiene afinidad similar al estradiol y genera regulación a la baja del receptor, por lo que reduce la concentración tanto de receptores de estrógeno como de receptores de progesterona de manera dependiente de dosis [3]. Ha demostrado ser eficaz en el manejo de cáncer de mama avanzado, en pacientes posmenopáusicas que previamente no respondieron a tratamientos con antiestrogénicos [4]. Investigaciones adicionales indican que la eficacia de fulvestrant es proporcional a la dosis administrada. En particular, el estudio de fase III CONFIRM reveló que un régimen de dosis de 500 miligramos de fulvestrant es superior al de 250 miligramos, resultando en una prolongación de la supervivencia global de 4,1 meses, favoreciendo la dosis más alta [5].
Dado que los estudios clínicos se realizan con pacientes altamente seleccionados, en condiciones óptimas; los resultados obtenidos en sobrevida y seguridad podrían no ser reproducibles en la práctica clínica habitual. En ella, la mayoría de los pacientes presentan una edad más avanzada, un mayor número de comorbilidades y suelen encontrarse en condiciones menos favorables. En consecuencia, se puede cuestionar si los resultados obtenidos de los estudios clínicos se reproducirán en la práctica clínica cotidiana.
Datos disponibles del uso de fulvestrant en la práctica clínica habitual en Canadá [6], China y Turquía [7,8], indican que en la práctica clínica cotidiana los resultados podrían ser similares al evidenciado en los estudios clínicos aleatorizados. Sin embargo, hay variaciones significativas en los resultados. Por ejemplo, un estudio en Turquía mostró que la mediana de supervivencia libre de progresión fue de nueve meses y la supervivencia global fue de 28 meses, con diferencias según la línea de tratamiento y características del paciente como índice de masa corporal y presencia de metástasis cerebrales [7]. Otro estudio turco reportó que el uso de fulvestrant antes de la quimioterapia mejoraba la supervivencia, con una sobrevida libre de progresión de 6,05 meses y una sobrevida global de 29,70 meses, destacando la importancia de la secuenciación óptima del tratamiento [8]. En contraste, en China la sobrevida libre de progresión reportada fue de 14,1 meses para la primera línea, 11,2 meses para la segunda línea y 6,7 meses para la tercera línea de fulvestrant [9]. Estas diferencias resaltan la necesidad de realizar estudios locales para entender mejor la eficacia de fulvestrant en diferentes contextos clínicos y poblacionales.
En Uruguay, los únicos datos que se disponen sobre la eficacia del fulvestrant en mujeres tratadas en la práctica clínica habitual, son los correspondientes a los obtenidos de un informe realizado por el Fondo Nacional de Recursos en el año 2022 [10].
La incorporación de medicamentos de alto costo a un sistema de cobertura universal requiere estrategias definidas para el control de las indicaciones y la evaluación de los resultados. Fulvestrant, un medicamento costoso, ha sido cubierto financieramente por el Fondo Nacional de Recursos en Uruguay desde 2009. Para lograr resultados similares a los estudios clínicos, el Fondo diseñó una normativa de cobertura basada en la revisión de la evidencia y recomendaciones internacionales. Esta normativa se revisa anualmente para adaptarse a la evolución científica y al contexto de salud uruguayo, permitiendo decisiones fundamentadas y sostenibles. Así, se asegura la calidad, equidad y sustentabilidad del sistema.
En los países de ingresos bajos o medios, resulta de importancia crucial el manejo adecuado de los recursos financieros. Este estudio tiene como objetivo proporcionar datos útiles para personal médico, pacientes y responsables políticos de la financiación sobre las características y evolución de pacientes tratadas con fulvestrant, de acuerdo con la normativa del Fondo Nacional de Recursos.
El objetivo de este estudio fue determinar la sobrevida libre de enfermedad y sobrevida global en pacientes con cáncer de mama hr+/her2˗ tratadas con fulvestrant en segunda línea o más allá.
Métodos
Diseño del estudio
Se trata de un estudio longitudinal analítico basado en datos secundarios.
Población y muestra
La muestra consistió en 1085 pacientes uruguayos diagnosticados con cáncer de mama loco-regionalmente avanzado o diseminado a distancia, receptores hormonales positivos y receptor de factor de crecimiento epidérmico humano 2 negativo. Estos pacientes fueron tratados con fulvestrant a través del Fondo Nacional de Recursos en el período del 1 de enero de 2009 al 30 de diciembre de 2022. Los pacientes fueron seleccionados por conveniencia.
Criterios de selección
Pacientes uruguayos diagnosticados con cáncer de mama avanzado HR+/HER2-, tratados con fulvestrant en el periodo mencionado.
Formularios del Fondo Nacional de Recursos completados por los médicos tratantes, incluyendo edad, sexo, estadio al diagnóstico, estatus menopáusico, procedencia, institución de asistencia médica, tabaquismo, alcoholismo, estado funcional según la escala de East Cooperative Oncology Group (ECOG), fecha de inicio de tratamiento, sitio de metástasis y fecha de muerte o último control.
Recopilación de datos
De los formularios se recabaron los siguientes datos: edad al diagnóstico, sexo, estadio al diagnóstico, estatus menopáusico, procedencia, institución de asistencia médica colectiva donde se atiende el paciente, tabaquismo, alcoholismo, estado funcional según la escala ECOG (donde 0 indica sano y 4 incapacitado), fecha de inicio de tratamiento, sitio de metástasis y fecha de muerte o último control para el cálculo de la sobrevida global. Los pacientes incluidos se atienden en centros asistenciales privados y públicos, tanto de Montevideo como del interior del país. Todos los centros asistenciales del país solicitan el tratamiento con fulvestrant al Fondo Nacional de Recursos. Estos datos permiten caracterizar de manera integral a pacientes con el diagnóstico de cáncer de mama avanzado y evaluar su evolución bajo tratamiento con fulvestrant.
Variables
-
Exposición: tratamiento con fulvestrant.
-
Respuesta (desenlace): sobrevida global y sobrevida libre de progresión.
-
Covariables: edad, estadio al diagnóstico, estatus menopáusico, procedencia, institución de asistencia médica, tabaquismo, alcoholismo, estado funcional según la escala ECOG, sitio de metástasis.
Desenlaces a evaluar
-
Sobrevida global: tiempo desde el inicio del tratamiento con fulvestrant hasta la fecha de muerte por cualquier causa.
-
Sobrevida libre de progresión: tiempo desde el inicio del tratamiento con fulvestrant hasta la fecha de progresión de la enfermedad o muerte, lo que ocurra primero.
Análisis estadístico
Para medir curvas de sobrevida se usó el método de Kaplan-Meier, evaluando las diferencias con el test de Log-Rank. Todos los resultados se consideraron estadísticamente significativos con valores de p < 0,05 (con test de dos colas).
Aprobación ética
Este trabajo fue aprobado por el comité de ética del Hospital de Clínicas Dr. Manuel Quintela de Montevideo. Se incluyeron pacientes que recibieron fulvestrant a través del Fondo Nacional de Recursos en el periodo de 2009 a 2022 que accedieron a que sus datos fueran utilizados en evaluaciones de resultados sanitarios. Los pacientes firmaron un "Consentimiento para el uso de datos personales en evaluaciones de resultados sanitarios". Este consentimiento permite que su información sea utilizada de manera anónima en evaluaciones realizadas por técnicos del Fondo Nacional de Recursos, entidades académicas o científicas avaladas por el mismo, asegurando que los datos personales se mantengan confidenciales y que las evaluaciones se realicen con los más altos estándares de calidad y seguridad. Los pacientes podían optar por no consentir el uso de sus datos. En ese caso, no fueron incluidos en la base de datos utilizada para este estudio.
Resultados
Se incluyeron 1085 pacientes, de los cuales el 98,8% (1072) eran mujeres y el 1,2% (13) eran hombres, con una edad media de 63,66 años. El 51,2% de los pacientes (556) eran procedentes de Montevideo. Al inicio del estudio, el 95% (1031) se encontraba en el Estadio IV. La mayoría de los tumores eran positivos para el receptor de estrógenos (83,2%, 903 pacientes) y para el receptor de progesterona (70,4%, 764 pacientes). Respecto a la presencia de metástasis, el 78,3% (850 pacientes) presentaron metástasis óseas, el 23,7% (257 pacientes) metástasis pulmonares, y el 17,5% (190 pacientes) metástasis hepáticas. El 41,9% de los pacientes (455) tenían exclusivamente metástasis óseas. En cuanto a los hábitos de vida, el 4,9% de los pacientes (53) eran fumadores y el 0,2% (2) consumidores de alcohol. Los detalles adicionales se presentan en la Tabla 1.
Con una mediana de seguimiento de 14 meses (de 0 a 163 meses), la mediana de sobrevida global fue de 16 meses (intervalo de confianza del 95%: de 15 a 18 meses). La sobrevida global a los 2 años fue del 36,0%, disminuyendo al 7% a los 5 años y al 1,2% a los 10 años. La mediana de sobrevida libre de progresión fue de 6 meses, con una sobrevida libre de progresión a los 2 años del 13,1%, disminuyendo al 4,3% a los 5 años y al 1,3% a los 10 años (Tabla 2).
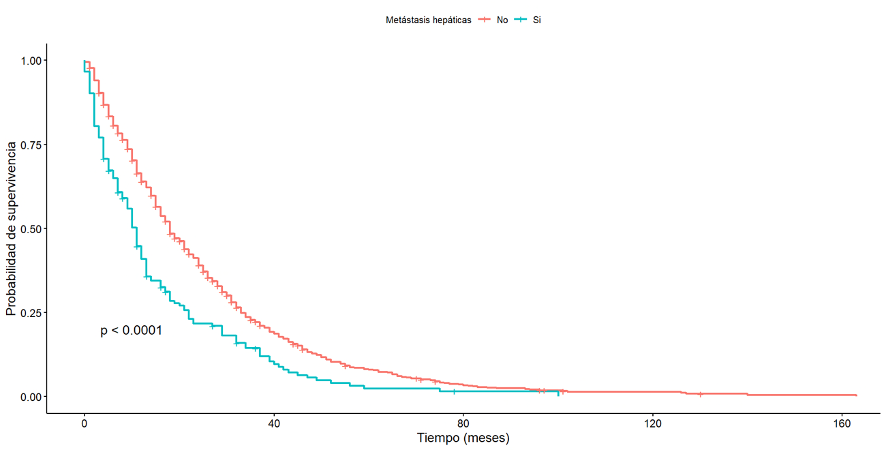
La presencia de metástasis hepáticas y óseas tuvo un impacto significativo tanto en la sobrevida global como en la sobrevida libre de progresión. Los pacientes con metástasis hepáticas mostraron una mediana de sobrevida global de 11 meses (intervalo de confianza del 95%: de 17 a 20), notablemente menor en comparación con una mediana de 18 meses (intervalo de confianza del 95%: de 9 a 12) en pacientes sin estas metástasis (p < 0,0001) (Figura 1). De manera similar, la sobrevida libre de progresión fue significativamente menor en pacientes con metástasis hepáticas (p < 0,001).
Sobrevida global según la presencia o no de metástasis hepáticas.
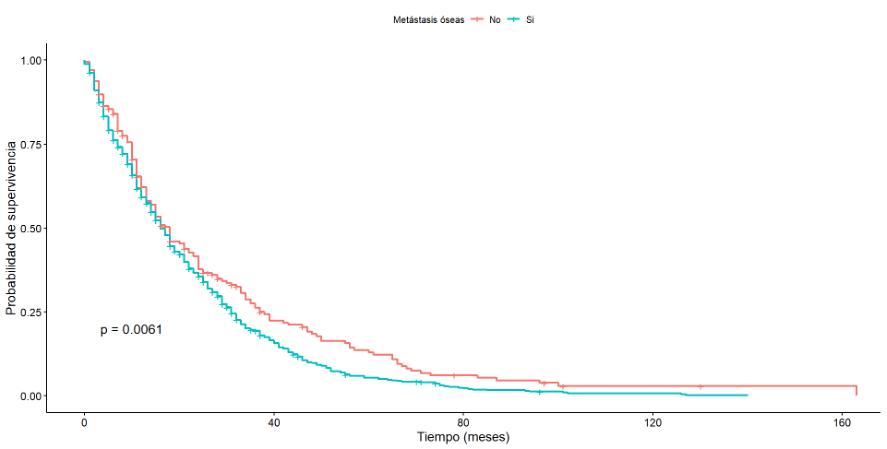
Para pacientes con metástasis óseas, la mediana de sobrevida global fue de 16 meses (intervalo de confianza del 95%: de 15 a 18) en comparación con una mediana de 18 meses (intervalo de confianza del 95%: de 15 a 23) para aquellas sin metástasis óseas, siendo esta diferencia estadísticamente significativa (p = 0,0061) (Figura 2). Este patrón se mantuvo en términos de la sobrevida libre de progresión, donde también se encontraron diferencias estadísticamente significativas entre los grupos con y sin metástasis en sitios óseos (p < 0,001).
Sobrevida global según la presencia o no de metástasis óseas.
En contraste, no se observaron diferencias significativas en la mediana de sobrevida global entre los pacientes con y sin metástasis pulmonares (p = 0,322). Este patrón se mantuvo en términos de la sobrevida libre de progresión (p = 0,939). Igualmente, no hubo diferencias significativas en sobrevida global ni en sobrevida libre de progresión entre pacientes con y sin metástasis encefálicas. En estos casos, la sobrevida global fue de 12 meses (intervalo de confianza del 95%: de 7 a 37) y de 17 meses (intervalo de confianza del 95%: de 15 a 18) respectivamente (p = 0,446), y la sobrevida libre de progresión fue de 5 y 6 meses respectivamente (p = 0,421). Tampoco se hallaron diferencias significativas en sobrevida global ni en sobrevida libre de progresión entre pacientes con y sin metástasis cutáneas/subcutáneas. Aquí, la sobrevida global fue de 17 meses (intervalo de confianza del 95%: de 15 a 18) y 16 meses (intervalo de confianza del 95%: de 12 a 21) respectivamente (p = 0,080), y la sobrevida libre de progresión fue de 6 meses para ambos grupos.
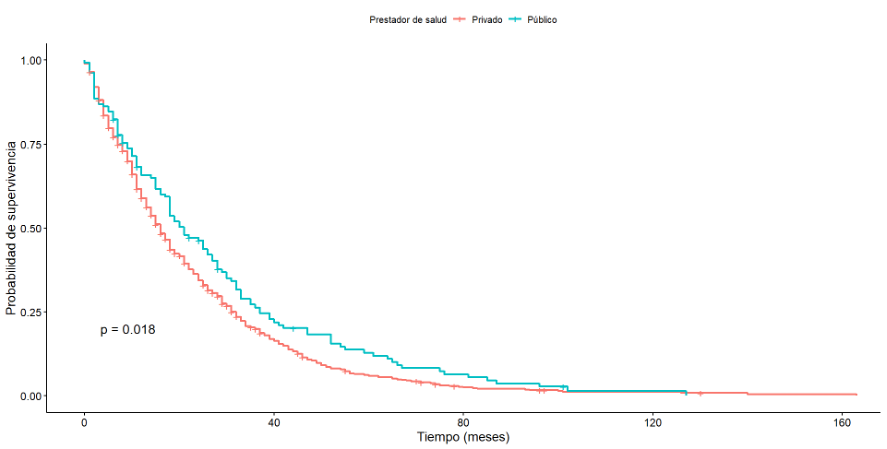
Se encontraron diferencias significativas en la sobrevida global según el prestador de salud (p = 0,018). Esta fue mayor en pacientes atendidos por salud pública en comparación con aquellos asistidos en instituciones privadas (Figura 3). En cambio, no hubo diferencias estadísticamente significativas (p = 0,271) entre los prestadores de salud en la sobrevida libre de progresión.
Sobrevida global según prestador de salud.
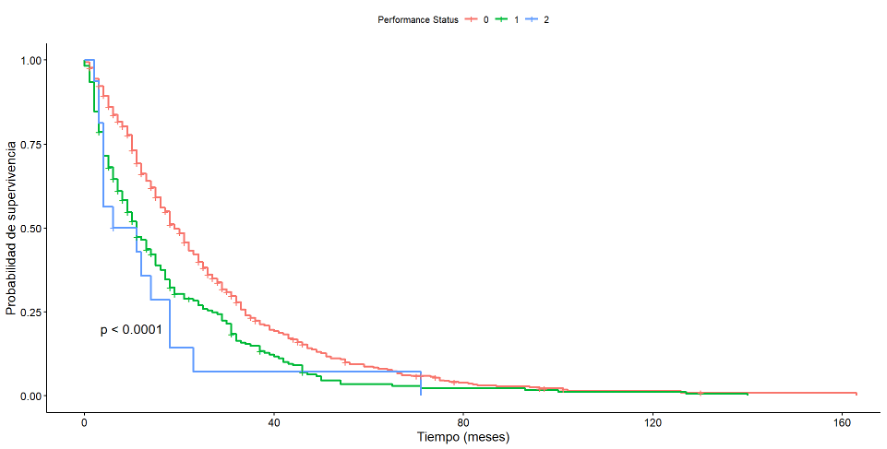
La evaluación del impacto de la escala de estado funcional en la sobrevida de los pacientes reveló diferencias significativas, tanto en la sobrevida global como en la sobrevida libre de progresión. La mediana de sobrevida global fue de 19 meses (intervalo de confianza del 95%: de 18 a 21), 11 meses (intervalo de confianza del 95%: de 9 a 14), y 8,5 meses (intervalo de confianza del 95%: de 4 a 23) para pacientes con estado funcional de 0, 1 y 2 según la escala ECOG, respectivamente (p < 0,0001; Figura 4). Mientras que la mediana de sobrevida libre de progresión fue de 7 meses (intervalo de confianza del 95%: de 6 a 8), 5 meses (95%: de 4 a 6), y 5 meses (95%: de 3 a 15) para pacientes con estado funcional de 0, 1 y 2 respectivamente (p < 0,00035).
Sobrevida global según escala de estado funcional .
No se observaron diferencias en la sobrevida global (p = 0,726), ni en la sobrevida libre de progresión (p = 0,398) entre pacientes procedentes de Montevideo y el resto del interior del país.
En el modelo de Cox para la sobrevida global, las variables escala de estado funcional y presencia de metástasis hepáticas resultaron significativas en los modelos simples. En el modelo múltiple dichas variables no cumplieron la proporcionalidad de los riesgos, de modo que fueron utilizadas como variables de estratificación. La variable presencia de metástasis hepáticas resultó también significativa en el modelo simple. Sin embargo, no mostró proporcionalidad en el riesgo, de modo que para el modelo múltiple fue incorporada como variable de estratificación (Tabla 3).
Discusión
La distribución de recursos para tratamientos hormonales en el cáncer de mama representa un reto significativo, tanto para los formuladores de políticas de salud como para las entidades que financian estos medicamentos [11,12]. La naturaleza selectiva y las condiciones ideales de los estudios clínicos a menudo no reflejan la complejidad de la práctica clínica diaria, donde los pacientes generalmente son de mayor edad y presentan más comorbilidades [13,14,15,16]. Esto suscita preguntas sobre la aplicabilidad de los resultados de los estudios clínicos en escenarios reales de atención médica.
Este estudio ofrece una visión valiosa sobre el pronóstico de pacientes uruguayos con cáncer de mama, revelando posibles diferencias respecto a los hallazgos de estudios clínicos. La inclusión de pacientes en un contexto de la práctica clínica cotidiana proporciona una perspectiva más representativa que la que a menudo se ve en investigaciones controladas. Además, los hallazgos sobre la eficacia del fulvestrant en la práctica cotidiana contribuyen a una base de datos más sólida, crucial para tomar decisiones políticas sobre la financiación de este tratamiento [17].
La mediana de la sobrevida global en el presente estudio fue de 16 meses y la sobrevida libre de progresión de 6 meses. Estos resultados son inferiores a los del estudio pivotal CONFIRM [5], que reportó medianas de sobrevida global y sobrevida libre de progresión de 25,1 y 22,8 meses, respectivamente. También son menores que los observados en pacientes occidentales de estudios realizados en la práctica clínica cotidiana, donde la sobrevida global con fulvestrant en segunda línea fue de 16 meses y la sobrevida libre de progresión de 12 meses [6], así como en estudios con pacientes orientales, donde la sobrevida libre de progresión fue de 11,6 meses [9]. No obstante, en el presente estudio la sobrevida libre de progresión resultó similar a la reportada en otros estudios, mientras que la sobrevida global resultó inferior [7,8]. Al interpretar estos resultados, es crucial considerar que se desconoce el volumen de pacientes que presentaban metástasis encefálicas, un factor que podría alterar el pronóstico. Además, también se desconocen los tratamientos que los pacientes recibieron luego de la progresión de la enfermedad lo que podría afectar significativamente la sobrevida global.
Los pacientes con una escala de estado funcional más alta tuvieron peor sobrevida global, siendo esta diferencia estadísticamente significativa. Esto se debe a que el estado funcional es un indicador pronóstico independiente, ya que refleja el estado general de salud y la capacidad de tolerancia al tratamiento. Los pacientes con escala de estado funcional 0 presentan un mejor estado de salud y tienden a tener una mayor sobrevida global, que aquellos con escala de estado funcional más elevado [18].
En lo que se refiere a la sobrevida global según la topografía de las metástasis, la presencia de metástasis cutáneas/subcutáneas o pulmonares no impactó en la sobrevida global. Por su parte, la presencia de metástasis hepáticas y óseas se asociaron a una menor sobrevida global. Esto podría indicar que se vinculan a un peor pronóstico, siendo esto concordante con lo ya reportado [19]. Es importante señalar que en el estudio CONFIRM [5], los pacientes con metástasis hepáticas extensas fueron excluidos. Para el presente estudio, la información sobre la carga hepática no estaba disponible. Esto podría sugerir que la hormonoterapia exclusiva podría no ser la mejor opción ante una carga metastásica hepática y/u óseas significativa. Esto es especialmente relevante, considerando que el tratamiento combinado con inhibidores de ciclinas-dependientes quinasas 4/6 ha demostrado mejorar el pronóstico de los pacientes con cáncer de mama avanzado receptores hormonales positivos [20].
En este estudio se incluyeron 1085 pacientes portadores de cáncer de mama con receptores hormonales positivos y receptor de factor de crecimiento epidérmico humano 2 negativo, de los cuales la mayoría eran mujeres (98,8%), con una mediana de edad de 63,66 años. Esto es concordante con lo reportado en estudios que evalúan la eficacia del tratamiento con fulvestrant en población occidental [6].
La prevalencia de tabaquismo encontrada en el estudio fue del 4,9%, un valor considerablemente más bajo en comparación con las tasas reportadas en la población general uruguaya. Según datos de la Encuesta Global de Tabaquismo en Adultos realizada en Uruguay durante el período de 2016 a 2017, la tasa de consumo de tabaco en mujeres fue del 18%, mientras que en 2009 fue del 24,1% [21]. Esta discrepancia sugiere que podría haber un subregistro en los datos de tabaquismo en la muestra. El subregistro podría estar relacionado con varios factores, como la reticencia de los pacientes a reportar hábitos de tabaquismo o la falta de documentación completa en los registros médicos. Futuras investigaciones deberían abordar estos posibles sesgos y buscar métodos para obtener datos más precisos sobre el consumo de tabaco entre pacientes con cáncer de mama en Uruguay.
Dentro de las fortalezas del presente estudio se destacan el tamaño de la muestra. Se incluyó un número considerable de pacientes, lo que proporciona una base de datos robusta para el análisis y aumenta la fiabilidad de los resultados, así como un largo período de seguimiento. Además, se incluyeron pacientes de la práctica clínica cotidiana, lo que constituye una fortaleza clave, ya que refleja una variedad más amplia de situaciones clínicas que los ensayos controlados. Esto permite una mejor generalización de los resultados a la población general, brindando información valiosa sobre la efectividad del fulvestrant en un contexto práctico y en pacientes con diferentes comorbilidades. Estos hallazgos son especialmente relevantes para la toma de decisiones en la práctica médica y la política de salud pública.
Las limitaciones del presente estudio incluyen la dependencia de la base de datos secundaria entregada por el Fondo Nacional de Recursos, restringiendo el acceso solo a los datos registrados y compartidos por ellos. Un aspecto crítico es el sesgo de información introducido por la falta de detalles sobre por qué los pacientes dejaron de recibir fulvestrant. Aunque la progresión de la enfermedad parece ser la causa principal, hay un sesgo potencial por aquellos que se perdieron en el seguimiento o discontinuaron el tratamiento por otros motivos. Además, la ausencia de datos sobre terapias post fulvestrant limita el análisis sobre la eficacia total de los tratamientos. Este factor es relevante, ya que las terapias posteriores pueden influir significativamente en la sobrevida global de los pacientes, lo que podría explicar al menos en parte, los resultados obtenidos en sobrevida global, aunque no para los resultados en sobrevida libre de progresión. En este contexto, tampoco se contó con datos sobre la presencia de metástasis del sistema nervioso central que son relevantes para la comprensión completa de la progresión de la enfermedad.
Conclusiones
Este estudio representa, hasta donde se conoce, el primer análisis exhaustivo en América Latina sobre pacientes diagnosticados con cáncer de mama avanzado con receptores hormonales positivos, receptor de factor de crecimiento epidérmico humano 2 negativo; tratados con fulvestrant en segunda línea o más allá.
Con un gran número de pacientes y un seguimiento prolongado, el estudio cumple sus objetivos brindando una visión valiosa sobre los resultados, el pronóstico de los pacientes y sobrevida en la práctica clínica habitual.
Los resultados obtenidos fueron algo inferiores a los reportados en los estudios pivotales, destacando la importancia de la investigación local para guiar la práctica clínica y las políticas de salud. Las metástasis hepáticas y óseas se asociaron con un peor pronóstico y una peor sobrevida.
Es crucial continuar con estudios locales que mejoren las estrategias de tratamiento en función del contexto específico. Además, se deben implementar políticas de salud que aseguren la gestión eficiente de los recursos financieros, especialmente en países de ingresos bajos y medios, para mejorar la efectividad del tratamiento y la gestión de recursos en el cuidado de la salud.

