Estudios originales
← vista completaPublicado el 21 de octubre de 2021 | http://doi.org/10.5867/medwave.2021.09.8474
Efectividad del uso de biosimilares en el tratamiento de la anemia en pacientes con enfermedad renal crónica: serie de casos
Effectiveness of biosimilar drugs in the treatment of renal anemia: A case series
Resumen
Introducción Los pacientes con enfermedad renal crónica presentan anemia que, en gran parte, se debe a un defecto en la producción de eritropoyetina. La aparición de fármacos biosimilares de agentes estimulantes de la eritropoyesis garantiza un acceso más generalizado a dichos fármacos.
Objetivo Los pacientes con enfermedad renal crónica presentan anemia que, en gran parte, se debe a un defecto en la producción de eritropoyetina.
Método Se trata de un estudio observacional retrospectivo, en el que analizamos datos de 111 pacientes consecutivos de las consultas de nefrología con enfermedad renal crónica, anemia y con criterios de uso de agentes estimulantes de la eritropoyesis. Recogimos datos basales epidemiológicos y de comorbilidad, así como hematológicos y de función renal. Analizamos la efectividad del fármaco en aquellos pacientes naïve así como en aquellos que ya tenían otros agentes estimulantes de la eritropoyesis, y que habían iniciado tratamiento con el biosimilar.
Resultados De los 111 pacientes incluidos, el 54% eran varones y la edad media se situó en 83 ± 8 años. En los pacientes que ya estaban en tratamiento con agentes estimulantes de la eritropoyesis, el uso del biosimilar mantuvo los valores de hemoglobina a los dos meses de tratamiento, mientras que en el grupo naïve se produjo un ascenso significativo de los mismos (p < 0,001). No hubo cambios en la función renal en ninguno de los grupos. El costo del uso de agentes estimulantes de la eritropoyesis se redujo una media de 82 ± 17% con el uso del biosimilar.
Conclusiones El uso de un biosimilar de epoetina αα es efectivo en pacientes con enfermedad renal crónica y genera una importante reducción de costos.
Ideas clave
|
Introducción
La anemia es una complicación habitual en los pacientes con enfermedad renal crónica. En general, obedece a una etiología múltiple y aumenta a medida que se deteriora el filtrado glomerular [1]. Las causas de anemia en la enfermedad renal crónica incluyen la ferropenia, la deficiencia de vitamina B12, de ácido fólico, las toxinas urémicas, las alteraciones del metabolismo mineral, la inflamación o el uso de determinados fármacos con capacidad mielotóxica y, sobre todo, la disminución de la capacidad para la producción de eritropoyetina a nivel renal [2]. Para paliar esta situación, en el momento actual disponemos de fármacos biológicos como los agentes estimulantes de la eritropoyesis. Desde su aparición, los agentes estimulantes de la eritropoyesis no solo han sido capaces de mejorar la calidad de vida de los pacientes y reducir el número de transfusiones, si no que han demostrado su capacidad para reducir la mortalidad y las hospitalizaciones de los pacientes con enfermedad renal crónica y anemia [3],[4]. Sin embargo, estos agentes no están exentos de efectos adversos. Además, su uso indiscriminado impacta de manera notable en la incidencia de eventos cardiovasculares, hipertensión o trombosis [5].
Los fármacos biológicos presentan un elevado costo, derivado de su intenso desarrollo y evaluación, lo que puede generar falta de equidad en su acceso para determinados grupos de pacientes. En el año 2008 se comercializó en España el primer fármaco biosimilar de epoetina α. Los fármacos biosimilares son productos similares a la molécula original, pero con un desarrollo específico e independiente, no idéntico, que deben ser capaces de demostrar su no inferioridad respecto al fármaco de referencia [6]. La regulación en la aprobación de fármacos biosimilares corre a cargo de la Agencia Europea del Medicamento desde el año 2005, e incluye la realización de ensayos clínicos fase 1 y 3 previo a su lanzamiento [7]. Hasta el momento de redacción de este trabajo, existen en Europa más de 60 fármacos biosimilares comercializados.
En el caso de los biosimilares de epoetina α, se han llevado a cabo algunos ensayos clínicos demostrando su perfil de seguridad en los estudios de fase 1 y su efectividad en los de fase 3 [8],[9]. Además, a la fecha de elaboración del presente estudio se están llevando a cabo estudios post autorización que tienen como objetivo reevaluar la efectividad y seguridad a largo plazo de dichos fármacos. Sin embargo, los estudios observacionales en vida real publicados hasta la fecha presentan algunas limitaciones. En términos generales, son heterogéneos en la inclusión de pacientes con y sin enfermedad renal crónica. Además, analizan la efectividad de los biosimilares en su conjunto sin que dispongamos hasta ahora de evidencia sobre agentes concretos en poblaciones determinadas. En el caso concreto de la epoetina α, los estudios disponibles en vida real son muy escasos, tanto de inicio del biosimilar como de cambio desde otros agentes estimulantes de la eritropoyesis.
El objetivo del presente estudio es evaluar el uso de un fármaco biosimilar de epoetina α en vida real en pacientes con enfermedad renal crónica. Para ello se analizó su efectividad y eficiencia tanto en pacientes que no recibían agentes estimulantes de la eritropoyesis como en pacientes que estaban siendo tratados.
Método
Diseño del estudio
Realizamos un estudio observacional retrospectivo. En él se incluyó a pacientes consecutivos de las consultas externas de nefrología, en los que se había iniciado un fármaco biosimilar de epoetina α en nuestro centro (Hospital Universitario de La Princesa) en el año 2018.
Participantes
Como criterios de inclusión se estableció que fueran pacientes mayores de 18 años, con enfermedad renal crónica estadio 3 o superior, con criterios de inicio de agentes estimulantes de la eritropoyesis o que ya estuvieran en tratamiento con ellos y mantuvieran dichos criterios. Para definir los criterios nos basamos en las guías Kidney Disease: Improving Global Outcomes (KDIGO) de anemia y las National Institute for Health and Care Excellence (NICE) publicadas en 2012 y 2015, respectivamente [10],[11]. De esta manera, iniciamos los agentes estimulantes de la eritropoyesis con cifras de hemoglobina inferiores a 10,5 gramos por decilitro para mantener un rango entre 10,5 y 11,5 gramos por decilitro y evitando aumentos superiores a 2 gramos por decilitro en un mes. Excluimos del estudio a pacientes con ferropenia o déficit de ácido fólico y vitamina B12, que hubieran tenido un ingreso hospitalario durante el estudio o en los dos meses antes del inicio del fármaco o que tuvieran alguna contraindicación para el uso de este. No se incluyó a los pacientes que no disponían de datos clínicos completos.
Variables
Haciendo uso de las mismas guías, definimos ferropenia absoluta como índice de saturación de transferrina inferior a 20% y ferritina inferior a 100 microgramos por decilitro, y déficit funcional de hierro como índice de saturación de transferrina inferior a 30% y ferritina inferior a 500 microgramos por decilitro.
En el momento basal se recogieron datos demográficos, de función renal (creatinina y filtrado glomerular estimado por la Chronic Kidney Disease Epidemiology Collaboration, CKD-EPI), hemoglobina, índice de saturación de transferrina, ferritina y uso previo de hierro [12]. Clasificamos a los pacientes en los estadios de enfermedad renal crónica en función del filtrado glomerular estimado [13].
En los pacientes que estaban en tratamiento con agentes estimulantes de la eritropoyesis, recogimos el agente que utilizaban y la dosis. Utilizamos un factor de conversión para realizar el cambio de agentes estimulantes de la eritropoyesis al biosimilar que consistió en mantener la dosis en el caso de epoetina β, multiplicar por 200 la dosis semanal en microgramos de darbepoetina α y multiplicar por 800 la dosis de metoxi-polietilenglicol epoetina β (también en microgramos) [14].
Se estableció una comparación de las variables recogidas en dos grupos, comparándose aquellos que recibían agentes estimulantes de la eritropoyesis frente a los que no.
Fuentes
Se utilizó como fuente la historia clínica electrónica.
Sesgos
Los potenciales sesgos de diseño (observacional), confusión y selección se intentaron paliar con la inclusión de una población homogénea y completa.
Tamaño muestral
Se determinó haciendo uso del registro clínico incluyendo a todos los pacientes con necesidad de agentes estimulantes de la eritropoyesis y que hubieran recibido un biosimilar.
Variables cualitativas (de resultado)
Teniendo en cuenta las guías clínicas, ficha clínica y protocolo de práctica clínica en nuestro medio, se evaluó a los pacientes a los dos meses del inicio del tratamiento con el biosimilar para analizar los cambios en la hemoglobina y en la función renal.
Métodos estadísticos
Las variables se expresan como media ± desviación estándar si siguen una distribución normal (según el test de Kolmogorov-Smirnov) o como mediana (rango intercuartílico) en caso contrario. Para la inferencia estadística utilizamos los tests Chi-cuadrado o test de Fisher y t de student o de Mann-Whitney en función de los resultados de la normalidad, tanto para comparar las características basales entre los grupos con y sin agentes estimulantes de la eritropoyesis como en el análisis a los dos meses de seguimiento. Para el análisis de costo, realizamos una evaluación económica completa, teniendo en cuenta los resultados clínicos y los costos, mediante un análisis de costo efectividad-incremental [15].
Todos los análisis estadísticos se realizaron con el programa SPSS (SPSS Inc., Chicago, IL) versión 21.0. Se consideró estadísticamente significativo un valor p < 0,05.
Resultados
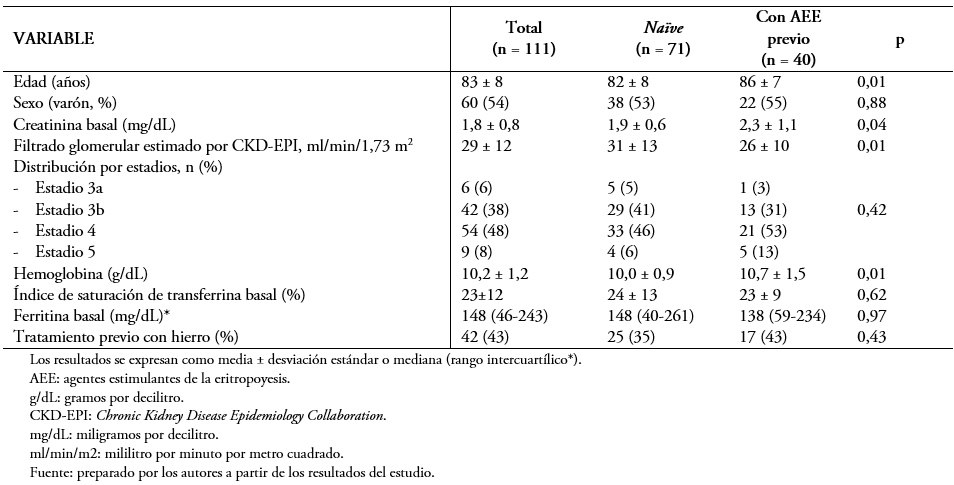
Se incluyó a 111 pacientes procedentes de las consultas externas de nefrología, con una edad media de 83 ± 8 años y de los que 60 (54%) eran varones. La distribución por estadios de la enfermedad renal crónica demostró que la mayoría de los pacientes presentaban un estadio 3b (42,38%) o 4 (54,48%). La creatinina media se situó en 1,8 ± 0,8 miligramos por decilitro y el filtrado glomerular estimado por CKD-EPI en 29 ± 12 mililitro por minuto por 1,73 metros cuadrados. En cuanto a los parámetros hematológicos, la hemoglobina media fue de 10,2 ± 1,2 gramos por decilitro. El resto de las características basales se muestran en la Tabla 1.
 Tamaño completo
Tamaño completo Setenta y un pacientes (64%) no recibían ningún tratamiento con agentes estimulantes de la eritropoyesis en el momento del inicio del estudio. De los 40 (36%) pacientes que sí recibían algún tipo de agentes estimulantes de la eritropoyesis, la mayoría se administraban metoxi-polietilenglicol epoetina β (72,5%), seguido de darbepoetina α (25%) y sólo una paciente epoetina β (2,5%). En la Tabla 2 se especifican las dosis basales medias de cada uno de ellos.
 Tamaño completo
Tamaño completo Realizamos una comparación entre los pacientes que recibían agentes estimulantes de la eritropoyesis y los que no. Encontramos que había diferencias significativas en la edad, la creatinina y el filtrado glomerular basal y la hemoglobina basal.
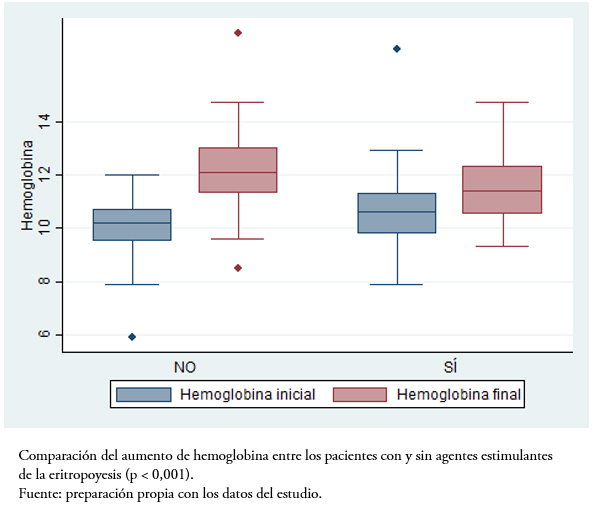
Tras el inicio del tratamiento con el fármaco biosimilar, analizamos la variación en los parámetros analíticos hematológicos y de función renal a los dos meses. Los pacientes naïve de agentes estimulantes de la eritropoyesis aumentaron significativamente las cifras de hemoglobina tras el inicio del biosimilar (diferencia entre las cifras basales y a los dos meses: 2,2 ± 1,4 gramos por decilitro, p < 0,001). Como era de esperar, en los pacientes a los que se realizó el cambio desde otros agentes estimulantes de la eritropoyesis, no se encontraron diferencias tras el inicio del biosimilar (0,6 ± 1,8 gramos por decilitro, con un valor de p no significativo). No hubo diferencias en la variación del filtrado glomerular estimado por CKD-EPI entre los pacientes naïve y los que recibían agentes estimulantes de la eritropoyesis (+1,7 ± 6,2 versus -0,1 ± 5,7, p = 0,23) (Figura1).
 Tamaño completo
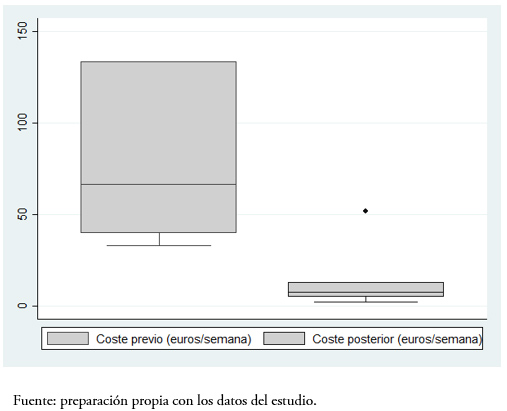
Tamaño completo El cambio al biosimilar supuso una reducción de costos de una media de 83 ± 11% frente al precio inicial (costo previo 81 ± 41 versus 10 ± 7 euros por semana, p < 0,001) (Figura 2). En la Tabla 3, se muestra la evaluación económica completa en ambos grupos del estudio, demostrándose un ahorro de 131 euros por unidad de hemoglobina y paciente con el uso del biosimilar.
 Tamaño completo
Tamaño completo 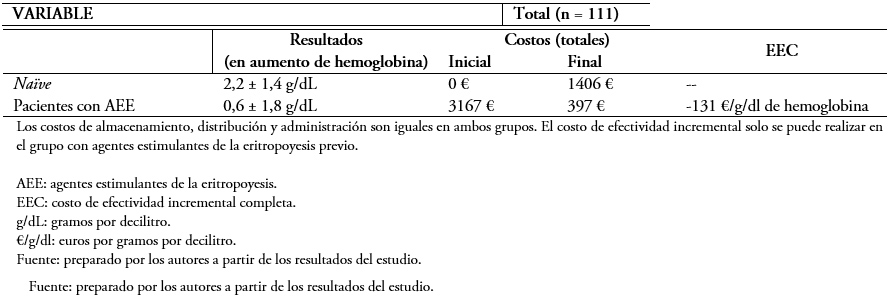 Tamaño completo
Tamaño completo No se registró ningún efecto adverso con el uso del biosimilar de epoetina α.
Discusión
Los resultados de nuestro estudio, por primera vez en vida real, confirman que los pacientes con anemia y enfermedad renal crónica sin tratamiento con agentes estimulantes de la eritropoyesis alcanzan un beneficio en términos de hemoglobina al recibir un biosimilar con un excelente perfil de seguridad. Además, aquellos que ya recibían tratamiento con agentes estimulantes de la eritropoyesis mantienen las cifras de hemoglobina tras el cambio al biosimilar, pero alcanzando una importante eficiencia. Este relevante ahorro en costos ha demostrado permitir un mayor acceso a tratamientos biológicos a más población, lo que supone un impacto clínico significativo. Concretamente, nuestros datos en vida real reflejan una reducción de más del 80% en los pacientes a los que se les realiza el cambio. Esta mejor eficiencia se había demostrado ya en un artículo publicado sobre un modelo de costos usando teóricamente un paciente con anemia inducida por cáncer en diferentes regiones del mundo, aunque no con tanta contundencia como reflejan nuestros datos [16].
El uso de biosimilares de epoetina α en la enfermedad renal crónica ha sido reportado en diferentes estudios con resultados similares a los nuestros. En cuanto al aumento en las cifras de hemoglobina en los pacientes que no recibían agentes estimulantes de la eritropoyesis, nuestros datos reflejan una media de 2,2 ± 1,4 gramos por decilitro a los dos meses de seguimiento. Uno de los pocos estudios que revela datos cuantitativos de la efectividad de los biosimilares fue el derivado del registro italiano de Treviso publicado por Ingrasciotta y colaboradores [17]. En dicho estudio se incorporó a todos los pacientes que habían recibido cualquier biosimilar de epoetina incluyendo a aquellos con enfermedad renal crónica y cáncer. El aumento en la hemoglobina fue significativo en el subgrupo de pacientes con enfermedad renal crónica (1,5 ± 1,1 gramos por decilitro) a los tres meses de tratamiento, sin diferencias frente a los pacientes que recibían el fármaco de referencia (1,6 ± 1,1 gramos por decilitro). Cabe destacar que la respuesta a los agentes estimulantes de la eritropoyesis tiene múltiples factores implicados como la inflamación, la uremia, la presencia de neoplasias, la nutrición o la interacción farmacológica. Aunque en nuestro estudio, los pacientes responden de manera homogénea a los biosimilares, la resistencia al uso de agentes estimulantes de la eritropoyesis debe ser evaluada y tratada con el fin de evitar riesgos relacionados con la excesiva dosificación de los mismos [18].
En el subgrupo de pacientes que ya recibían agentes estimulantes de la eritropoyesis analizamos la variación de la hemoglobina tras el cambio (switch) al biosimilar. Tras dos meses de seguimiento, no encontramos diferencias en las cifras de hemoglobina antes y después del cambio. En un estudio analizado por pareamiento por puntaje de propensión publicado por Belleudi y colaboradores, se analiza la efectividad y seguridad en el cambio de un agente estimulante de la eritropoyesis por un biosimilar. Basándose en una red de estudio de fármacos biosimilares (ItaBioNet), los autores obtienen información de 14 400 pacientes incidentes en el uso de agentes estimulantes de la eritropoyesis para anemia, de los cuales 1866 cambian a un biosimilar [19]. Los resultados en términos de efectividad concluyeron con la no inferioridad del fármaco biosimilar con similares efectos adversos a los publicados en pacientes con agentes estimulantes de la eritropoyesis [5].
A pesar de que la edad se considera un predictor de falta de respuesta a los agentes estimulantes de la eritropoyesis, la edad media de los pacientes de nuestro estudio se situó en 83 ± 8 años superando a la de los estudios publicados con anterioridad y demostrando la efectividad del fármaco incluso en poblaciones envejecidas [20]. Además, en nuestra serie encontramos diferencias en la edad media de ambos grupos (naïve y aquellos que ya recibían agentes estimulantes de la eritropoyesis), sin que eso supusiera un cambio en la respuesta esperable a uso del biosimilar.
En cuanto a los efectos adversos, no detectamos ninguno relevante tras los dos meses de seguimiento. El estudio post-autorización realizado con el mismo agente que nuestro estudio (EPO-PASS) reveló reacciones adversas con frecuencias similares a la esperadas. En dicho estudio, ningún paciente desarrolló anticuerpos frente a epoetina, ni anemia pura de células rojas [21].
Nuestro estudio no está exento de limitaciones. Por un lado, posee las propias de un estudio retrospectivo y observacional tales como la pérdida de datos en el seguimiento o el uso de la historia clínica como fuente. Sin embargo, en este estudio se siguieron las recomendaciones de las guías clínicas por lo que los pacientes presentaban determinaciones seriadas de hemoglobina. Además, aquellos pacientes en los que no disponíamos de información clínica en términos de efectividad fueron excluidos del estudio para que fuera más homogéneo. Por otro lado, el tamaño muestral y la falta de seguimiento también constituyen limitaciones. Sin embargo, a pesar de ello, los resultados obtenidos son concluyentes para el análisis tanto de efectividad como de eficiencia, ambos objetivos de la serie presentada, siendo esta la mayor publicada hasta la fecha. La decisión de marcar un punto de evaluación de dos meses radica en las guías clínicas y la ficha técnica del fármaco, que además coincide con nuestra práctica clínica habitual [10],[11]. Esta evaluación nos permite determinar los resultados que produce el biosimilar en pacientes estables y a corto plazo. En cualquier caso, debemos ser cautos con la extrapolación de datos de estudios observacionales atendiendo a las limitaciones inherentes de los mismos.
Además, los resultados de seguridad en nuestro caso solo se refieren a los dos primeros meses tras el inicio del fármaco, por lo que hacen falta estudios a más largo plazo para comprobar dicha situación en vida real. Finalmente, encontramos diferencias esperables entre los dos grupos de estudio en sus características basales (edad, hemoglobina y función renal) que no creemos que interfieran en los resultados del estudio. Además, estas diferencias son lógicas atendiendo a que unos se encontraban en tratamiento previo con agentes estimulantes de la eritropoyesis (los que tenían más disfunción renal y mejores cifras de hemoglobina).
Conclusión
El uso de un fármaco biosimilar de epoetina α es efectivo para aumentar los niveles de hemoglobina en pacientes sin tratamiento con agentes estimulantes de la eritropoyesis. Además, supone una importante reducción de costos frente al uso de los fármacos de referencia.
Sin duda, nuestros resultados abren nuevas evidencias en el uso de biosimilares que tendrán que ser refrendados en posteriores estudios a más largo plazo, también en vida real y abordando la importancia de la eficiencia. Por otro lado, el campo de los fármacos biosimilares aún permanece con muy poco desarrollo, por lo que es deseable que la investigación clínica avance y su uso se pueda universalizar.
Notas
Roles de autoría
PMR: diseño del estudio, adquisición de datos, revisión y aprobación de la versión final. YGG: adquisición de datos, revisión y aprobación de la versión final. VAC: diseño del estudio, redacción del artículo. BQ: diseño del estudio, adquisición de datos, análisis e interpretación, redacción del artículo.
Conflictos de intereses
BQ y VA han participado en ponencias remuneradas por parte de Sandoz con el contenido de la presente investigación.
Financiamiento
Los autores declaran que no han recibido financiamiento para la realización del presente trabajo.
Consideraciones éticas
Aprobado por el Comité Ético de Investigación Clínica de Cantabria obteniendo la adecuación del Hospital Universitario de la Princesa el 9 de octubre de 2017.
Disponibilidad de datos
Disponibilidad de entrega de datos a solicitud.

