Revisión clínica
← vista completaPublicado el 11 de diciembre de 2021 | http://doi.org/10.5867/medwave.2021.11.002132
Troponinas cardíacas: información actual sobre las principales características analíticas de los métodos para la determinación y nuevas posibilidades diagnósticas
Cardiac troponins: current information on the main analytical characteristics of determination methods and new diagnostic possibilities
Resumen
Los métodos de determinación utilizados en el diagnóstico de laboratorio de enfermedades cardiovasculares se mejoran constantemente, lo que conduce a un cambio en la percepción del valor diagnóstico de los biomarcadores de laboratorio y al surgimiento de nuevas posibilidades de diagnóstico. Uno de los ejemplos sorprendentes de esto son los principales biomarcadores utilizados para el diagnóstico de laboratorio del infarto agudo de miocardio: las troponinas cardíacas. Los primeros métodos para determinar las troponinas cardíacas, propuestos hace unos 30 años, se caracterizaban por una sensibilidad extremadamente baja. Por lo tanto, solo podían detectar infartos agudos de miocardio de amplia zona. Estos métodos también se caracterizaron por una baja especificidad, que se expresó en una alta probabilidad de reactividad cruzada de anticuerpos de diagnóstico con isoformas de troponina esquelética, acompañada de resultados falsos positivos en miopatías esqueléticas y lesiones músculo esqueléticas. Con la introducción de troponinas cardíacas de alta sensibilidad en la práctica clínica, la posibilidad de diagnóstico precoz y exclusión del infarto agudo de miocardio mediante la evaluación de la cinética de la concentración de troponinas en las primeras horas (de 0 a 1 hora, de 0 a 2 horas y de 0 a 3 horas) se ha vuelto más específica desde el momento en que el paciente ingresa a urgencias. Además, algunas de nuestras ideas sobre la biología de las troponinas cardíacas han cambiado, y han surgido nuevas oportunidades prometedoras para su uso en medicina. Esta revisión sistematiza los datos actuales sobre el valor diagnóstico de las troponinas cardíacas, los principales métodos de su determinación y sus características analíticas desde los puntos de vista histórico y moderno.
|
Ideas clave
|
Introducción
El complejo de troponina del tejido del músculo cardíaco estriado consta de tres moléculas de proteína: troponina I (cTnI), troponina T (cTnT), troponina C (cTnC), que junto con la proteína tropomiosina juegan un papel importante en la regulación de la contracción y relajación de la capa muscular del corazón [1]. La estructura de aminoácidos de las moléculas de proteína del complejo de troponina es importante para mantener el papel funcional de estas proteínas. Así, según estudios genéticos, se encontró una gran cantidad de mutaciones diferentes en genes que codifican moléculas proteicas del complejo de troponina. Estos fueron la causa de trastornos hereditarios graves y potencialmente mortales de la función contráctil del tejido del músculo cardíaco, conocidos como miocardiopatías [2]. En dos de los tres componentes del complejo de troponina del miocardio (troponina I y troponina T), la estructura de aminoácidos difiere de los componentes proteicos del complejo de troponina de los músculos esqueléticos, lo que los hace únicos y permite usarlos como biomarcadores para detectar daño miocárdico isquémico en el infarto agudo de miocardio. La estructura de aminoácidos de troponina C es la misma en los tejidos del músculo cardíaco y esquelético y, por lo tanto, esta proteína no tiene especificidad para el diagnóstico de laboratorio de infarto agudo de miocardio. Aunque se cree que las troponinas I y T se localizan sólo en el miocardio, algunos investigadores han destacado la expresión extramiocárdica de las troponinas I y T, concretamente en el tejido del músculo esquelético [3],[4],[5], en la membrana muscular de las paredes de la vena cava y las venas pulmonares en humanos y otros mamíferos [6]. Teniendo en cuenta estos datos, las troponinas I y T no pueden considerarse cardiomarcadores absolutamente específicos. Es por este motivo que se debe continuar el estudio de las causas y mecanismos de la expresión extramiocárdica de las troponinas cardíacas.
El tejido muscular cardíaco contiene aproximadamente de cuatro a seis miligramos de troponina I y de 10 a 11 miligramos de troponina T en un gramo. Aproximadamente, 95% de esta cantidad es parte del complejo de troponinas (fracción estructural de troponinas) y ambas participan en la función contráctil del miocardio. El otro 5% de las moléculas de troponinas I y T del total de troponinas se localizan directamente en el citosol de las células del miocardio (fracción citoplásmica de troponinas), y no regulan la actividad contráctil del tejido muscular cardíaco [7].
Valor diagnóstico y mecanismos para aumentar las troponinas cardíacas séricas
Entre la gran cantidad de biomarcadores propuestos para el diagnóstico de infarto agudo de miocardio, solo las troponinas I y T son los más confiables y demandados en la práctica clínica. Sin embargo, no cumplen completamente con todos los criterios de un biomarcador ideal para el diagnóstico de infarto agudo de miocardio, ya que se elevan relativamente tarde desde el momento del desarrollo de la isquemia miocárdica (síndrome de dolor) y no tienen especificidad absoluta para la detección de necrosis de cardiomiocitos de etiología isquémica. Esta última circunstancia se expresa en el hecho de que los niveles de troponinas I y T también pueden aumentar significativamente en otras lesiones miocárdicas (no isquémicas) que no están relacionadas con infarto agudo de miocardio, lo cual puede conducir a diagnósticos incorrectos [8],[9],[10],[11],[12],[13]. Dada esta circunstancia, una formulación más competente y moderna sobre el valor diagnóstico de troponinas I y T debería ser la siguiente: “troponina I y troponina T son cardiomarcadores específicos para la identificación de cualquier daño a los cardiomiocitos (independientemente de la etiología), pero no pueden considerarse cardiomarcadores específicos para el diagnóstico de ningún tipo particular de daño, incluida la necrosis isquémica de las células miocárdicas en el infarto agudo de miocardio”. Por lo tanto, los médicos en ejercicio no deben confiar solo en el resultado de los métodos de diagnóstico de laboratorio (troponina I positivo y/o troponina T) durante el proceso de diagnóstico terapéutico cuando ingresan pacientes con signos de infarto agudo de miocardio.
Es importante destacar que en las primeras etapas de muchos procesos patológicos que causan daño miocárdico irreversible (infarto agudo de miocardio, miocarditis y otros), o reversible (esfuerzo físico, condiciones de estrés y otros), la dinámica de aumento de las troponinas I y T puede ser casi similar, lo que crea dificultades significativas en el diagnóstico diferencial [12],[14]. Los investigadores aún no han establecido finalmente los mecanismos exactos de daño a los cardiomiocitos en estos casos, pero es probable que la naturaleza de una serie de efectos adversos en muchas patologías sea muy compleja. Por ejemplo, en la inflamación sistémica (sepsis), se ha identificado que las citoquinas circulantes en la sangre causan daño directo a las células del miocardio. Pero además de este tipo de daño, la sepsis aumenta la demanda de oxígeno del miocardio, lo que resulta en isquemia miocárdica en arterias coronarias intactas, que en este caso corresponde a la patogénesis de infarto agudo de miocardio tipo 2 [15].
Cuando se consideran los mecanismos de aumento de troponinas I y T en la insuficiencia renal crónica, también influyen varios factores. Según algunos datos, el aumento de las troponinas en la insuficiencia renal crónica se debe a la disminución en la tasa de eliminación de la sangre a la orina. En pacientes con una tasa reducida de filtración glomerular, el grado de aumento de las troponinas puede ser bastante impresionante y con una tasa reducida de filtración glomerular más baja, los niveles séricos de troponina T aumentan más significativamente [16]. Se ha sugerido que en la insuficiencia renal crónica, un papel importante en el daño a los cardiomiocitos y el aumento de los niveles séricos de troponinas I y T lo juega el efecto negativo directo que causan en las células del miocardio los productos tóxicos de los procesos metabólicos, en particular los productos de metabolismo del nitrógeno. Y, finalmente, se planteó la hipótesis de que en la insuficiencia renal crónica se activa la expresión de troponinas I y T en los músculos esqueléticos, lo cual puede ser otro mecanismo interesante [4],[12],[16].
El daño reversible de las células del miocardio en determinadas condiciones fisiológicas (actividad física durante una carrera prolongada o situaciones estresantes graves y condiciones patológicas, como por ejemplo episodios isquémicos transitorios en la angina de pecho), se caracteriza por una dinámica menos aguda del aumento de los niveles de troponinas I y T. El grado de exceso generalmente no supera entre 5 y 10 veces los valores iniciales. El pequeño grado de aumento de troponinas I y T sugiere que es responsable de esto solo la fracción citoplásmica de troponinas. En tanto, de las concentraciones más altas de troponinas I y T se responsabiliza la fracción estructural de troponinas del aparato contráctil de cardiomiocitos, que se destruye en lesiones miocárdicas irreversibles.
Inmunoensayos de alta sensibilidad: ¿cómo ha cambiado nuestra comprensión de la bioquímica y del valor diagnóstico de las troponinas?
En el contexto de la mejora de los métodos de laboratorio para la determinación y creación de los llamados inmunoensayos de alta sensibilidad (high-sensitive) para la detección de troponina I y troponina T (hs-cTnI y hs-cTnT), las capacidades de diagnóstico y las direcciones prometedoras para futuras investigaciones se han ampliado significativamente [1],[8],[12]. En particular, surgió la posibilidad de determinar concentraciones más bajas de moléculas de troponinas I y T que previamente habían permanecido invisibles para los inmunoensayos moderadamente sensibles.
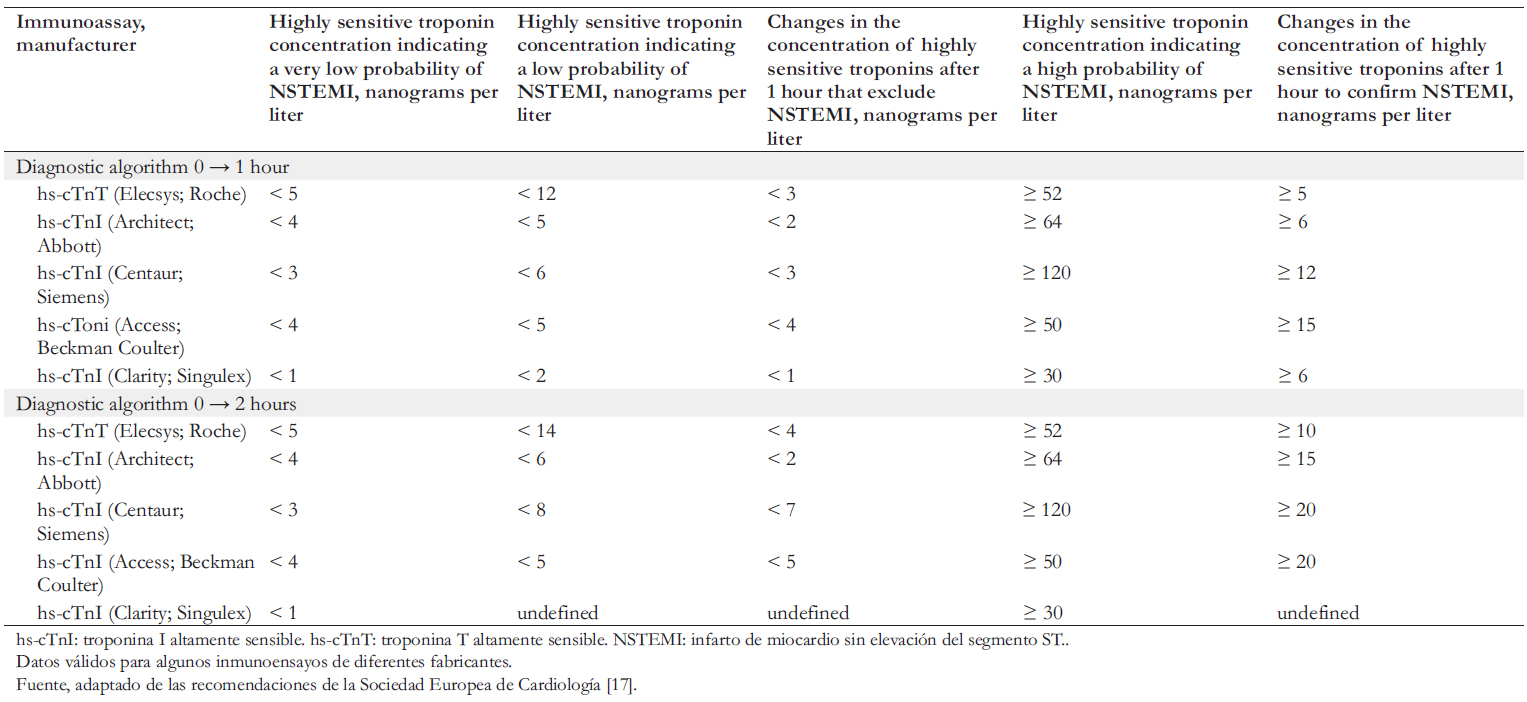
Ello permitió el desarrollo de algoritmos de diagnóstico tempranos para la confirmación/exclusión de infarto agudo de miocardio. Las recomendaciones de la sociedad Europea de Cardiología enfatizan la alta eficiencia en el uso de algoritmos tempranos (0 → 1 h y 0 → 2 h) para excluir y confirmar el infarto de miocardio sin elevación del segmento ST [17]. Estos algoritmos de diagnóstico temprano de infarto de miocardio sin elevación del segmento ST se basan en evaluar los niveles de troponinas cardíacas altamente sensibles en el momento del ingreso y luego volver a determinar la concentración después de una o dos horas. Las concentraciones de umbral de troponinas cardíacas altamente sensibles para la confirmación/ exclusión de infarto de miocardio sin elevación del segmento ST son específicas para los inmunoensayos de diferentes fabricantes (Tabla 1).
Si la concentración de troponinas cardíacas altamente sensibles medida al ingreso es muy baja o baja y no hay un aumento significativo cuando se vuelve a determinar después de una (o dos) horas (Tabla 1), se excluye el diagnóstico de infarto de miocardio sin elevación del segmento ST. En estos casos se recomienda el alta temprana y el tratamiento ambulatorio o de rutina a dichos pacientes. Si en la concentración de troponinas cardíacas altamente sensibles, medida al ingreso por encima de los umbrales o cuando se vuelve a determinar después de una (o dos horas), se observa un aumento significativo, existe una alta probabilidad de diagnóstico de infarto de miocardio sin elevación del segmento ST. A tales pacientes se recomienda la hospitalización y la realización de angiografía coronaria invasiva en caso de emergencia.
 Tamaño completo
Tamaño completo Además, el aumento de la sensibilidad de los métodos de determinación ha permitido detectar concentraciones que se pronostican desfavorables de las troponinas cardíacas de alta sensibilidad I y T en muchas patologías que causan daño a las células del miocardio [12]. El percentil 99 (niveles de troponina sérica que se encuentran en el 99% de las personas completamente sanas), se propuso como el valor de referencia superior para indicar niveles que se pronostican desfavorables.
Los métodos altamente sensibles para la determinación de troponina I y troponina T han alterado varios conceptos nuestros acerca de las características bioquímicas. En particular, se ha demostrado que los niveles séricos de troponinas en pacientes sanos dependen del sexo, la edad y el momento de la toma de biomateriales durante las 24 horas [18],[19],[20],[21],[22]. Sobre la base de esto, se propuso calcular el percentil 99 en función de la influencia de algunos de estos factores. Por lo tanto, el efecto de las características de género en los niveles de troponinas resultó ser muy significativo, lo que se tuvo en cuenta al calcular los valores de 99 percentil en nuevos algoritmos rápidos para el diagnóstico de infarto agudo de miocardio [1],[22],[23]. Se ha sugerido que las características de género de los niveles de troponinas (niveles más altos de troponinas cardíacas de alta sensibilidad I y Ten hombres) se explican por la masa del miocardio ventricular izquierdo, que es mayor en hombres que en mujeres [22]. Se observó el efecto de la edad en los niveles de troponinas cardíacas de alta sensibilidad I y T: en pacientes sanos más jóvenes, los niveles séricos de troponinas son significativamente más bajos que en pacientes mayores. Según los investigadores, las características de troponinas cardíacas de alta sensibilidad I y T asociadas con la edad, están relacionadas con la presencia en pacientes ancianos de algunas patologías comórbidas crónicas (latentes) que pueden afectar negativamente a las células del miocardio y promover una mayor liberación de las moléculas troponinas I y T de estas células [23],[24].
Y, por último, son muy interesantes los informes de los investigadores sobre la existencia de ritmos circadianos de troponinas cardíacas de alta sensibilidad I y T, es decir, la dependencia de la concentración de estos en el momento de la toma de muestras de suero de los pacientes. Por lo tanto, se ha demostrado que los niveles séricos de troponinas cardíacas de alta sensibilidad I y T en los mismos pacientes son significativamente más altos en la mañana en comparación con los valores vespertinos [18]. Además, esta tendencia es característica tanto para pacientes sanos [18] como para pacientes con insuficiencia renal crónica [25].
Los mecanismos específicos de formación de los ritmos circadianos de troponinas cardíacas de alta sensibilidad I y T no se conocen de manera concluyente, pero existen especulaciones sobre su asociación con los ritmos circadianos de otros sistemas que pueden tener ciertos efectos negativos en las células del miocardio. Por ejemplo, por la mañana, los sistemas simpáticos y renina-angiotensina-aldosterona tienen la actividad máxima, lo que provoca aumento en la carga del tejido muscular cardíaco, aumento en la frecuencia cardíaca y la presión arterial. Los mecanismos de impacto de estos factores en el miocardio son algo similares a los mecanismos de acción que ocurren durante el ejercicio y el estrés, que se acompañan del aumento de troponinas cardíacas de alta sensibilidad I y T. Se cree que el aumento de la actividad de estos sistemas en el período matutino del día se formó durante el desarrollo evolutivo para garantizar un período normal de vigilia. Sin embargo, estos sistemas desempeñan funciones clave en la patogénesis de enfermedades cardiovasculares, incluida el infarto agudo de miocardio. En consecuencia, pueden tener un efecto negativo adicional en el miocardio de aquellos pacientes que tienen ciertos factores de riesgo de enfermedades cardiovasculares (aterosclerosis, dislipidemia, trastornos hemostáticos y otros) [26].
Vale la pena señalar que la influencia de la edad y la hora del día en los niveles de troponinas cardíacas de alta sensibilidad I y T es discutible, debido a la falta de estudio y la presencia de resultados de investigación contradictorios. Por lo tanto, en los algoritmos de diagnóstico rápidos modernos de infarto agudo de miocardio, la influencia de estos factores aún no se tiene en cuenta. Por ejemplo, el estudio de van der Linden [25] informó sobre el efecto pronunciado de los ritmos circadianos de troponina T cardíaca de alta sensibilidad en el diagnóstico temprano del infarto de miocardio; mientras que, según otro estudio de Klinkenberg [18], los ritmos circadianos de troponina T cardíaca de alta sensibilidad no tienen efecto significativo sobre los algoritmos de diagnóstico precoz del infarto agudo de miocardio. Al analizar el diseño de estos dos estudios, contradictorios en cuanto a la importancia clínica de los ritmos circadianos de troponina T cardíaca de alta sensibilidad, se pueden observar algunas diferencias en las características clínicas de los pacientes. En particular, el grado de fluctuaciones diurnas en los niveles de troponina T cardíaca de alta sensibilidad en el estudio de van der Linden parece haber sido influenciado por una enfermedad concomitante, la insuficiencia renal crónica.
Posibilidades de investigación de troponinas cardíacas en fluidos corporales producidos de manera no invasiva
El principal fluido biológico para determinar los niveles de troponina es la sangre. Sin embargo, con el advenimiento de métodos altamente sensibles, se hizo posible determinar troponinas en otros fluidos biológicos que se pueden obtener de forma no invasiva, lo cual es otra ventaja importante y prometedora. La obtención de este biomaterial de los pacientes es atraumática e indolora, reduce el riesgo de desarrollo de infecciones de transmisión sanguínea (virus de la inmunodeficiencia humana, hepatitis viral, entre otros). Tampoco requiere personal médico capacitado y el propio paciente puede tomar su biomaterial en su domicilio. Por ejemplo, las concentraciones de troponinas en la orina son bastante pequeñas y no son detectadas por sistemas de prueba moderadamente sensibles, mientras que al utilizar el método de investigación altamente sensible, se detectó en la orina de la mañana de todos los individuos investigados. Asimismo, en la orina de los pacientes con hipertensión los niveles de troponina T cardíaca de alta sensibilidad fueron significativamente más altos que en pacientes con presión arterial normal [27],[28].
El líquido oral es otro biomaterial no invasivo prometedor para el diagnóstico de muchas enfermedades endocrinas, oncológicas y cardiovasculares, incluido el infarto agudo de miocardio [29],[30],[31],[32]. Así, en nuestro estudio piloto unicéntrico, se demostró recientemente que la concentración de troponina I cardíaca de alta sensibilidad en el líquido oral en pacientes con infarto agudo de miocardio es significativamente mayor que en el grupo de control de pacientes. Además, los niveles de troponina I cardíaca de alta sensibilidad en el suero sanguíneo y el líquido oral tienen una correlación moderada [31]. Se planean más estudios sobre muestras de pacientes más grandes para establecer valores de referencia y estandarizar la etapa preanalítica para aumentar el valor clínico y diagnóstico de troponina I cardíaca de alta sensibilidad en el líquido oral.
Métodos de determinación de troponinas cardíacas: una breve historia del desarrollo de inmunoensayos de troponina
La determinación de troponinas en la sangre se lleva a cabo utilizando varios métodos inmunoquímicos diferentes (radioinmunoensayo, inmunoensayo enzimático, análisis de inmunofluorescencia e inmunoquimioluminiscencia), cuyo principio fundamental incluye varias etapas sucesivas: la inmunológica, la química, la de detección.
En la primera etapa (inmunológica) se produce interacción específica de los anticuerpos de diagnóstico de un kit comercial con un antígeno, que en este caso es la troponina. En la segunda y tercera etapas o se produce una reacción inmunológica adicional de anticuerpos y la formación de un complejo tipo sándwich, o una reacción química (enzimática) y el registro de la señal recibida. Los métodos de detección de señales también difieren según el marcador de anticuerpos utilizado: en el caso de un inmunoensayo enzimático, se evalúa la intensidad del color utilizando un fotómetro/espectrofotómetro. En el caso del radioinmunoensayo, en que se usan como marca radioisótopos (radionúclidos), se evalúa con un radiómetro (radio espectrómetro), y en el caso de usar fluoróforos la señal se registra en un fluorómetro. El nivel (fuerza) de la señal desarrollada es directamente proporcional a la concentración de troponinas en la muestra biológica. El resultado se expresa con mayor frecuencia en valores cuantitativos (nanogramos por mililitro, nanogramos por litro, microgramos por litro), o se lleva a cabo es una evaluación visual del número de tiras formadas, lo cual es típico de los métodos cualitativos (tiras de prueba de diagnóstico) utilizado al lado de la cama del paciente.
La necesidad de crear ensayos inmunoquímicos específicos para la determinación de troponina I y troponina T para el diagnóstico de infarto agudo de miocardio surgió hace mucho tiempo. Los primeros métodos (inmunoensayos de primera generación) se crearon hace más de 35 años y, a medida que avanzaban los trabajos, sus características analíticas mejoraron. En 1987, Cummins informó de la creación del primer método para determinar troponina I. Este método tenía una concentración mínima determinable extremadamente grande (alrededor de 10 microgramos por litro o 10 000 nanogramos por litro). Pero, el grado de este aumento de troponinas se observó solo en infarto agudo de miocardio de gran escala y en fechas tardías desde el momento del ingreso del paciente. Por lo tanto, dicho inmunoensayo no era adecuado para la medicina práctica y era significativamente inferior al valor diagnóstico de la creatina cinasa MB, que en aquel momento se consideraba generalmente el estándar de oro para el diagnóstico de infarto agudo de miocardio [33]. En los años siguientes, un equipo de investigación dirigido por Katus informó sobre la creación de un ensayo inmunoenzimático para determinar troponina T. La concentración mínima detectable en este método fue de 100 nanogramos por litro, y el tiempo de prueba de laboratorio tomó 90 minutos [34]. Según un estudio que utilizó este inmunoensayo, los niveles de troponina T se correlacionaron estrechamente con la actividad de la enzima creatina cinasa MB en el suero sanguíneo. Aunque este inmunoensayo era superior en su valor diagnóstico a otros biomarcadores de infarto agudo de miocardio (aspartato aminotransferasa, lactato deshidrogenasa y creatina cinasa MB), tenía un inconveniente muy importante: la presencia de un gran número de interacciones cruzadas (no específicas o falsas positivas) de anticuerpos diagnósticos con troponinas esqueléticas, lo que dio lugar a resultados falsos positivos frecuentes en el daño y/o enfermedades del músculo esquelético.
En los métodos de determinación de troponinas de segunda generación, la especificidad aumentó y el número de falsos positivos disminuyó. La mejora adicional en los métodos de determinación de troponinas cardíacas dio como resultado inmunoensayos de tercera y cuarta generación que carecían casi por completo de respuestas no específicas, y se redujo la concentración mínima definida. Esto condujo al diagnóstico más temprano de infarto agudo de miocardio, dentro de las 6 a 8 horas desde el momento en que los pacientes ingresaron con quejas de dolor en el pecho. Por lo tanto, la troponina I y troponina T se convirtieron en el nuevo estándar de oro en el diagnóstico de infarto agudo de miocardio, que finalmente fue documentado en 2000 por los principales expertos de las comunidades cardiológicas europeas y estadounidenses [35].
Sin embargo, el tiempo requerido para la confirmación de laboratorio de la necrosis isquémica de cardiomiocitos siguió siendo relativamente grande y no fue adecuado para el diagnóstico temprano de infarto agudo de miocardio. Por esta razón, se continuó el trabajo adicional para encontrar nuevos biomarcadores y mejorar la sensibilidad de los métodos de determinación de troponinas [36]. Así, entre 2007 y 2010, surgieron los primeros datos sobre métodos altamente sensibles para la determinación de troponinas (troponinas cardíacas de alta sensibilidad I y T), también llamados inmunoensayos de quinta generación. La concentración mínima detectable de los datos de los métodos inmunoquímicos fue de solo de 1 a 10 nanogramos por litro, decenas y cientos de veces menos que algunos de los métodos moderadamente sensibles utilizados hasta ese momento, y miles de veces más que los primeros prototipos creados hacen más de 35 años. El tiempo empleado en el estudio de laboratorio con inmunoensayos altamente sensibles fue solo entre 20 y 30 minutos [37].
Actualmente hay una gran cantidad de inmunoensayos de diagnóstico en el mercado, diseñados para detectar troponina I y troponina T. Todos ellos difieren en sus características analíticas, y los resultados de laboratorio obtenidos al usar el mismo suero por diferentes métodos no coinciden. El problema de estandarizar diferentes métodos para definir la troponina I y troponina T es esencial [38]. Por ejemplo, si un paciente necesita ser trasladado a otro hospital que utiliza un método diferente para determinar la troponina, entonces los resultados no pueden compararse para identificar la cinética de elevación característica de infarto agudo de miocardio. En este caso es necesario realizar estudios repetidos, lo que requiere tiempo y dineros adicionales.
La Federación Internacional de Química Clínica realiza una evaluación de expertos independientes y sistematiza los datos sobre los métodos de determinación de troponinas cardíacas. De acuerdo con los datos de la Federación Internacional de Química Clínica, los inmunoensayos altamente sensibles más confiables y de alta calidad son producidos por las siguientes compañías: Roche Diagnostics, Abbot, Beckman Coulter, Ortho, Siemens, Singulex, bioMerieux, LSI Medience. Roche Diagnostics fabrica kits para la determinación de troponina T cardíaca de alta sensibilidad únicamente, mientras que las otras empresas enumeradas anteriormente fabrican kits de diagnóstico para determinar troponina I cardíaca de alta sensibilidad, por lo que el problema de estandarización se refiere principalmente a esta última.
Los resultados de troponina I cardíaca de alta sensibilidad en el mismo paciente, obtenidos por métodos altamente sensibles de diferentes fabricantes, pueden diferir varias veces. Una de las principales razones de los resultados no coincidentes es que los distintos fabricantes en sus kits utilizan diferentes anticuerpos de diagnóstico que se dirigen a diferentes epítopos de las moléculas troponina I y troponina T. En el infarto agudo de miocardio, un gran número de fragmentos de moléculas de troponina circulan en el suero de los pacientes, que tienen diferente estabilidad, vida media y duración de eliminación. Cuando se usan anticuerpos contra epítopos inestables de moléculas de troponina, el resultado de laboratorio puede subestimarse, mientras que cuando se usan anticuerpos contra epítopos más estables, el resultado puede sobreestimarse. Los procesos de descomposición y eliminación de troponinas son poco estudiados, pero es probable que ocurran continuamente y puedan depender de una serie de factores, incluso de la prescripción de medicamentos. Además, algunos epítopos antigénicos de las moléculas troponina I y troponina T son objetivos de autoanticuerpos y anticuerpos heterófilos que causan resultados de laboratorio falsos positivos y falsos negativos. El estudio de los procesos de descomposición y eliminación de las moléculas de troponinas, así como la influencia de los autoanticuerpos y los anticuerpos heterófilos, es el tema de investigaciones adicionales destinadas a mejorar la calidad de los inmunoensayos de troponina.
Hasta la fecha, muchas instituciones de salud han pasado al uso de sistemas de prueba de troponina altamente sensibles. Anand y colegas realizaron recientemente un estudio global para evaluar la implementación de las recomendaciones clave de la Definición Universal de Infarto de Miocardio (2018) sobre el uso de troponinas altamente sensibles, utilizando un cuestionario telefónico de formato especialmente diseñado. Los autores entrevistaron a médicos en 1902 centros médicos en 23 países de los cinco continentes. La troponina cardíaca se utilizó como marcador diagnóstico principal para diagnosticar infarto agudo de miocardio en 96% de los centros; el uso de creatina cinasa MB continúa se usó en algunos países de América Latina (Argentina, México). Solo 41% de los centros utilizaron ensayos de alta sensibilidad, con una amplitud desde 7% en América del Norte hasta 60% en Europa. En las instituciones que utilizaron métodos de análisis altamente sensibles, se utilizó con más frecuencia la estrategia de medición en serie con predominio de vías de diagnóstico aceleradas (de 0 a 3 horas), tomándose en cuenta con mayor frecuencia el umbral de diagnóstico del percentil 99. Sin embargo, solo 18% de los centros utilizaron los umbrales del percentil 99 asociados con las características de sexo/género [39].
Métodos altamente sensibles para la determinación de troponinas: sus características analíticas, criterios, clasificación
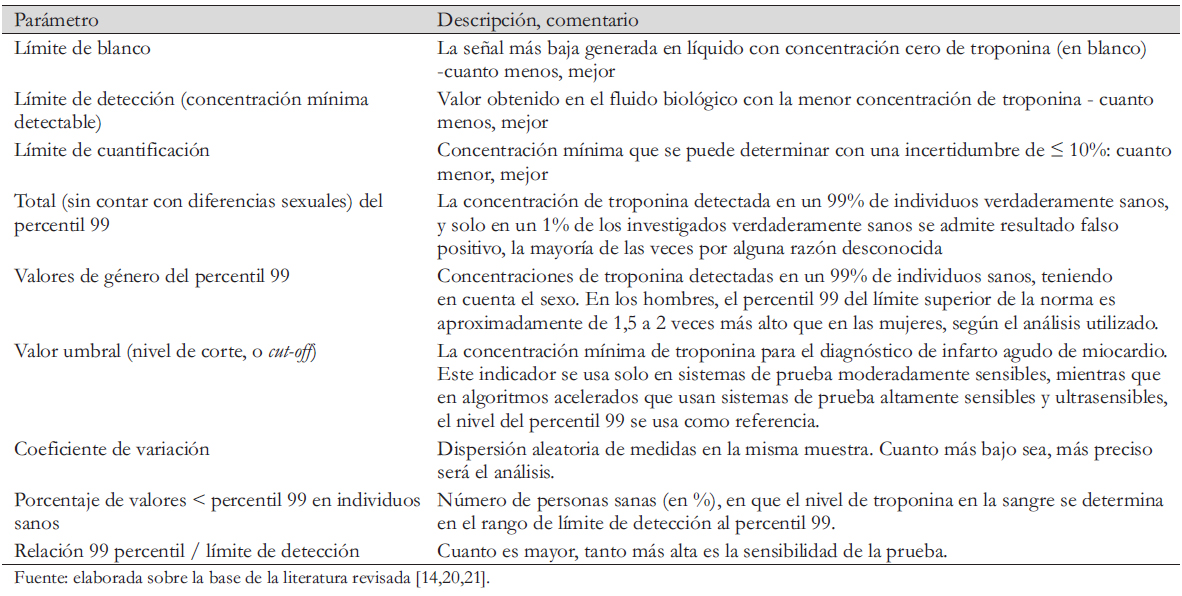
Las principales características analíticas de la calidad de los inmunoensayos de troponina son: límite de blanco ─ la concentración máxima del analito que se puede detectar en una muestra que no lo contiene; límite de detección ─ la concentración mínima detectable); límite de cuantificación (límite de determinación cuantitativa); percentil 99; características de género del percentil 99; porcentaje de valores medibles en individuos sanos; coeficiente de variación y relación de 99 percentil/límite de detección (Tabla 2) [21],[40],[41].
Muchos investigadores tienen una inquietud. ¿Qué análisis debería calificarse como altamente sensible? El Grupo de Trabajo de la Federación Internacional de Química Clínica del Comité de Aplicación Clínica de Biomarcadores Cardíacos ha propuesto que sea designado como altamente sensible un método que cumpla dos criterios [21]. Primero, el porcentaje de coeficiente de variación al establecerse los valores del percentil 99, no debe exceder al 10%. En segundo lugar, en más del 50% de las personas sanas, la concentración de troponinas debería ser superior al límite de detección del método analítico. Sin embargo, muchos de los métodos designados como altamente sensibles no se ajustan a estos criterios. Para los ensayos altamente sensibles, todas las revistas, fabricantes, laboratorios e instituciones deben utilizar la unidad de medición nanogramos por litro para evitar confusiones, y puntos decimales seguidos de ceros innecesarios utilizados en análisis moderadamente sensibles y algunos análisis modernos de alta sensibilidad [21].
El valor clínico y diagnóstico de los resultados de la determinación de troponinas cardíacas de alta sensibilidad T e I está directamente relacionado con las características analíticas de los diagnósticos de troponina utilizados (Tabla 2). Para establecer los parámetros analíticos del sistema de prueba, se deben seguir las recomendaciones de los expertos de la Federación Internacional de Química Clínica. Entonces, por ejemplo, para establecer los valores del percentil 99 de acuerdo con el género, es necesario determinar la troponina en al menos 300 mujeres y 300 hombres.
 Tamaño completo
Tamaño completo Posteriormente, se pueden ajustar cuando se reciban nuevos datos. Idealmente, cada laboratorio debe establecer su propio percentil 99, que en este caso corresponderá no solo al sistema de prueba y al analizador utilizado, sino también a las características de la población dada. Sin embargo, dada la complejidad y el costo de tales estudios, es admisible centrarse en los parámetros proporcionados por los fabricantes [21],[42].
Establecer valores óptimos para el percentil 99 es muy importante e implica una serie de preguntas clave: ¿cómo se deben seleccionar los grupos de referencia? ¿Qué método de cálculo estadístico debería aplicarse? La definición de lo que constituye una persona sana es un tema para discutir [21]. ¿Cómo se deben seleccionar los pacientes por edad: jóvenes (inferior a 30 años) o aquellos que coinciden con los pacientes con infarto agudo de miocardio clásico (de 40 a 90 años)? ¿Qué criterios deben utilizarse para designar a los pacientes "sanos", utilizando una encuesta simple (cuestionario) o un examen médico completo, que incluya estudios tanto físicos como instrumentales de laboratorio (electrocardiografía, ecocardiografía, determinación de la concentración de péptidos natriuréticos, nivel de creatinina)? La última opción es ideal, pero cara.
La selección del grupo de control de acuerdo con criterios estrictos desplaza el percentil 99 a valores más bajos [21],[42],[43]. Además, al calcular el percentil 99, es necesario un enfoque estadístico unificado. Los cálculos propuestos, el método no paramétrico (método de Harrell-Davis) y el método de estadística robusta (estable), dan diferentes valores del percentil 99. Las discusiones sobre este tema continúan [42],[43]. Así, las condiciones anteriormente señaladas tienen una fuerte influencia sobre el establecimiento del nivel del percentil 99, lo cual viene siendo una de las explicaciones de su significativa variación entre los métodos de análisis de diferentes fabricantes.
Al mismo tiempo, algunos algoritmos nuevos de diagnóstico rápido (de una y dos horas) no se centran en el nivel del percentil 99 como umbral de diagnóstico de referencia, sino que utilizan valores de corte más bajos para tomar decisiones sobre hospitalización/intervenciones invasivas, o de enviar al paciente a casa. Esto se debe a que muchos pacientes con concentraciones de troponina cardíaca de alta sensibilidad que van desde el límite de detección (o límite de cuantificación) al percentil 99, tienen un mayor riesgo de resultados adversos en comparación con aquellos con valores mínimos o no detectables (es decir, inferior al límite de detección o límite de cuantificación). El éxito de estas estrategias se ha demostrado en varios estudios para excluir rápidamente el síndrome coronario agudo e identificar a los pacientes con elevado riesgo de eventos cardiovasculares adversos a los 30 días [44],[45],[46],[47],[48].
Muy importante en el diagnóstico temprano de infarto agudo de miocardio es límite de detección. Por ejemplo, el método de inmunoensayo de primera y segunda generación tuvo un límite de detección en el rango de 100 a 500 nanogramos por litro, debido a que el infarto agudo de miocardio se diagnosticó demasiado tarde (después de 12 a 24 horas). En algunos casos, se pasaron por alto infartos de foco pequeño y no se detectó troponina en ningún paciente sano (0% de los valores medidos en la población de referencia).
En la etapa actual de desarrollo de análisis altamente sensibles, el límite de detección puede ser solo de unos pocos nanogramos por litro e incluso inferior a 1 nanogramo por litro, lo que es cientos de veces más sensible y permite detectar daño miocárdico casi a nivel de células individuales. El porcentaje de valores medidos de troponinas oscila entre 50 y 100% [21]. A GarcíaOsuna y colaboradores recientemente estudiaron las características analíticas del nuevo método que detecta la troponina I a nivel de moléculas individuales. El estudio mostró que este método es aproximadamente 10 veces más sensible que el método de troponina I cardíaca de alta sensibilidad que se utiliza actualmente. El límite de detección de este método fue de 0,08 a 0,12 nanogramos por litro, y la proporción de personas sanas con concentraciones de troponina medibles alcanzó el 99,5%. Al mismo tiempo, los sujetos sanos fueron seleccionados de manera muy rígida (sobre la base de su anamnesis, niveles normales de péptidos natriuréticos y creatinina). La mediana de troponina I cardíaca de alta sensibilidad fue significativamente mayor en los hombres en comparación con las mujeres y en los ancianos en comparación con los jóvenes, lo que indica la necesidad de reflejar las características relacionadas con la edad en los niveles de troponina I cardíaca de alta sensibilidad. Este inmunoensayo hipersensible es significativamente superior a otros métodos altamente sensibles existentes [49]. Esta sensibilidad se logró mediante el uso de cuatro tipos de anticuerpos: dos de ellos están dirigidos a epítopos ubicados en el centro de la troponina y dos a epítopos ubicados en ambos extremos de la molécula. Ello proporciona una mayor captación de la molécula de troponina I y sus fragmentos en comparación con los sistemas de prueba basados en el uso de dos o tres tipos de anticuerpos.
El parámetro importante que determina la precisión del inmunoensayo es el coeficiente de variación. El método se considera altamente preciso y cumple los requisitos de la Federación Internacional de Química Clínica, si al determinar en serie el nivel de troponina en la misma muestra, la dispersión media de los resultados obtenidos no supera el 10% (coeficiente de variación menor o igual a 10%).
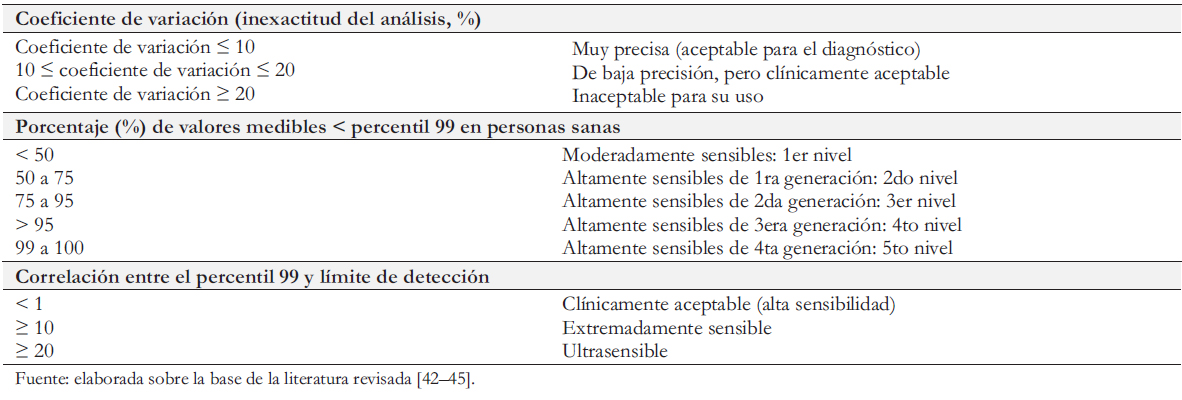
Sin embargo, debido a la escasa disponibilidad comercial de pruebas de alta precisión, todavía se utilizan ampliamente en muchos laboratorios las pruebas de troponina con un coeficiente de variación entre un 10% y un 20%. El uso de estos sistemas de prueba puede dar lugar a resultados falsos positivos y falsos negativos. Las pruebas con coeficiente de variación superior a 20% son inaceptables para uso clínico y deben excluirse (Tabla 3)[50].[Una mejora significativa en los parámetros analíticos de las pruebas altamente sensibles hizo posible introducir una clasificación adicional de métodos denominada "funcional" basada en la relación entre el percentil 99 y el límite de detección. Cuanto mayor es la correlación percentil 99/límite de detección, mayor es la probabilidad de identificar sujetos con valores medibles.
En la Tabla 4 se resumen algunos de los sistemas de prueba modernos altamente sensibles disponibles para uso clínico, así como sus parámetros analíticos (según datos de Federación Internacional de Química Clínica, 2020) [50].
 Tamaño completo
Tamaño completo 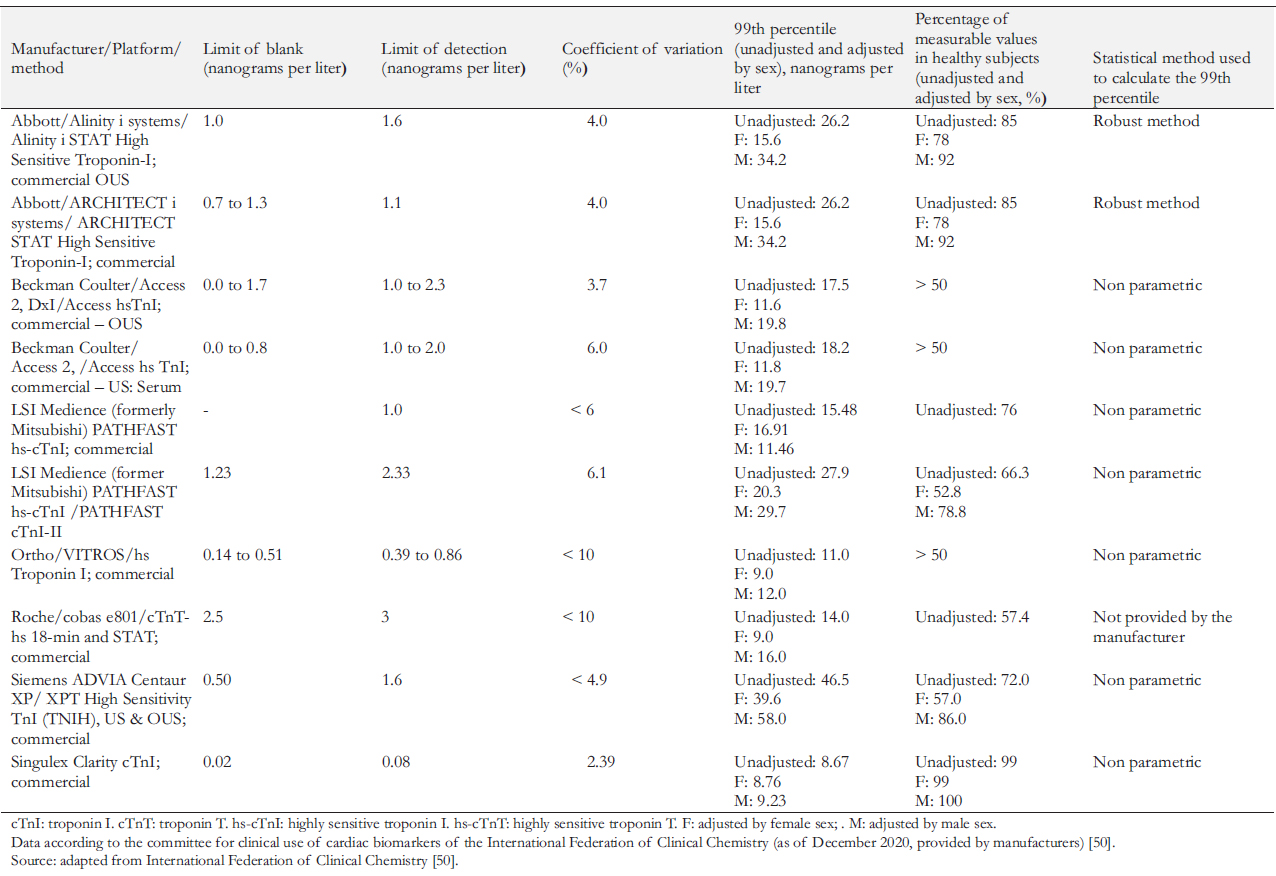 Tamaño completo
Tamaño completo Conclusión
Los métodos de laboratorio para la detección de troponinas cardíacas siguen siendo una herramienta de diagnóstico importante, que se mejora cambiando continuamente nuestras ideas sobre la bioquímica de las moléculas de troponinas cardíacas. Además, abren nuevas posibilidades de su uso en el diagnóstico de laboratorio.
Las troponinas cardíacas son un indicador específico de cualquier daño al miocardio, independientemente de la etiología. En el futuro se pueden usar no solo en cardiología, sino también en otras áreas de la medicina.
Para el uso óptimo y efectivo de las troponinas cardíacas en el diagnóstico, es importante comprender que el resultado de su estudio depende estrechamente de los métodos de su determinación y sus principales características analíticas, como el percentil 99 común y el percentil 99 (por género), el límite en blanco, la concentración mínima definida, el coeficiente de variación y otros.
También es necesario continuar el trabajo para estudiar los mecanismos y los efectos de la edad y la hora del día, en los niveles de troponinas altamente sensibles. Además, se deben evaluar nuevas oportunidades prometedoras para investigar las moléculas de troponinas cardíacas en fluidos corporales no invasivos.
Notas
Autoría
AMCh: conceptualización, metodología, software, validación, análisis formal, investigación, recursos, curaduría de datos, escritura, primera redacción, revisión, edición.
Conflictos de intereses
El autor completó la declaración de conflictos de interés de ICMJE y declaró que no recibió fondos por la realización de este artículo; no tiene relaciones financieras con organizaciones que puedan tener interés en el artículo publicado en los últimos tres años y no tiene otras relaciones o actividades que puedan influenciar en la publicación del artículo. El formulario se puede solicitar contactando al autor responsable o al Comité Editorial de la Revista.
Financiamiento
El presente trabajo no recibió financiamiento para la elaboración del manuscrito.
Aspectos éticos
El presente artículo se exime de la evaluación por un comité de ética, debido al diseño del estudio, que corresponde a una revisión de la literatura (estudio en fuentes secundarias de literatura disponible).
Declaración de acceso a datos
Disponibilidad de entrega de datos a solicitud.
Origen y arbitraje
No solicitado. Con revisión por pares externa, por tres árbitros a doble ciego.
Idioma del envío
Español.

