Revisión clínica
← vista completaPublicado el 1 de marzo de 2011 | http://doi.org/10.5867/medwave.2011.03.4949
Actualización en el manejo de hepatitis B
An update in the management of hepatitis B
Resumen
La primera descripción de lo que se llamó el antígeno de superficie (HBsAg) data del año 1965. Han pasado prácticamente 45 años desde que se descubrió en Australia en un aborigen y de ahí en adelante comienza una escalada de investigación básica y clínica, que permite en la actualidad encasillar la enfermedad como una enfermedad viral, que tiene a su vez varios genotipos.
Hoy en día se describen 9 genotipos virales, de la A a la I. El último aparecido el año 2010. El genoma marca la diferencia, habiendo más de 3.000 nucleótidos que permiten hacer genotipos distintos cuando hay más de 5 a 7% de diferencia. No se conoce en detalle cuál es la relevancia de estos genotipos, pero sí se conoce que el genotipo C tiene mayor gravedad, determinando mayor riesgo de progresión hacia cirrosis y hepatocarcinoma que los genotipos A y B, los cuales tienen una mejor respuesta al interferón (antiviral), lo cual a futuro podría tener cierto impacto en las decisiones de tratamiento.
Desarrollo
Distribución de la enfermedad
La distribución de la hepatitis B en el mundo es variable. En Asia predominan los genotipos B y C. En estos países la infección se adquiere fundamentalmente en la niñez por transmisión vertical, por ende, los niños pueden quedar con el virus por el resto de su vida y tienen una alta tasa de cronicidad. La respuesta a interferón, especialmente del genotipo C, no es buena y tiene una alta tasa de transformación a hepatocarcinoma.
En los países en los cuales las tasas de hepatitis B son bajas, como Europa, Estados Unidos, algunos países de Sudamérica (Argentina y Chile), los genotipos más frecuentemente identificados son A, D, F y G. En Chile el genotipo más frecuente es el F, habitualmente por transmisión horizontal (siendo adultos), por lo tanto las tasas de cronicidad son más leves, pues el individuo es inmunocompetente. La cronicidad después de una infección aguda en un adulto inmunocompetente se acerca al 3–4% de los casos. Las tasas de respuesta a interferón en aquellos países con más genotipo A son mejores y la transformación a hepatocarcinoma es menor, dado que hay menos portadores.
Vía de inoculación
Las vías de transmisión son la vertical y la horizontal. Es importante tener en cuenta la vía de inoculación aguja-transfusión y la vía laboral. Cabe destacar que cuando se está realizando algún procedimiento de endoscopía y se punciona con una aguja de algún enfermo que tiene hepatitis B activa, el riesgo de contraer la infección con una punción o un corte infectado se aproxima al 30%. Esto va a depender de la carga viral del paciente. En aquellos con altas cargas virales y HBeAg positivo el riesgo de infección puede llegar a ser entre un 50 y un 60%. En aquellos con HBeAg negativo y bajas cargas virales, el riesgo de contagio de hepatitis B es mucho menor, alrededor de un 10-20%. La acción inmediata debe ser verificar si la persona que se accidentó está vacunada o no; si hay adecuados títulos de anticuerpo (Anti-HBsAg > 10 U/L) otorga una alta protección. Si no lo está, se debe vacunar inmediatamente y proteger con gammaglobulina en las siguientes 24 horas, lo que le dará una protección sobre el 75%. Esta conducta debe ser aplicada por cualquier gastroenterólogo o internista en cualquier parte de Chile.
Cuando se comparan los riesgos, el virus B es de alta transmisibilidad. El riesgo de transmisibilidad de hepatitis C con una punción es10 veces menos (3%) y para el virus VIH con una aguja 100 veces menos que el virus B (0,3%).
Riesgo transfusional
En la literatura se ha demostrado que al realizar tamizaje regularmente en los donantes de banco de sangre con HBsAg y anticore total, el riesgo de transmisión de hepatitis B mediante trasfusiones de sangre es tan bajo como 1 en 60.000. Este riesgo puede explicarse porque el donante se pudo haber encontrado en un periodo de ventana o con cargas virales muy bajas. Para hepatitis C el riesgo de trasmisión mediante trasfusión de sangre es de1 en 100.000 y para VIH de 1 en 100.000 gracias al tamizaje con anticuerpos específicos. En Chile los bancos de sangre sólo realizan tamizaje con antígeno de superficie (HBsAg), teniendo en cuenta que es un país baja prevalencia de enfermedad, por lo que la mayoría de los especialistas en salud pública consideran que es una medida razonable y suficiente.
En países con altas tasas de hepatitis B, es recomendable utilizar ambos métodos (anticore y antígeno de superficie) para tamizar la sangre, porque hay muchos pacientes que tienen antígenos de superficie negativo y anticore total positivo (infección oculta) que pueden transmitir la enfermedad vía trasfusiones.
Evolución de la enfermedad
La evolución e historia natural de la enfermedad es bien conocida por múltiples estudios en los últimos años. Si ésta se hace crónica, lo que es más frecuente cuando la infección se adquiere siendo niños, el riesgo de progresión hacia cirrosis es de alrededor de 1 de cada 3 casos. Una vez que existe cirrosis por hepatitis B (o incluso sin haber cirrosis), el riesgo hepatocarcinoma es real (3-4% por año de riesgo de hepatocarcinoma en el caso de cirróticos) y se sabe que una vez que se diagnostica cirrosis alrededor del 25% en los siguientes 5 años se descompensará (ascitis, hemorragia, encefalopatía), requiriendo eventualmente del trasplante hepático o fallecerá.
El virus B es la sexta causa de trasplante hepático en el mundo al analizar las etiologías. El estudio REVEAL (1) en el que se incluyeron más de 3.500 pacientes de Taiwán y corresponde a 40.000 años/persona de seguimiento, demostró que la carga viral era el principal factor de riesgo de evolución a cirrosis y hepatocarcinoma. Aquellos pacientes que tenían más de 1.000.000 de copias, tenían 15% de riesgo de hepatocarcinoma en los siguientes 7-11 años de seguimiento y 35% de riesgo de cirrosis. En aquellos con cargas virales bajas, el riesgo de hepatocarcinoma y cirrosis era mucho menor independiente de la presencia del antígeno “E” y de los niveles de transaminasas.
Hay una gradiente de riesgo de hepatocarcinoma y cirrosis: desde cargas virales muy bajas, bajo 9.999 copias por ml, con 3% de riesgo a 13 años de presentar un hepatocarcinoma, a cargas virales mayores con el consiguiente mayor riesgo de hepatocarcinoma y cirrosis (2). Esto ha hecho que la carga viral sea uno de los exámenes más relevantes al momento de definir el tratamiento del paciente con hepatitis B.
Estos hallazgos también se ven reforzados en el estudio de Liaw y cols. (3), también de Taiwán, con terapia con lamivudina y seguimiento a largo plazo. En este estudio clínico aleatorizado, en un grupo de 600 pacientes con hepatitis B y fibrosis avanzada o cirrosis seguidos durante un promedio de 32 meses, se evaluó la evolución clínica con tratamiento con lamivudina v/s placebo, con una aleatorización 2 a 1. Los pacientes eran fundamentalmente asiáticos y hombres. En la rama de placebo, el riesgo de progresión de la enfermedad hepática hacia una complicación (ascitis, peritonitis, muerte o hemorragia) fue alrededor del 20%, mientras que con lamivudina durante esos 3 años, el riesgo bajó prácticamente a la mitad. Así mismo el riesgo de hepatocarcinoma de alrededor de 10% a 3 años en la rama placebo, fue de sólo 4% en el grupo tratado con lamivudina.
Algunos pacientes pueden desarrollar cepas mutantes resistentes a lamivudina, hecho que hoy en día se ha resuelto con el uso de nuevos y potentes antivirales. En el estudio de Liaw y cols. (3) se evidenció que el grupo que desarrollaba la mutación YMDD tuvo mayor riesgo de evolución hacia cirrosis, comparado con los que no desarrollaban cepas mutantes.
En el mundo hay alrededor de 400 millones de personas con infección crónica por virus de hepatitis B; la mayoría (80%) viven en Oriente y en África subsahariana. De esos pacientes, es probable que una cuarta parte fallezca por alguna de las complicaciones de la enfermedad hepática, estimándose en un millón de muertes al año.
Epidemiología
Chile es un país de baja endemia de hepatitis B, al igual que Europa, Estados Unidos y Canadá. La infección ocurre fundamentalmente en adultos y la vía de transmisión habitual es sexual y percutánea.
En América Latina, Chile se encuentra en una situación privilegiada, pues todos los trabajos publicados demuestran, en población general, tasas menores a 0,2-0,3%. Sin embargo, dentro de América Latina hay zonas como las amazónicas (Norte de Perú, Norte de Brasil y algunas zonas ecuatorianas) en donde hasta el 8% de la población tiene hepatitis B crónica.
Según la notificación del Ministerio de Salud de Chile hay un aumento sostenido en los últimos 5 a 6 años de la cantidad de casos anuales de hepatitis B, de 200 casos a 354 casos por año en 2008, aunque la tasa de hepatitis B aguda sigue siendo bastante baja (2 por 100.000 habitantes). Sin embargo, hay preocupación por algunas zonas en el norte y en el sur, en las cuales se especula que el frío o calor extremo podrían generar conductas de mayor riesgo. Este es un tema que se debe analizar e intentar implementar medidas que disminuyan esta infección.
Los estudios en población de Banco de Sangre en Chile (población seleccionada y de bajo riesgo por encuestas previas a la donación) arrojan una tasa aproximada de prevalencia de 0,02%, considerada baja respecto de otros países del mundo.
En población general, según un estudio de Brahm y cols (6) la tasa de prevalencia de hepatitis B es de 0,3%; en personal de salud en que aumenta el riesgo, es de alrededor de 0,6%; en prostitutas, 2%; en pacientes con VIH, alrededor de 6%; y en pacientes hemodializados crónicos, hasta un 9%.
Es importante reconocer que la infección por hepatitis B está subnotificada por diferentes motivos. Se debe recordar la necesidad y la urgencia de notificar esta enfermedad, pues es la única forma de saber cuán relevante es la enfermedad. La información para notificar se encuentra en la página web de epidemiología, del ministerio de salud.
Según un estudio colaborativo de varios centros en Chile con más de 3300 cirróticos, sólo el 1% de ellos tenía hepatitis B como causa de la cirrosis. Otro estudio, de una muestra de casi 500 pacientes trasplantados hepáticos (la mitad por cirrosis y la otra mitad por hepatitis fulminante) de varios centros en Chile durante más de una década, mostró que sólo el 1% de los pacientes tenía hepatitis B.
Fases de cronicidad de la hepatitis B
La primera fase de la infección crónica por el virus de la hepatitis B es la fase inmunotolerante, habitualmente en pacientes niños o jóvenes que se infectan, cursan con HBeAg positiva, antígenos de superficie positivo, cargas virales habitualmente altas, con transaminasas normales y sin impacto histológico en el hígado.
Hay una fase posterior replicativa en el adulto inmunocompetente que se infectó y se hizo crónico donde se encuentran cargas virales moderadas a altas, pero tienen alto impacto de inflamación hepática (por una situación inmunológica) y son pacientes que requieren tratamiento antiviral. Por lo general tienen antígeno de superficie positivo, transaminasas elevadas y biopsia que demuestra actividad inflamatoria.
Posteriormente se encuentra la fase de portador inactivo; estos son pacientes que mediante su inmunidad logran controlar la infección y mantener cargas virales muy bajas, con transaminasas normales, periodo que puede mantenerse por muchos años sin necesidad de tratamiento.
Por último existe la posibilidad de reactivación con cepas mutantes de promotor core y son la forma antígeno e negativo, que también vuelve a tener actividad inflamatoria con transaminasas elevadas y que requiere tratamiento antiviral.
Los dos grupos que tienen transaminasas elevadas (fase replicativa y fase de reactivación) requieren tratamiento.
Tratamiento de la hepatitis B
Las hepatitis agudas no se tratan pues en general mejoran sin tratamiento y sólo algunos casos se hacen crónicos.
La hepatitis fulminante puede requerir un tratamiento antiviral corto, entre uno o dos meses, ya que muchas formas agudas mejoran, incluso sin necesidad de trasplante. El objetivo en la hepatitis fulminante es reducir la carga viral en espera de un eventual trasplante si lo requiere.
En la hepatitis crónica se debe evaluar cada caso particular. El paciente cirrótico con carga viral presente debe recibir tratamiento. En el coinfectado se debe tener especial cuidado porque los enfermos, por su situación de cofactores virales (ej. VIH, virus C), evolucionan con mayor frecuencia hacia la enfermedad hepática avanzada. Se debe considerar el riesgo de complicación hepática de cada enfermo en particular; si es una hepatitis crónica inmunoactiva con antígeno e positivo o negativo, así como los costos o efectos colaterales que puede tener que enfrentar el enfermo.
En el caso de un paciente con una hepatitis crónica por virus B (más de 6 meses con antígeno de superficie positivo), se deben evaluar las transaminasas: si se encuentran elevadas, se considera que el paciente puede ser candidato a recibir tratamiento. Se debe también evaluar la carga viral: en personas con antígeno e positivo o negativo y si el paciente tiene más de 2,000 UI, se debe considerar el tratamiento antiviral. En los casos complejos (carga viral baja, transaminasas normales) puede considerarse la realización de la biopsia hepática para definir la conducta terapéutica. Si en la biopsia hepática se encuentra fibrosis o inflamación relevante, se aconseja el inicio de terapia antiviral.
El objetivo del tratamiento antiviral es prevenir la progresión de la enfermedad a largo plazo (cirrosis y hepatocarcinoma). Por lo general, los gastroenterólogos se plantean diferentes objetivos al tratar la enfermedad; hasta hace un tiempo el objetivo era mejorar los parámetros bioquímicos del enfermo, pero actualmente se evalúa la mejoría histológica y los niveles de DNA intentando llegar a tener cargas virales indetectables. Si el antígeno e era positivo al inicio del tratamiento, el objetivo va encaminado a lograr la seroconversión (que se haga negativo durante el tratamiento) e idealmente la negativización del antígeno de superficie (lo cual se logra en un pequeño porcentaje de los casos: 3-5%). Finalmente, se intenta el aclaramiento del DNA viral incorporado, lo que por lo general no es posible.
Algoritmo del manejo de hepatitis crónica
La mayoría de las guías clínicas actuales están cambiando los valores de umbral para definir el inicio del tratamiento antiviral. Muchas guías definen una carga viral mayor a 2000 UI/ml como umbral para inicial antivirales (Guía Australiana, Nueva Zelanda, Alemana, Europea EASL, entre otras). La han cambiado a 2000UI/ml porque muchos pacientes que no eran considerados según la guía Americana (con carga viral entre 2.000 y 20.000 UI/ml) para iniciar terapia antiviral, evolucionaban a cirrosis o hepatocarcinoma.
En pacientes con antígeno e positivo, se considera que si tienen carga viral sobre 2.000 UI/ml y ALT elevada deberán recibir tratamiento. Pacientes con carga viral mayor a 2000 y ALT normal, es probable que se encuentren en fase inmunotolerante, por lo que se debe observar y controlar (Figura 1).
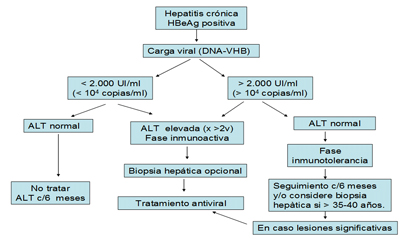 Tamaño completo
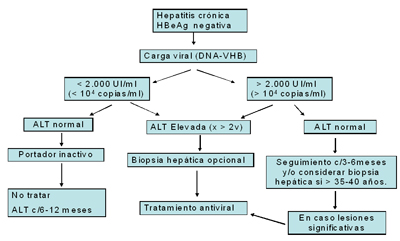
Tamaño completo El manejo en pacientes con antígeno e negativo (Figura 2), si la carga viral es mayor a 2000 UI/ml y con ALT elevada, se debe indicar tratamiento; si la ALT es normal, se deberá hacer seguimiento en forma regular cada 3- 6 meses. Si la carga viral es muy baja, con ALT normal, probablemente se trata de un paciente portador inactivo quien no debe recibir tratamiento y debe ser controlado cada 6 a 12 meses.
 Tamaño completo
Tamaño completo En la actualidad existen diferentes guías internacionales para el manejo de la hepatitis B de gran calidad y muy bien realizadas. Cada una tiene diferencias discretas en términos de puntos de corte, objetivos, etc.
Medicamentos para el tratamiento de la hepatitis B
En los últimos cinco años se ha determinado que el peginterferón, entecavir y tenofovir son las drogas de elección para el tratamiento de la hepatitis B. Hoy en día los medicamentos son de alta potencia y tienen una alta barrera genética, es decir que pueden asociarse a resistencia o mutaciones en un bajo porcentaje de casos.
Las consideraciones a favor del uso del peginterferón en algunos pacientes son: a) que el tiempo de tratamiento es limitado (un año); b) reciben sólo una dosis semanal; c) no se asocian a resistencia; d) tiene mejor respuesta terapéutica, especialmente en aquellos pacientes con mayor inflamación en genotipo A y B y antígeno e positivo.
Las consideraciones en contra del peginterferón incluyen: a) la respuesta es limitada, un tercio probablemente seroconvierte; b) son inyecciones semanales, lo que puede ser mal tolerado por el paciente (en algunos casos un año de molestias recurrentes tipo gripales con reposo parcial; c) su costo es bastante elevado; d) pueden descompensar a un paciente cirrótico (en estos casos puede estar contraindicado su uso).
Entre las ventajas de los antivirales orales se considera que son muy bien tolerados, dosis única diaria, alta barrera genética, prácticamente no generan resistencia (entecavir, tenofovir), son de elección en el cirrótico Child B y C pues no se descompensa el enfermo, y el efecto es muy rápido. En dos semanas se logra un 98% de descenso de la carga viral. Las desventajas incluyen el costo elevado, el tratamiento se puede extender por un tiempo muy largo (incluso de por vida), y también que puede generar resistencia a antivirales.
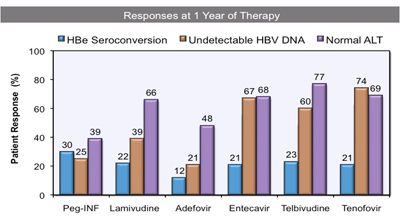
Dientstag y cols. mostraron las comparaciones de la respuesta al año de tratamiento en hepatitis B crónica HBeAg (+) (Figura 3). Con peginterferón hubo 30% de seroconversión de HBeAg y 39% de normalización de transaminasas al año; con entecavir hubo 21% de seroconversión de HBeAg y 67% de normalización de transaminasas (4, 5).
 Tamaño completo
Tamaño completo En pacientes en tratamiento con lamivudina, adefovir o con entecavir en dos o tres semanas se obtiene una respuesta extraordinaria. Sin embargo, los pacientes tratados con lamivudina o adefovir presentan una tasa elevada de resistencia a antivirales con lo cual hoy en día es preferible iniciar la terapia con un antiviral de bajo riesgo de generar resistencia (entecavir o tenofovir). A cinco años de tratamiento con lamivudina casi el 70% de las cepas son resistentes a lamivudina; 30% a adefovir; 1,2% a entecavir (esto es lo que le otorga una gran calidad antiviral). En el caso de tenofovir que se ha estudiado sólo a tres años y se ha demostrado 0% de resistencia.
Los trabajos a largo plazo, 5-10 años, sólo han sido realizados con lamivudina y adefovir. Se debe esperar para tener más información acerca de los últimos medicamentos antivirales.
Es importante evaluar en pacientes bajo tratamiento prolongado con lamivudina si desarrollan una elevación de la carga viral. En ellos debe considerarse el desarrollo de algunas mutaciones particulares y si desarrollan resistencia bajo lamivudina se deberá agregar algún medicamento que inhiba dichas cepas virales resistentes. Si está recibiendo lamivudina la elección es agregarle adefovir, o si estudiamos la resistencia, eventualmente considerar alguna otra posibilidad como tenofovir.
La monitorización de la respuesta en los pacientes sometidos a terapia oral se ha ido modificando (roadmap). En general se recomienda controlar a las 12 semanas, a las 24 semanas y al año de tratamiento. Ahora con el uso del entecavir y tenofovir esto se debe modificar ya que estos medicamentos no desarrollan resistencia al año.
Actualmente la recomendación del Ministerio de Salud de Chile es que se controle la carga viral a los 6 meses. Si ésta ha ido descendiendo en forma razonable, con una respuesta adecuada, se espera al año antes de tomar decisiones. Si la respuesta es mala se debe agregar un medicamento más potente que no tenga resistencia cruzada.

