Revisión clínica
← vista completaPublicado el 13 de diciembre de 2023 | http://doi.org/10.5867/medwave.2023.11.2719
Neumonía adquirida en la comunidad: epidemiología, diagnóstico, escalas pronósticas de gravedad y nuevas opciones terapéuticas
Community-acquired pneumonia: Epidemiology, diagnosis, prognostic severity scales, and new therapeutic options
Resumen
Este artículo de revisión narrativa tiene como objetivo explorar el conocimiento actual disponible basado en datos científicos respeto a la definición, la epidemiología, los criterios diagnósticos, la microbiología, el tratamiento y la prevención de la neumonía grave adquirida en la comunidad) en individuos adultos inmunocompetentes. En la actualidad, pese a los grandes avances científicos obtenidos en la evaluación diagnóstica, el manejo clínico, la terapia antimicrobiana y la prevención, la neumonía grave adquirida en la comunidad sigue siendo una causa importante de morbilidad y mortalidad, además de producir un gran impacto económico con la elevación de los costes sanitarios en todo el mundo. Esta patología es considerada una de las principales causas de sepsis/choque séptico, con una tasa de mortalidad global extremadamente elevada, lo que justifica todo el esfuerzo en el diagnóstico precoz, el manejo en un ambiente adecuado y el inicio temprano y apropiado de la terapia antimicrobiana. La inclusión de biomarcadores (aislados o en combinación) asociada a la aplicación de los criterios diagnósticos y escalas pronósticas de gravedad en la práctica clínica, sirven para identificar a los pacientes con neumonía adquirida en la comunidad grave, definir el ingreso inmediato en la unidad de cuidados intensivos y, de esta forma, minimizar los resultados negativos de esta grave patología.
Ideas clave
- La infección de las vías aéreas inferiores es una de las principales causas de morbilidad en todo el mundo.
- Las escalas pronósticas de gravedad más utilizadas en la práctica clínica en la evaluación de la neumonía adquirida en la comunidad son el Índice de la Gravedad de la Neumonía y el CURB-65, ambos con un buen desempeño en predecir la mortalidad a 30 días.
- La identificación precoz del patógeno causante de la neumonía grave adquirida en la comunidad es un importante paso en el diagnóstico etiológico, puesto que permite una mejor adecuación de la terapia antimicrobiana y da lugar a un mejor resultado clínico. No obstante, los métodos tradicionales utilizados en el diagnóstico microbiológico solo consiguen identificar a los patógenos entre el 30 y 40% de los casos de neumonía adquirida en la comunidad.
- Se aguarda la realización de nuevos ensayos clínicos que incluyan pacientes con neumonía grave adquirida en la comunidad, que realicen análisis de superioridad, en vez de estudios de no inferioridad de los nuevos antibióticos, de evaluación de casos adversos a largo plazo.
Introducción
La infección de las vías aéreas inferiores es una de las principales causas de morbilidad en todo el mundo. La neumonía adquirida en la comunidad es la segunda causa más frecuente de internación hospitalaria [1,2]. La incidencia de pacientes que necesitan de cuidados intensivos por neumonía grave adquirida en la comunidad viene aumentando globalmente, principalmente en la población de edad avanzada (mayor a 65 años), portadores de enfermedades crónicas (diabetes mellitus, demencia, insuficiencia cardiaca crónica, miocardiopatía isquémica), y en individuos con algún grado de inmunosupresión [3].
Jain et al, en 2015, a través de un amplio estudio poblacional en el que se hizo un seguimiento de pacientes hospitalizados con diagnóstico de neumonía adquirida en la comunidad, estimaron que el 21% de estos enfermos ingresaron en la unidad de cuidados intensivos y el 26% necesitaron soporte ventilatorio invasivo [4]. La mortalidad hospitalaria por neumonía grave adquirida en la comunidad es elevada, oscilando entre el 25% y más del 50% [5,6]. El retraso en la admisión en la unidad de cuidados intensivos se presenta como uno de los factores de peor pronóstico y mayor mortalidad intrahospitalaria [7]. A lo largo de los años, se han desarrollado y validado algunas escalas pronósticas de gravedad en la evaluación clínica de neumonía adquirida en la comunidad, con la finalidad de identificar a los pacientes que deben ser hospitalizados y admitidos inmediatamente en las unidades de cuidados intensivos e iniciarse el tratamiento antimicrobiano apropiado [8]. Aunque no exista un consenso mundial sobre la definición de neumonía grave adquirida en la comunidad, los criterios actualmente aceptados se basan en guías de práctica clínica internacionales. En esta revisión serán utilizadas las de la Sociedad de Enfermedades Infecciosas de América y de la Sociedad Torácica Americana (IDSA/ATS, por su siglas en inglés Infectious Diseases Society of America/American Thoracic Society), publicadas en el 2007 [9] y actualizadas por las mismas sociedades en 2019 [10]. La etiología microbiana de la neumonía grave adquirida en la comunidad no siempre es evidente en la práctica clínica, y los distintos estudios muestran resultados variables. El Streptococcus pneumoniae es el patógeno más comúnmente asociado a la neumonía bacteriana adquirida en la comunidad. La implementación de la técnica de reacción en cadena de la polimerasa (PCR) ha permitido identificar la implicación de los virus respiratorios en la etiología de la neumonía adquirida en la comunidad, especialmente el influenzavirus y el rinovirus [4] y, más recientemente, la implicación pandémica del virus SARS-CoV-2 (COVID-19) como causa de neumonía grave adquirida en la comunidad [11]. En pacientes con factores de riesgo se ha observado un aumento en la incidencia de neumonía adquirida en la comunidad causada por un grupo de bacterias multirresistentes a los antimicrobianos, y que recientemente se las nombró con el acrónimo PES (Pseudomonas aeruginosa, Enterobacteriaceae productoras de β-lactamasas de amplio espectro y Staphylococcus aureus resistente a la meticilina) [12].
Esta revisión narrativa tiene el objetivo de explorar el conocimiento actual relacionado con la definición, epidemiologia, criterios diagnósticos, etiología microbiana, tratamiento y prevención de la neumonía grave adquirida en la comunidad en individuos adultos inmunocompetentes. Su finalidad es el evidenciar la importancia del diagnóstico precoz, el tratamiento adecuado de las formas graves de neumonía adquirida en la comunidad y mejorar los resultados clínicos de esta afección.
Métodos
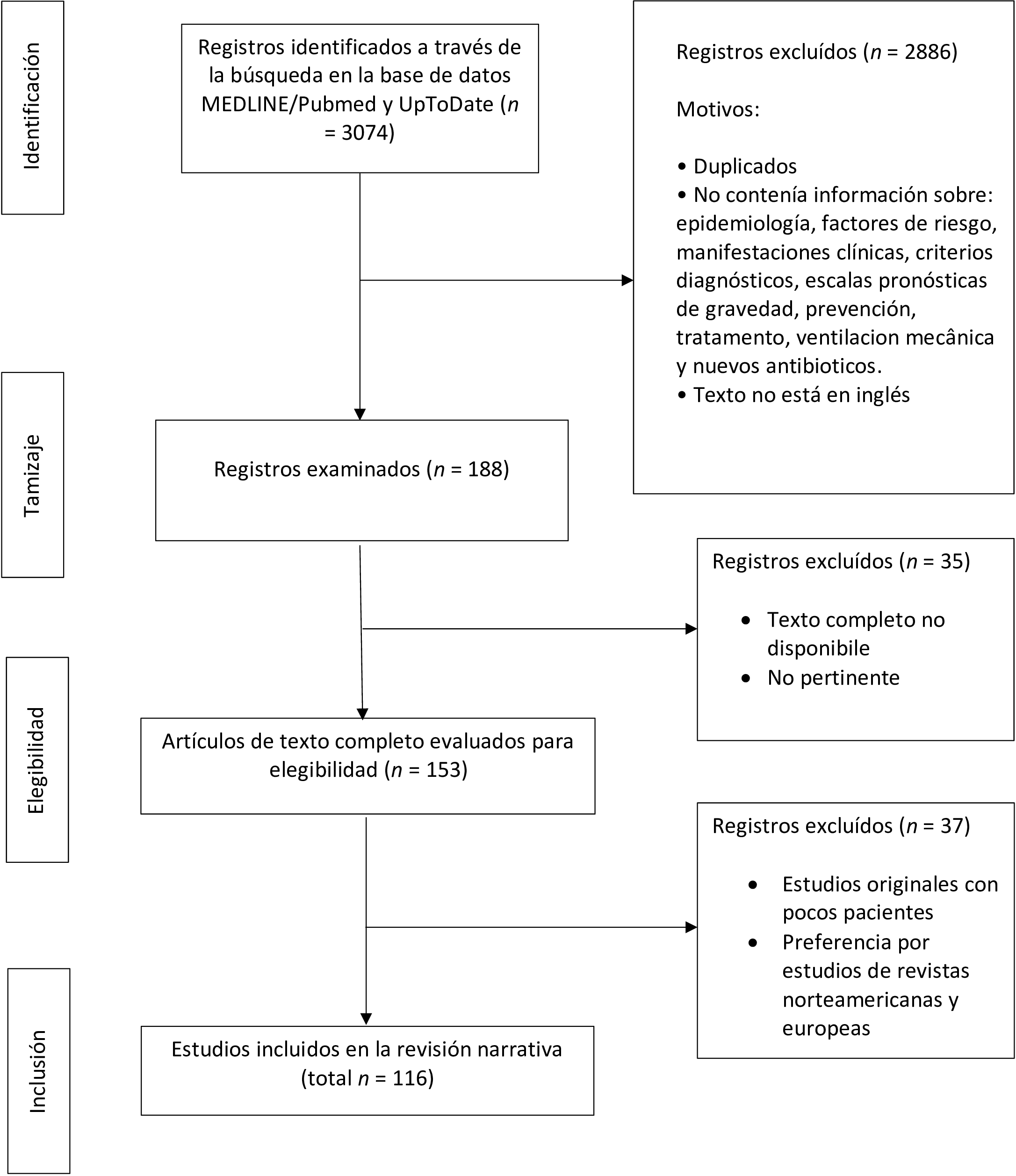
Se realizó una revisión bibliográfica mediante una búsqueda en la base de datos MEDLINE/PubMed, para el período comprendido entre 2017 y 2022, utilizando los siguientes términos: “pneumonia”, “severe community-acquired pneumonia” y “community-acquired pneumonia”. Se dio prioridad a las publicaciones de guías internacionales, artículos de revisión narrativa, revisiónes sistemáticas y metanálisis, en inglés. Los resúmenes de los artículos debían contener informaciones sobre los siguientes parámetros: epidemiología, factores de riesgo, manifestaciones clínicas, criterios diagnósticos y escalas pronósticas de gravedad, prevención y tratamiento. Solo se seleccionaron los artículos con acceso al texto completo. También se realizó una búsqueda en la base de datos UpToDate® utilizando el término “community-acquired pneumonia” (Figura 1).
Identificación y selección de los artículos.
Definición y epidemiología
La neumonía adquirida en la comunidad es una infección aguda que afecta a las unidades alveolares del parénquima pulmonar, con síntomas que se inician en la comunidad o incluso en las primeras 48 horas de hospitalización [13]. Puede presentarse con formas leves, caracterizadas por fiebre y tos productiva, y formas graves. La neumonía grave adquirida en la comunidad es frecuentemente una enfermedad multisistémica que puede evolucionar con fallo multiorgánico. Según los criterios de la Sociedad de Enfermedades Infecciosas de América y de la Sociedad Torácica Americana (IDSA/ATS), publicados en 2007 [9], la neumonía grave adquirida en la comunidad requiere la presencia de uno o más criterios mayores (ventilación mecánica invasiva o choque séptico con necesidad de vasopresor) o al menos tres de nueve criterios menores: frecuencia respiratoria mayor o igual a 30 respiraciones por minuto, relación entre presión arterial de oxígeno/fracción inspirada de oxígeno inferior a 250 milímetros de mercurio, infiltrado pulmonar multipolar, confusión/desorientación, nitrógeno ureico en sangre mayor o igual a 20 microgramos por decilitro, leucocitos inferior a 4000 células por milímetro cúbico, plaquetas inferior a 100 000 células por milímetro cúbico, temperatura corporal inferior a 36 grados Celsius, hipotensión arterial con necesidad de reanimación con fluidos.
La incidencia de hospitalización por neumonía adquirida en la comunidad varía considerablemente según la localización geográfica analizada, la metodología del estudio epidemiológico, la definición de caso utilizada y las características de la población estudiada. Recientemente, dos estudios estimaron la incidencia de hospitalización por neumonía adquirida en la comunidad en los Estados Unidos [4,14]. Griffon et al identificaron una incidencia anual de hospitalizaciones por neumonía adquirida en la comunidad, por cada 1000 adultos, de 1,2 entre 65 y 74 años; de 2,39 entre 75 y 84 años; y de 4,39 para los individuos con edad mayor o igual a 85 años en el periodo de 2007 a 2009 [14] Asimismo, observaron una mayor incidencia de enfermedad grave en edades más avanzadas. También en un estudio portugués, realizado en el periodo de 2000 a 2009, Froes et al reportaron una tasa de hospitalización por neumonía adquirida en la comunidad de 3,61 por 1000 individuos adultos, con una importante elevación de 13,3 por 1000, en el rango de edad mayor o igual a 65 años. Los autores también observaron que en el periodo de 2000 a 2009, la tasa anual de hospitalización por neumonía adquirida en la comunidad por cada 1000 individuos aumentó 28,2% [15].
En Brasil, la neumonía adquirida en la comunidad es la principal causa de hospitalización en el Sistema Único de Salud. En el año 2017 ocurrieron 598 688 hospitalizaciones por neumonía adquirida en la comunidad [16].
Entre los factores de riesgo relacionados con una mayor mortalidad por neumonía adquirida en la comunidad se encuentran: edad avanzada (mayor a 65 años), presencia de enfermedades crónicas (enfermedad pulmonar obstructiva crónica, bronquiectasias, asma, cardiopatías crónicas, accidente cerebrovascular, diabetes mellitus), sepsis, choque séptico, antibioticoterapia inadecuada, necesidad de ventilación mecánica e hipoalbuminemia [9].
Por su parte, Restrepo et al observaron que el retraso en el inicio de los antimicrobianos apropiados y/o la demora en la admisión en la unidad de cuidados intensivos, se asociaban con pronósticos desfavorables en la evolución de los pacientes internados por neumonía grave adquirida en la comunidad [17].
Asimismo, la presencia de tabaquismo activo aumenta significativamente el riesgo de desarrollar neumonía adquirida en la comunidad, principalmente cuando se vincula a la existencia de inmunodeficiencia [18].
Escalas pronósticas de gravedad
La identificación precoz de los pacientes con neumonía grave adquirida en la comunidad se considera una etapa fundamental en la evaluación inicial de los enfermos y muy necesaria para la definición del tratamiento clínico más rápido y apropiado, además de evitar retrasos en el traslado del paciente a la unidad de cuidados intensivos y, por lo tanto, minimizar los resultados desfavorables relacionados con la gravedad de la enfermedad [19,20].
Se han validado múltiples escalas pronósticas de gravedad, que se utilizan en la evaluación clínica inicial y que ayudan a decidir si tratar la neumonía adquirida en la comunidad en el ámbito ambulatorio o en el hospitalario. Sin embargo, la mayoría aún falla en predecir la necesidad de admisión en la unidad de cuidados intensivos [21]. La identificación del entorno más apropiado para el tratamiento clínico del paciente con neumonía grave adquirida en la comunidad es una importante variable que debe evaluarse mediante escalas pronósticas de gravedad. Estudios clínicos identificaron que el tiempo de hospitalización y la mortalidad intrahospitalaria fueron mayores en los pacientes con neumonía grave adquirida en la comunidad y que, inadvertidamente, iniciaron el tratamiento en una unidad de hospitalización no destinada a pacientes graves, siendo posteriormente trasladados a la unidad de cuidados intensivos, en comparación con los que fueron apropiadamente trasladados de la sala de urgencias a la unidad de cuidados intensivos [17,22].
Las escalas pronósticas de gravedad más utilizadas en la práctica clínica para la evaluación de la neumonía adquirida en la comunidad son el Índice de Gravedad de la Neumonía (PSI) y el CURB-65 (acrónimo en inglés para confusión: calificación menor a 8 en la prueba mental abreviada; urea: mayor a 43 miligramos por decilitro o nitrógeno ureico en sangre mayor a 7 milimol; respiración: frecuencia mayor a 30 respiraciones por minuto; presión sanguínea: sistólica menor a 90 milímetros de mercurio o diastólica menor o igual a 60 milímetros de mercurio; y edad igual o superior a 65 años). Ambas herramientas funcionan bien para predecir la mortalidad a 30 días, pero son poco útiles para identificar la neumonía grave adquirida en la comunidad que requiere ingreso en la unidad de cuidados intensivos [23]. Sobre esto, Torres et al identificaron que los predicadores de mortalidad en la neumonía adquirida en la comunidad están muy influidos por la edad del paciente y muy poco por la presencia de insuficiencia respiratoria y otras disfunciones orgánicas, que suelen conducir a la necesidad de cuidados intensivos [22].
Se han propuesto otras escalas pronósticas como IDSA/ATS 2007, criterios menores de la IDSA/ATS simplificados, SMART-COP (presión sanguínea sistólica inferior a 90 milímetros de mercurio; afectación multilobar; albúmina menor a 3,5 gramos por decilitro; frecuencia respiratoria ajustada por la edad; taquicardia menor o igual a 125; confusión; oxigenación ajustada por edad; pH menor a 7,35), SCAP (Severe Community Acquired Pneumonia), y más dirigidas a identificar la existencia de disfunciones orgánicas en pacientes con neumonía adquirida en la comunidad. Los criterios clínicos y laboratoriales de IDSA/ATS 2007 son los más pragmáticos y sólidos para identificar a los pacientes con neumonía grave adquirida en la comunidad y que necesitan de terapia intensiva [22] (Tabla 1).
Recientemente se ha demostrado que los criterios diagnósticos de Sepsis-3, representados por el q-SOFA (frecuencia respiratoria mayor o igual a 22 incursiones respiratorias por minuto, estado mental alterado y presión arterial sistólica menor o igual a 100 milímetros de mercurio), también pueden auxiliar en la identificación de los pacientes con neumonía adquirida en la comunidad grave atendidos en urgencias. Con todo, la utilización de instrumentos específicos de la enfermedad (Índice de Gravedad de la Neumonía y CURB-65) ha evidenciado un mejor poder discriminatorio en predecir el riesgo de muerte [24].
Diagnostico microbiológico
La identificación precoz del patógeno causante de la neumonía grave adquirida en la comunidad es un importante paso en el diagnóstico etiológico, puesto que permite una mejor adecuación de la terapia antimicrobiana y da lugar a un mejor resultado clínico. Sin embargo, los métodos tradicionales utilizados en el diagnóstico microbiológico solo son capaces de identificar a los patógenos entre el 30 y 40% de los casos de neumonía adquirida en la comunidad [4,25]. Cillóniz et al, demostraron que los hemocultivos presentan una baja sensibilidad diagnóstica, con una tasa de detección bacteriana estimada entre el 5 y el 15%. Cuando son positivos presentan un importante valor clínico, ya que ayudan a dirigir la terapia antimicrobiana. La presencia de un menor tiempo en la posibilidad de hemocultivos (inferior a 10 horas) se considera un factor de riesgo independiente para la necesidad de ventilación mecánica invasiva, mayor tiempo de permanencia hospitalaria, mayor mortalidad intrahospitalaria y mayor mortalidad a 30 días [26]. Pese a que las técnicas de diagnóstico molecular basadas en la PCR han mejorado las tasas de diagnóstico para algunos virus y bacterias más comúnmente relacionados con la etiología de la neumonía adquirida en la comunidad [27,28]; el valor diagnóstico de estas técnicas sigue restringido a un bajo número de agentes microbianos [29]. Recientemente, la técnica de secuenciamiento metagenómico de próxima generación se ha convertido en una potente y prometedora herramienta diagnóstica en la identificación de microorganismos responsables de la etiología de enfermedades infecciosas, cuyos resultados no se ven afectados por el uso previo de antibioticoterapia. Se han publicado estudios científicos sobre la utilización de secuenciamiento metagenómico de próxima generación en material obtenido de lavado broncoalveolar, en la identificación del microorganismo causante de la neumonía grave adquirida en la comunidad [30,31]. La implementación de estas nuevas técnicas diagnósticas en la práctica clínica es parcialmente difícil; en parte debido a su elevado coste y en parte, por la falta de estandarización de estas pruebas. Otro factor a tener en cuenta es el carácter altamente sensible de estas técnicas, que dificulta en algunos casos la diferenciación entre colonización e infección [21].
En la publicación de 2019, la IDSA/ATS a través de la guía para el diagnóstico y tratamiento de la neumonía adquirida en la comunidad en adultos, sugirió que el diagnóstico etiológico debe obtenerse mediante técnicas de tinción utilizando la técnica de Gram y cultivos de muestras obtenidas de las vías respiratorias inferiores, hemocultivos, investigación de la presencia de antígenos urinarios para Legionella y neumococo. También sugiere pruebas virales para influenza y coronavirus, en pacientes adultos que requieran tratamiento en un ambiente hospitalario y clasificados con neumonía grave adquirida en la comunidad [32], o con factores de riesgo de Staphylococcus aureus resistente a la meticilina (SAMR) o Pseudomonas aeruginosa (Tabla 2).
El Streptococcus pneumoniae sigue siendo el patógeno bacteriano más común en la neumonía grave adquirida en la comunidad, independientemente de la edad o las comorbilidades [9]. Aunque se ha observado un aumento de la incidencia de cepas de Streptococcus pneumoniae resistentes a los antimicrobianos, Gattarello et al reportaron una disminución de la mortalidad intrahospitalaria en pacientes internados en la unidad de cuidados intensivos con diagnóstico de neumonía neumocócica grave adquirida en la comunidad, posiblemente debido al inicio precoz de los antimicrobianos y a la terapia combinada [33]. Por otro lado, en un estudio de cohorte retrospectivo de pacientes diagnosticados de neumonía grave adquirida en comunidad Valles et al identificaron al Streptococcus pneumoniae como el patógeno más frecuente, con una incidencia total del 41,6% y superior al 80% cuando se consideraran conjuntamente todas las causas de bacteriemia [34]. Otros patógenos implicados en la etiología de la neumonía grave adquirida en la comunidad son los virus (influenza y sus serotipos, virus sincitial respiratorio, SARS-CoV-2, MERS-CoV, rinovirus humano), las bacterias atípicas (Legionella pneumophila, Mycoplasma pneumoniae), Haemophilus influenzae, Staphylococcus aureus (incluido Staphylococcus aureus resistente a la meticilina), enterobacterias gramnegativas (Pseudomonas aeruginosa, Acinetobacter baumanii, Klebsiella pneumoniae) y más raramente, bacterias anaeróbicas.
La utilización de nuevas técnicas de diagnóstico molecular ha permitido detectar la presencia de partículas virales en muestras de material obtenidas de las vías aéreas de pacientes con neumonía e identificar una mayor incidencia de virus en la etiología de la neumonía grave adquirida en la comunidad [4,35,36]. Más recientemente, el virus SARS-CoV-2 originado en Wuhan, China, en 2019 (COVID-19), ha sido identificado como causa de neumonía grave adquirida en la comunidad y ha generado rápidamente una pandemia mundial por sus elevadas tasas de transmisibilidad. Pese a que las infecciones virales respiratorias sean consideradas una de las principales causas de neumonía grave adquirida en la comunidad, Qhah et al observaron que entre los pacientes con coinfección bacteriana había un mayor riesgo de mortalidad intrahospitalaria [37]. Varios mecanismos virales, como la rotura de la pared epitelial bronquial, la regulación positiva de las proteínas de adhesión celular o la desregulación del sistema inmunológico, pueden facilitar la infección bacteriana concomitante [38]. Este sinergismo puede explicar el peor pronóstico de los pacientes con neumonía grave adquirida en la comunidad causada por coinfección vírico-bacteriana, principalmente entre virus influenza y Streptococcus pneumoniae [39]. Los patógenos atípicos más frecuentemente asociados como causantes de la neumonía grave adquirida en la comunidad son Legionella pneumophila y Mycoplasma pneumoniae; la prevalencia de Chlamydia pneumoniae como causa de neumonía grave adquirida en la comunidad es inferior al 1%, según estudios recientes [40,41]. Mientras que el Mycoplasma pneumoniae produce, en la mayor parte de las veces, una enfermedad leve y autolimitada. En cambio, la Legionella pneumophila puede ser causa de la neumonía grave adquirida en la comunidad [42,43]. Para que un patógeno atípico sea identificado como causante de la neumonía adquirida en la comunidad, es necesario que el paciente presente un cultivo positivo, una reacción en cadena de la polimerasa positiva o detección de antígeno urinario para Legionella pneumophila o incluso, frotis orofaríngeo positivo para Mycoplasma pneumoniae, en ausencia de identificación de otro agente bacteriano [44].
Las Pseudomonas aeruginosa, las enterobacterias productoras de β-lactamasa de espectro amplio y el Staphylococcus aureus resistente a la meticilina forman otro importante grupo de patógenos causantes de la neumonía grave adquirida en la comunidad. Este grupo bacteriano es responsable por aproximadamente el 6% de los pacientes con neumonía adquirida en la comunidad, admitidos para recibir tratamiento en ambiente intrahospitalario [12]. Los factores de riesgo de patógenos de tipo enterobacterias productoras de β-lactamasa de espectro amplio positivos y Staphylococcus aureus resistente a la meticilina, incluyen pacientes con uso previo de antimicrobianos parenterales en los últimos 180 días, baja funcionalidad (índice funcional de Barthel inferior a 50), hospitalización previa por un tiempo superior a 48 horas en los últimos 90 días, necesidad de hemodiálisis e inmunosupresión [45].
Tratamiento
De acuerdo a las guías IDSA/ATS para el manejo clínico de las reacciones de neumonía adquirida en la comunidad en individuos adultos inmunocompetentes, publicadas en 2019, la terapia antimicrobiana de elección dependerá del lugar donde se vaya a realizar el tratamiento, ya sea en el ambiente intrahospitalario o ambulatorio [32]. La terapia antimicrobiana empírica debe iniciarse tan pronto como se realice el diagnóstico de neumonía grave adquirida en la comunidad y se basa en los siguientes criterios: análisis de la microbiología local, patógeno más probable, presencia de comorbilidades y/o existencia de factores de riesgo de patógenos resistentes a los antimicrobianos [46].
Una vez que se diagnostique la neumonía grave adquirida en la comunidad y sean colectadas las muestras para cultivos, los antimicrobianos deben iniciarse de inmediato con el objetivo de reducir la progresión de la enfermedad y mejorar el pronóstico con una disminución de la mortalidad intrahospitalaria. La guía de la Sociedad Torácica Americana para el tratamiento de la neumonía adquirida en la comunidad en adultos, recomienda que el antibiótico sea administrado en las primeras cuatro horas luego del diagnóstico [47]. Vale resaltar que, en publicación de 2019 la IDSA/ATS ha recomendado el abandono del término “neumonía asociada a la asistencia sanitaria”, utilizado en la publicación de 2007 [9]. El objetivo de este cambio de nominación es el evitar la utilización excesiva de terapia empírica basada en antimicrobianos de amplio espectro, puesto que los estudios clínicos no evidenciaron un aumento de la incidencia de bacterias resistentes a los antibióticos en esta población [48,49]. En relación a las características farmacocinéticas y farmacodinámicas de la terapia antimicrobiana en pacientes graves, las concentraciones orgánicas de los antibióticos presentan oscilaciones tanto en el plasma como en el líquido extracelular, especialmente en condiciones clínicas concomitantes como la lesión renal aguda y en el estado circulatorio hiperdinámico presente en pacientes sépticos, lo que puede comprometer la eficacia del fármaco.
Durante la decisión para el uso del antimicrobiano más apropiado para el tratamiento grave por reacción en cadena de la polimerasa grave, todos los pacientes deberán ser evaluados para detectar la presencia de factores de riesgo de bacterias resistentes a los antibióticos. Actualmente, los factores de riesgo individuales más importantes para la infección respiratoria por Staphylococcus aureus resistente a la meticilina y Pseudomonas aeruginosa son el aislamiento previo de estos microorganismos mediante cultivos, especialmente del tracto respiratorio, la hospitalización previa durante más de 48 horas en los últimos 90 días, y la exposición a antibioticoterapia endovenosa previa [50,51,52]. Se sabe que hasta el momento no existe ningún sistema de puntuación con una buena probabilidad posterior a la prueba que pueda ser utilizado en la práctica clínica para la identificación de pacientes con riesgo de infección respiratoria por bacterias multirresistentes [32].
Las guías IDSA/ATS [32], recomiendan que el enfermo con neumonía grave adquirida en la comunidad, admitido en la unidad de cuidados intensivos y sin factores de riesgo de bacterias resistentes a los antimicrobianos, sea tratado con doble terapia, o sea, betalactámico asociado con macrólido o quinolona respiratoria (levofloxacino o moxifloxacino). Los estudios demuestran que la asociación terapéutica entre betalactámico y un macrólido presenta un beneficio en la disminución de la mortalidad [53,54,55,56]. En esta línea, tres teorías pueden explicar este hecho: mejor cobertura para patógenos atípicos, incluida la Legionella; supresión de la producción de endotoxinas (como la neumolisina) por el Streptococcus pneumoniae [57]; y efecto inmunomodulador en el organismo del paciente.
Por otro lado, en pacientes con neumonía grave adquirida en la comunidad y con factores de riesgo de infección por bacterias multirresistentes, las guías IDSA/ATS 2019 [32], recomiendan la terapia empírica de acuerdo al microorganismo sospechoso. Si es Staphylococcus aureus resistente a la meticilina, vancomicina (15 miligramos por kilogramo cada 12 horas, con ajustes según nivel sérico o mediciones de concentración de acuerdo al parámetros farmacocinéticos y farmacodinámicos) o linezolida (600 miligramos cada 12 horas). Si es Pseudomonas aeruginosa: piperacilina/tazobactam (4,5 gramos cada 6 horas), cefepima (2 gramos cada 8 horas), ceftazidima (2 gramos cada 8 horas) o meropenem (1 gramo cada 8 horas).
Se reconoce que la etiología vírica es una causa frecuente de neumonía grave adquirida en la comunidad y, en muchos pacientes se observa la presencia de coinfección viral y bacteriana [21]. Las guías de la Infectious Diseases Society of America/American Thoracic Society (IDSA/ATS) recomiendan la utilización de tratamiento anti-influenza (oseltamivir) en todos los pacientes con infección grave documentada por el virus influenza, independientemente de la duración de los síntomas [32]; aunque se reconoce que el mayor beneficio del antiviral se produce en las primeras 48 horas del inicio de los síntomas o de la hospitalización [58]. Adicionalmente, los estudios clínicos demuestran que es beneficioso iniciar el tratamiento antiviral hasta 4 o 5 días luego del inicio de los síntomas [59,60]. Asimismo, debido a la elevada incidencia de coinfección viral y bacteriana, se recomienda la asociación de antibioticoterapia, especialmente para cubrir Streptococcus pneumoniae y Staphylococcus aureus. No obstante, se debe realizar la desescalada antibiótica en caso de que no haya evidencia clínica o laboratorial de coinfección bacteriana y el paciente presente estabilidad clínica después de 48 a 72 horas de tratamiento [32].
Además de eso, en pacientes con COVID-19, se observa con cierta frecuencia la neumonía bacteriana [61,62]. La mayoría de los enfermos con infiltrado pulmonar han evidenciado en pruebas de diagnóstico por imagen que deben recibir antibioticoterapia, y esta debe ser discontinuada basándose en la evaluación clínica y en el nivel sérico de biomarcadores como la procalcitonina [63,64]. También en pacientes hospitalizados con COVID-19, el uso del antiviral remdesivir mostró algún beneficio, particularmente cuando se ha iniciado precozmente en el transcurso de la enfermedad [65]. El estudio ACT-1 [66] ha demostrado que el remdesevir fue superior al placebo en la reducción del tiempo de recuperación en adultos hospitalizados, mientras que el estudio SOLIDARITY [67] no evidenció ningún beneficio en la reducción de la mortalidad. Actualmente, el remdesevir es recomendado en pacientes con COVID-19 grave que necesitan de oxigenoterapia, excluyendo la ventilación mecánica y el soporte respiratorio extracorpóreo [68].
Corticosteroides
Independientemente del patógeno asociado, la infección de las vías aéreas inferiores está asociada a una importante respuesta inflamatoria local, y en algunos casos sistémica, mediada por citoquinas inflamatorias, lo que resulta en la alteración de la permeabilidad capilar en la membrana alveolar y a la salida del contenido inflamatorio hacia los alvéolos, siendo este el mecanismo responsable de la gravedad de la enfermedad respiratoria [69]. Los corticoides tienen como principal mecanismo de acción la supresión de la expresión de los genes relacionados con la producción de proteínas proinflamatorias de la respuesta inmunológica, lo que explica su efecto predominantemente antinflamatorio [70]. Debido a sus efectos inmunomoduladores, los corticoides son frecuentemente utilizados como terapia adjunta en el tratamiento de la neumonía grave adquirida en la comunidad [71]. Sin embargo, su eficacia y seguridad siguen siendo cuestionable [72].
En los últimos años se han publicado diversas revisiones sistemáticas y metanálisis que exploran la eficacia de la corticoterapia en el tratamiento de la neumonía grave adquirida en la comunidad. En 2017, Cochrane publicó un metanálisis que incluyó 17 ensayos clínicos aleatorizados, con 2264 pacientes y que ha evidenciado una reducción de la mortalidad y morbilidad en adultos diagnosticados de neumonía grave adquirida en la comunidad [73]. Más recientemente, otro metanálisis ha mostrado diferentes resultados, dependiendo del tipo de corticoide utilizado, siendo que la terapia con prednisolona y metilprednisolona tuvo un impacto en la reducción de la mortalidad de los pacientes, lo que no fue observado en la utilización de hidrocortisona. Los autores también observaron que el tiempo de permanencia en la unidad de cuidados intensivos fue significativamente menor en el grupo de pacientes que utilizó corticoides en comparación con el grupo control, habiendo también una tendencia a la reducción de la necesidad de ventilación mecánica en los pacientes del grupo de intervención [72]. Ya Meduri et al, mediante el estudio ESCAPe (ensayo clínico doble ciego, aleatorizado y controlado con placebo), en el que participaron 584 pacientes hospitalizados en la unidad de cuidados intensivos por neumonía grave adquirida en la comunidad, cuyo grupo de intervención recibió metilprednisolona durante 20 días: 40 miligramos al día durante 7 días, 20 miligramos al día durante los siguientes 7 días, 12 miligramos al día durante 3 días y, finalmente, 4 miligramos al día en los últimos 3 días, observaron que no hubo reducción significativa de la mortalidad a los 60 días, en comparación con el grupo de control [74].
Recientemente, PF Dequien et al a través del estudio CAPE COD Trial (ensayo multicéntrico, doble ciego, aleatorizado y controlado con placebo), en el que fueron evaluados 800 pacientes con neumonía grave adquirida en la comunidad hospitalizados en la unidad de cuidados intensivos, han demostrado que el uso de hidrocortisona a dosis de 200 miligramos al día, en comparación con el placebo, disminuyó la mortalidad a los 28 días, y se asoció a una disminución de la necesidad de vasopresores y ventilación mecánica [75].
Actualmente, las guías recomiendan que no se utilicen corticoides en el tratamiento de la neumonía grave adquirida en la comunidad por virus influenza. Sin embargo, mencionan que puede ser importante en el tratamiento de la neumonía bacteriana grave, especialmente en casos de choque séptico o en casos de neumonía adquirida en la comunidad por neumococos, y en la neumonía neumocócica asociada a meningitis [32].
Por otra parte, varios estudios clínicos sugieren que el uso de corticoides como terapia adjunta en el tratamiento de enfermos con neumonía grave por influenza, puede estar asociado a una mayor tasa de mortalidad, además de estar relacionado con un incremento en el número de días dependientes de ventilación mecánica, del tiempo de hospitalización y el aumento en la tasa de infecciones secundarias, posiblemente como resultado de la inmunosupresión concomitante [76,77,78].
A diferencia de la neumonía grave adquirida en la comunidad por influenza, los pacientes con COVID-19 grave, es decir, los que evolucionan con insuficiencia respiratoria y necesidad de oxigenoterapia no invasiva o ventilación mecánica invasiva; presentan una mejor sobrevida a los 28 días cuando son tratados con corticoides [79]. Lo mismo se evidenció en los pacientes con síndrome de estrés respiratorio agudo moderado o grave por COVID-19 y necesidad de ventilación mecánica invasiva, en quienes el uso de corticoides en dosis más elevadas estuvo asociado a un aumento en el número de días vivo y libre de ventilación mecánica a los 28 días [75,80]. Este beneficio del uso de corticoides en COVID-19 se vio reforzado posteriormente por un metanálisis que incluyó siete estudios aleatorizados controlados que incluyeron un total de 1703 pacientes críticos con COVID-19 de 12 países diferentes, en los que se evidenció una disminución de la mortalidad por todas las causas a los 28 días [81].
Biomarcadores
Los biomarcadores son sustancias que se miden objetivamente que pueden utilizarse como indicadores de un proceso fisiológico, o patológico, de una respuesta a una intervención terapéutica o de la progresión de una enfermedad [82]. Los biomarcadores de infección deben poseer características que faciliten el diagnóstico, el pronóstico y el seguimiento clínico [83]. En la neumonía, diversos estudios han evaluado el papel de los biomarcadores en el diagnóstico, la etiología, la estratificación del riesgo, la gravedad de la enfermedad, así como el inicio, la duración y la interrupción de la terapia antimicrobiana [84]. Los biomarcadores inflamatorios más estudiados y utilizados en la práctica clínica son la proteína C reactiva y la procalcitonina [85].
La proteína C reactiva es una importante proteína de fase aguda producida por los macrófagos en respuesta a cualquier tipo de inflamación, incluidas las infecciones bacterianas y virales. Es detectada en la sangre entre 4 y 6 horas después de la agresión aguda, con un máximo de concentración entre 36 y 48 horas. Pese a esto, la proteína C reactiva tiene una baja especificidad en el diagnóstico de neumonías, pudiendo estar elevada en otras condiciones inflamatorias, como la neoplasia, las enfermedades autoinmunes y los procesos inflamatorios agudos no infecciosos, como en el trauma [86].
La procalcitonina es un péptido precursor de la hormona calcitonina, producido en la glándula tiroidea y se encuentra elevada durante la evolución de enfermedades infecciosas e inflamatorias, primariamente como un reactante de fase aguda producido por el hígado. En individuos saludables, la concentración de procalcitonina es extremadamente baja (inferior a 0,1 nanogramo por mililitro). Sin embargo, sus niveles son elevados en infecciones bacterianas [86]. En individuos hospitalizados por neumonía adquirida en la comunidad, la procalcitonina se ha estado estudiando con el objetivo de utilizarla como una herramienta que puede ayudar a reducir la duración de la terapia antimicrobiana. Diversos estudios vienen utilizando la medición seriada de la procalcitonina como parámetro para la creación de algoritmos clínicos que permitan determinar con seguridad la interrupción del tratamiento antibiótico [87,88,89].
Así, por ejemplo, Salluh et al, propusieron un algoritmo en el que la antibioticoterapia se inicia con un tiempo de duración predeterminado. Posteriormente, se utiliza la medición seriada de la procalcitonina en asociación con la evolución clínica del paciente con neumonía adquirida en la comunidad para determinar el momento de descontinuación del antimicrobiano de forma segura [90].
Nuevos antibióticos
En las últimas décadas, se vienen realizando muchos esfuerzos en la investigación y el desarrollo de nuevos fármacos antimicrobianos para el tratamiento de la neumonía grave adquirida en la comunidad bacteriana (Tabla 3). No obstante, estos nuevos antibióticos son frecuentemente dirigidos al tratamiento de infecciones por bacterias multirresistentes.
La mayoría de los ensayos clínicos fueron realizados en pacientes con neumonía grave adquirida en la comunidad, de tipo bacteriana y sin criterios de gravedad; en los que se excluyó a los pacientes con neumonía adquirida en la comunidad grave y necesidad de hospitalización en unidad de cuidados intensivos [91,92,93,94,95,96,97,98]. Las recomendaciones para el uso de estos nuevos fármacos en el grupo de enfermos con neumonía adquirida en la comunidad grave son extrapolaciones de estudios clínicos donde estos pacientes no estaban debidamente representados. Por lo tanto, se aguarda la realización de nuevos ensayos clínicos con inclusión de pacientes con neumonía grave adquirida en la comunidad, que realicen análisis de superioridad, en vez de estudios de no inferioridad de los nuevos antibióticos, además de la evaluación de casos adversos a largo plazo [99].
Pese a que el Streptococcus pneumoniae es el principal patógeno responsable de la neumonía grave adquirida en la comunidad , en las últimas décadas ha crecido el interés por el papel de las bacterias gramnegativas en este tipo de neumonía, especialmente en pacientes con enfermedades pulmonares crónicas y en aquellos con uso previo de antimicrobianos [100].
El incremento en la resistencia bacteriana es un factor limitante en el tratamiento de neumonías causadas por bacterias gramnegativas multidrogorresistentes, dificultando la antibioticoterapia eficaz y haciendo de esta condición una preocupación global en salud pública. Además, ello desencadena un aumento en los costes sanitarios, en el tiempo de hospitalización y en la mortalidad [101].
Por este motivo, diversos nuevos antimicrobianos vienen siendo desarrollados orientados a aumentar las posibilidades terapéuticas contra gérmenes que pueden presentar diferentes mecanismos de resistencia ante los antimicrobianos comúnmente utilizados. Un ejemplo es el ceftobiprol, una cefalosporina de quinta generación con actividad frente a bacterias gramnegativas como Haemophilus influenzae, Moraxella catarrhalis y Pseudomonas aeruginosa, débil actividad contra bacterias productoras de β-lactamasas do tipo AmpC, y ninguna actividad frente a enterobacteriaceae productoras de β-lactamasas de espectro extendido, productoras de carbapenemasas y de metalo-β-lactamasas. Además, no presenta actividad contra Burkholderia cepacia y Stenotrophomonas maltophilia. El ceftobiprol también presenta una actividad significativa contra gérmenes grampositivos, como, Streptococcus pneumoniae y Staphylococcus aureus resistente a la meticilina [102].
Por otra parte, el ceftolozane-tazobactam es una combinación de la cefalosporina modificada ceftolozane con el inhibidor de β-lactamasa tazobactam. El ceftolozane presenta estabilidad ante diferentes mecanismos de resistencia de las bacterias gramnegativas como las productoras de β-lactamasas de tipo AmpC y las bombas de eflujo, además de ser el β-lactámico con mayor actividad frente a Pseudomonas aeruginosa incluidas las cepas multirresistentes. La combinación ceftolozane-tazobactam muestra actividad frente a enterobacteriaceae productoras de β-lactamasas de espectro extendido. Sin embargo, no presenta actividad ante gramnegativas productoras de carbapenemasas, incluyendo Pseudomonas aeruginosa. Esta combinación también carece de efecto contra Acinetobacter baumanni y Stenotrophomonas maltophilia [103].
Ya la ceftazidima-avibactam es una combinación formada por una cefalosporina de tercera generación y un inhibidor de β-lactamasa no β-lactámico. El avibactam protege a la ceftazidima de la hidrólisis causada por diferentes clases de β-lactamasas, como las β-lactamasas de tipo A (enterobacterias productoras de β-lactamasa de espectro amplio y Klebsiella pneumoniae productoras de carbapenemasas), de tipo C (productoras de β-lactamasas de tipo AmpC) y de tipo D (OXA-48). Con todo, presenta una baja actividad contra β-lactamasas de tipo B, Acinetobacter baumanni, bacterias gramnegativas anaerobias y cocos grampositivos. La ceftazidima-avibactam también es activa contra las enterobacteriaceae resistentes a los carbapenémicos, donde se ha demostrado que el 80% de las cepas aisladas demuestran susceptibilidad in vitro. Al rededor del 90% de las cepas de Pseudomonas aeruginosa aisladas presentan susceptibilidad a la ceftazidima-avibactam; así como cerca de dos tercios de las cepas no susceptibles a la ceftazidima y tres cuartas partes de las cepas de Pseudomonas aeruginosa resistentes a los carbapenemes son susceptibles a esta combinación [104,105].
El cefiderocol es una nueva cefalosporina modificada con una cadena lateral de catecol que forma un complejo quelado con hierro. El cefiderocol inhibe la síntesis de la pared celular al unirse a las proteínas de unión a la penicilina, frenando así la síntesis de peptidoglucano. Este nuevo tipo de cefalosporina mantiene su misma actividad en presencia de β-lactamasas de tipo A, B, C y D. En más de 28 000 cepas de bacterias gramnegativas aisladas se encontró más del 99% de enterobacterias (Escherichia coli, Klebsiella spp, Citrobacter spp y Serratia spp) susceptibles al cefiderocol. De la misma forma, se encontró susceptibilidad in vitro por parte de Pseudomonas aeruginosa, Burkholderia cepacia y Stenotrophomonas maltophilia [106,107].
Soporte ventilatorio
El aspecto principal en el tratamiento no farmacológico del paciente con neumonía grave adquirida en la comunidad consiste en el soporte respiratorio, que varía desde la oxigenoterapia convencional, la ventilación mecánica no invasiva, la oxigenoterapia con cánula nasal de alto flujo, hasta la ventilación mecánica invasiva.
La ventilación mecánica no invasiva y la cánula nasal de alto flujo son dos métodos de asistencia respiratoria que disminuyen el trabajo respiratorio. Estos procedimientos proporcionan una mejor oxigenación, con el objetivo de evitar entubación y disminuir la mortalidad en pacientes con insuficiencia respiratoria aguda hipoxémica. Según la bibliografía disponible hasta la fecha, la decisión entre usar ventilación mecánica no invasiva o cánula nasal de alto flujo sigue siendo incierta.
En pacientes con insuficiencia respiratoria aguda secundaria a neumonía, el uso de ventilación mecánica no invasiva mediante Helmet podría disminuir la necesidad de entubación endotraqueal en comparación con la oxigenoterapia convencional con mascarilla Venturi [108]. Un metanálisis de tres ensayos clínicos aleatorizados con 151 pacientes demostró que el uso de ventilación mecánica no invasiva en neumonía puede disminuir la necesidad de entubación endotraqueal, la mortalidad en terapia intensiva y el tiempo de hospitalización en la unidad de cuidados intensivos [109]. En el grupo de inmunodeprimidos, si bien la ventilación mecánica no invasiva pudo reducir la necesidad de entubación endotraqueal en pacientes con fiebre, infiltrado pulmonar e insuficiencia respiratoria aguda hipoxémica [110], el uso precoz de esta modalidad de soporte ventilatorio no invasivo, es decir, con menos de 72 horas después del inicio del fallo respiratorio; no fue capaz de disminuir la mortalidad a los 28 días de seguimiento en este mismo grupo de pacientes, en comparación con la oxigenoterapia convencional [111].
A pesar de que la oxigenoterapia por cánula nasal de alto flujo permite la administración de altas concentraciones de oxígeno y, debido al elevado flujo también permite alcanzar bajos niveles de presión positiva al final de la expiración, el principal estudio que comparó la oxigenoterapia por cánula nasal de alto flujo, la oxigenoterapia convencional y ventilación mecánica no invasiva no demostró diferencia en la tasa de entubación endotraqueal a los 28 días en pacientes con insuficiencia respiratoria aguda hipoxémica. Es importante resaltar que este mismo estudio encontró una menor mortalidad a los 90 días en el grupo de pacientes sometidos a oxigenoterapia por cánula nasal de alto flujo [112].
Tanto la oxigenoterapia por cánula nasal de alto flujo como la ventilación mecánica no invasiva son métodos de asistencia respiratoria ampliamente disponibles y, por lo tanto, están indicados en casos de neumonía adquirida en la comunidad con insuficiencia respiratoria hipoxémica aguda en el lugar de la oxigenoterapia convencional con el objetivo de evitar la entubación endotraqueal, cuando no hay necesidad de entubación inmediata [113]. Hasta el momento, no se dispone en la literatura de una comparación entre ventilación mecánica no invasiva y cánula nasal de alto flujo en la neumonía adquirida en la comunidad.
La ventilación mecánica invasiva puede ser necesaria en pacientes con neumonía grave adquirida en la comunidad. La entubación endotraqueal tardía de los enfermos con neumonía grave y fallo respiratorio agudo puede llevar a un incremento en la mortalidad [114]. En casos de neumonía adquirida en la comunidad con síndrome de estrés respiratorio agudo grave, se recomienda encarecidamente el uso de parámetros de ventilación mecánica protectora, es decir, con volúmenes corrientes bajos (de 4 a 8 mililitros por kilogramo) [115]. En pacientes con neumonía de menor gravedad, la estrategia protectora puede disminuir el riesgo de evolución a lesión pulmonar inducida por ventilación mecánica [116].
Conclusión
La morbimortalidad de la neumonía grave adquirida en la comunidad grave aún es elevada, principalmente entre ancianos, los portadores de enfermedades crónicas y los pacientes inmunodeprimidos. Es muy importante la adopción de medidas preventivas, como aumentar la tasa de vacunación de la población adulta y promover la cesación del consumo de tabaco. Las escalas pronósticas de gravedad pueden auxiliar en el diagnóstico de los casos más graves de neumonía adquirida en la comunidad, De esta forma, es posible ayudar en la definición de la pauta de tratamiento a seguir, ya sea en ambulatorio, hospitalario o en la unidad de cuidados intensivos. El inicio precoz del tratamiento antimicrobiano, especialmente en los casos más graves, es fundamental para mejorar la sobrevida y disminuir el riesgo de complicaciones relacionadas con la neumonía adquirida en la comunidad. Aunque diversos estudios muestran un beneficio en el uso de corticoides en el tratamiento de la neumonía grave, su uso sigue siendo controvertido, especialmente en los casos más leves y en algunas neumonías virales. El incremento de la incidencia de patógenos multirresistentes, así como el aumento de la edad poblacional con el coincidente crecimiento de la prevalencia de comorbilidades, son desafíos cada vez más presentes en la práctica clínica. Se necesitan nuevos estudios para evaluar la eficacia y eficiencia de los nuevos antimicrobianos en la neumonía adquirida en la comunidad causada por bacterias multirresistentes.

